
题目列表(包括答案和解析)
2.将石墨置于熔融的钾或气态的钾中,石墨会吸收钾而形成钾石墨,其结成可以是C8K、C24K、C36K和C48K。在钾石墨中,钾元素处于石墨层中间,因石墨层之间被胀大,层间的距离增加。下列对钾石墨的叙述中,不正确的是 ( D )
A.钾石墨中可能存在K+
B.钾石墨导电性比石墨强
C.钾石墨与水相遇,可能发生化学反应
D.C8K、C24K、C36K和C48K同属于同素异形体
1.许多环境问题是跨国界的,甚至是全球性的。根据《蒙特利尔议定书》的有关要求,我国政府采取了一系列措施来保护地球环境。如,2002年起我国汽车业全面禁用氟里昂(Freon)空调、2005年开始停止生产“哈龙(Halons)1211灭火器”等。下列环境问题中,由于大量使用氟里昂、哈龙等物质而导致的为( B )
A.酸雨 B.臭氧空洞 C.温室效应 D.光化学烟雾
31、(9分)向Cu与CuO的混合物中加入混酸(硝酸和硫酸)后加热,使之恰好完全反应,反应中不产生SO2和Cu(NO3)2,硝酸的还原产物只有NO,且得到NO8.96L(标准状况)。将溶液冷却后刚好全部结晶(无其它任何残留物),得到CuSO4·5H2O 250g。
求:(1)混酸中硝酸和硫酸的物质的量之比。
(2)原混合物中Cu和CuO的物质的量之比。
(3)混酸中硫酸的质量分数。
30.(6分)用密度为1.19g/cm3、质量分数为36.5%的浓盐酸252mL与足量的二氧化锰反应,生成的氯气在标准状况下的体积为16.8L。计算:
(1)在反应中被氧化的HCl的物质的量为多少?
(2)浓盐酸中HCl的物质的量浓度最小值为多少?
29.(10分)已知:①R-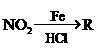 -
-
②苯环上原有的取代基对新导入的取代基进入苯环的位置有显著影响.当一取代苯进行取代反应时,新引进的取代基因受原取代基的影响而取代邻、对位或间位。使新取代基进入它的邻、对位的取代基:-CH3、-NH2;使新取代基进入它的间位的取代基:-COOH、-NO2;
以下是用苯作原料制备一系列化合物的转化关系图:

(1)A转化为B的化学方程式是______________________________________________。
(2)图中“苯→①→②”省略了反应条件,请写出①、②物质的结构简式:
①________________________,②_______________________________。
(3)B在苯环上的一氯代物有 种同分异构体。
(4)有机物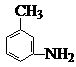 的所有原子 (填“是”或“不是”)在同一平面上。
的所有原子 (填“是”或“不是”)在同一平面上。
28.(10分)实验测得某烃中碳元素的质量分数为91.3%,相对分子质量为92,则该烃的分子式为____________。若该烃为芳香烃,在其分子的“C-C”键或“H-C”键中
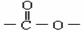
插入基团“ ”可形成六种含苯环的酯,请写出其中四种酯的结构简式:
__________________________________、____________________________________、
__________________________________、____________________________________。
27.(14分)已知在pH为4-5的溶液中,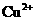 几乎不水解,而
几乎不水解,而 几乎完全水解。某学生拟用电解
几乎完全水解。某学生拟用电解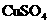 溶液的方法测定铜的相对原子质量.其实验流程图如下:
溶液的方法测定铜的相对原子质量.其实验流程图如下:
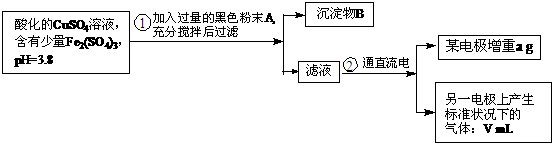
试回答下列问题:
(1) 步骤①中加入A的化学式为________,其作用是_____________;沉淀物B是________(填化学式)。
(2)步骤②中所用部分仪器如下图所示:则A应连接直流电源的________极,写出B电极上发生反应的电极方程式________________________________________。
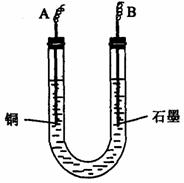
(3)下列实验操作属必要的是________(填字母)。
A.称量电解前电极的质量
B.电解后电极在烘干前,必须用蒸馏水冲洗
C.刮下电解后电极上的铜,并清洗、称量
D.电极在烘干称重的操作中必须按如下顺序:烘干→称重→再烘干→再称重进行两次
E.在空气中烘干电极,必须采用低温烘干法
(4)电解后向溶液中加入石蕊试液,观察到的现象是_________________________。
(5)铜的相对原子质量的计算式是_________________。
(6)从能量转化的角度来看,步骤②的变化是将________能转化为________能。
26.(6分)下列有关实验的叙述,正确的是(填序号)(少一个扣一分,多一个倒扣一分,扣完为止) 。
(A)配制500mL某物质的量浓度的溶液,可用两只250mL的容量瓶
(B)用渗析法分离淀粉中混有的NaCl杂质
(C)无法用分液漏斗将甘油和水的混合液体分离
(D)用酸式滴定管量取20.00mL高锰酸钾溶液
(E)为了测定某溶液的pH,将经水润湿的pH试纸浸入到待测溶液,过一会取出,与标准比色卡进行对比
(F)用浓氨水洗涤做过银镜反应的试管
(G)配制银氨溶液时,将稀氨水慢慢滴加到硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止
(H)浓硫酸不小心沾到皮肤上,立刻用稀NaOH溶液洗涤
(J)在氢氧化铁胶体中加少量硫酸会产生沉淀
(K)用结晶法可以除去硝酸钾中混有的少量氯化钠
25.(6分)高炉炼铁中发生的基本反应之一如下:FeO(固)+CO(气)≒Fe(固)+CO2(气)-Q ,其平衡常数可表达为 K=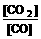 ,已知1100℃时,K=0.263 。
,已知1100℃时,K=0.263 。
(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO和体积比值
平衡常数K值 (本小题空格均备选:增大、减小或不变)
(2)1100℃时测得高炉中[CO2]=0.025mol/L [CO]=0.1mol/L,在这种情况下,该反应是否处于化学平衡状态 (选填是或否),此时,化学反应速度是V正 V逆(选填大于、小于或等于),其原因是___________________________________________________。
24.(12分)A、B、C、D均为4种常见的短周期元素,常温下A、B可形成两种常见的液态化合物,其最简式分别为BA和B2A;B与D可形成分子X,也可形成阳离子Y,X、Y在水溶液中酸、碱性正好相反,D元素气态氢化物的水溶液与其最高价氧化物的水化物的水溶液酸、碱性也相反;C+的焰色反应呈黄色。
(1)C元素在周期表中位于 __ 周期________族,C+ 离子的电子排布式为_______________________;D元素的最高价氧化物的水化物与其氢化物的水溶液互相反应的离子方程式 ____ ;阳离子Y与水反应的离子方程式为 ____ ;最简式为BA的分子的电子式可表示为_________________。
(2)M、N是由A、B、C、D四种元素中任意三种元素组成的不同类型的强电解质,M的水溶液呈碱性,N的水溶液呈酸性,且M溶液中水的电离程度小于N溶液中水的电离程度。 则M、N分别为(填化学式) ____ 、____________ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com