
题目列表(包括答案和解析)
5.下列各组离子在指定条件下,一定能大量共存的是
A.PH为1的无色溶液:K+、Fe2+、SO42-、NO3-、Cl-
B.能使碘化钾淀粉试纸变蓝的溶液:Na+、NH4+、S2-、Br-
C.水电离出的c(H+)=10-12mol/L的溶液:Ba2+、Na+、NO3-、Cl-
D.加入铝条有氢气放出的溶液:Na+、NH4+、HCO3-、NO3-
4.甲、乙两种物质的溶解度曲线如下图所示:下列说法一定正确的是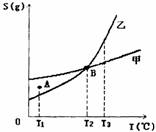
A.A点表示示T1℃时甲的溶液已饱和,乙的溶液未饱和
B.B点表示T2℃时甲、乙两物质的溶液均达饱和且两溶液的物质的量浓度相等
C.将T3℃(时甲、乙两物质的饱和溶液分)分别降温至T2℃,析出的乙比析出的甲多
D.若乙中含有少量的甲,可用重结晶的方法提纯乙
3.沼气是一种能源,它的主要成分是CH40.5molCH4完全燃烧生成CO2和H2O时,放出
445kJ热量,则下列热化学方程式中正确的是 ( )
A.2CH4 (g)+4O2 (g) = 2CO2 (g)+4H2O(l) △H=+890kJ·mol-1
B.CH4 (g)+2O2 (g) = CO2 (g)+2H2O(l) △H=+890kJ·mol-1
C.CH4 (g)+2O2 (g) = CO2 (g)+2H2O(l) △H=-890kJ·mol-1
D.1/2 CH4 (g)+O2 (g) = 1/2CO2 (g)+H2O(l) △H=-890kJ·mol-1
2.将石墨置于熔融的钾或气态的钾中,石墨会吸收钾而形成钾石墨,其结成可以是C8K、C24K、C36K和C48K。在钾石墨中,钾元素处于石墨层中间,因石墨层之间被胀大,层间的距离增加。下列对钾石墨的叙述中,不正确的是
A.钾石墨中可能存在K+ B.钾石墨与水相遇,可能发生化学反应
C.钾石墨导电性比石墨强 D.C8K、C24K、C36K和C48K同属于同素异形体
1.化学与科技、社会、生产密切结合,下列有关说法不正确的是
A.“乙醇汽油”的广泛使用能有效减少有害气体的排放
B.“无磷洗涤剂”的推广使用,能有效减少水体富营养化的发生
C.“无氟冰箱”取代“含氟冰箱”,对人类的保护伞--臭氧层起到保护作用
D.“海水淡化”可以解决“淡水供应危机”,向海水中加入净水剂明矾可以使海水淡化
24.硝酸工业生产中的尾气可用纯碱溶液吸收,有关的化学反应为:
2NO2 + Na2CO3 → NaNO2 + NaNO3 + CO2↑ ①
NO + NO2 + Na2CO3 → 2NaNO2 + CO2↑ ②
(1)(2分)根据反应①,每产生22.4L(标准状况下)CO2,吸收液质量将增加__________g。
(2)(3分)现有1000g 质量分数为21.2%的纯碱吸收液,吸收硝酸工业尾气,每产生22.4L(标准状况下)CO2时,吸收液质量就增加44g。计算吸收液中NaNO2 和NaNO3 的物质的量之比
23. 向100mL 3 mol·L-1的NH4Al(SO4)2溶液中逐滴加入
向100mL 3 mol·L-1的NH4Al(SO4)2溶液中逐滴加入
1 mol·L-1 Ba(OH)2溶液.
(1)(3分)写出当沉淀的总物质的量为最大值时的离子方
程式(用一个式子表示):
.
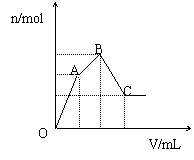
(2)(4分)随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化
如图所示.写出B点和C点所对应的Ba(OH)2溶液的体积:B mL,C mL.
22.(6分)国务院强调,“南水北调”工程必须坚持节水、治污和生态环境保护与工程建设相协调,以水资源合理配置为主线,把节水、治污、生态环境保护与调水作为一个完整的系统来分析的原则。在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患。检测某工厂废液中,含有大量的Mg2+、Al3+、Cu2+、Ag+。试分析回答下列问题:
(1)该废液中可能大量存在的一种阴离子是 (填序号)。
A.S042- B.NO3- C.Cl- D.CO32-
(2)经检测废液中铝元素的含量较高,需将其与其它三种离子分开,请选用合适的试剂,写出铝元素与该试剂反应时的离子方程式 。
(3)为了回收废液中的金属银,某同学设计了如下图所示的方案:
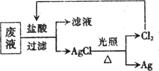
若依该方案获得Agl08g,为保证不污染环境和Cl2的循环利用,理论上应提供标准状况下的H2体积为 L。
21.(6分)A、B两元素,A的原子序数为X,A、B所在周期的元素数目分别为m和n,如A、B同在ⅠA族,当B在A的上周期时,B的原子序数为(1)____ ;
如A、B同在ⅦA族,当B在A的上周期时,B的原子序数为(2)__ ;当B在A的下周期,B的原子序数为(3) _ 。
20.(6分)同族元素的同类物质的结构、性质既有相似性,也有特殊性。回答下列问题:
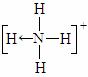 (1)已知酸性FCH2COOH>CH3COOH,试推断:①BrCH2COOH、②ClCH2COOH、③FCH2COOH的酸性由强到弱的顺序(填序号)_________________。
(1)已知酸性FCH2COOH>CH3COOH,试推断:①BrCH2COOH、②ClCH2COOH、③FCH2COOH的酸性由强到弱的顺序(填序号)_________________。
(2)已知P4、NH4+、N4H44+的空间构型均为四面体,NH4+的结构式为
(→表示共用电子对由N原子单方面提供)。
请画出N4H44+的结构式_____________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com