
题目列表(包括答案和解析)
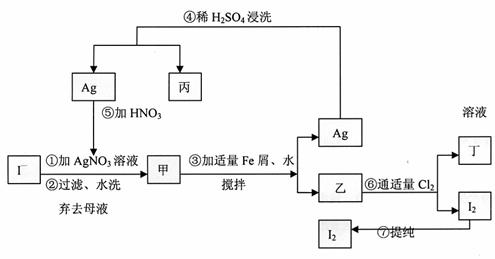 29.(14分)在已知提取氯化钠、溴、镁等化学物质的富碘卤水中,采用下面的工艺流程生产单质碘:
29.(14分)在已知提取氯化钠、溴、镁等化学物质的富碘卤水中,采用下面的工艺流程生产单质碘:
试回答:
(1)乙、丁中溶质的分子式:乙 ,丁 。
(2)第④步操作中用稀H2SO4浸洗的目的是 (填写字母编号)
a.除去未反应的NO3- b.除去未反应的I-
c.除去未反应的Fe d.除去碱性物质
(3)第⑦步操作可供提纯的两种方法是 和 (不要求写具体步骤)。
(4)实验室检验I2的方法是 。
(5)甲物质见光易变黑,其原因是(用化学方程式表示) 。
(6)(1)溶解银的硝酸应该用 硝酸(填浓或稀)。原因是
。
30.(共16分)
Ⅰ(6分)矿泉水一般是由岩石风化后被地下水溶出其可溶部分生成的。风化作用是指矿物与水和CO2同时作用的过程。例如:以下是黑云母(一种硅酸盐)这种矿物风化成高岭石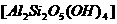 (一种硅酸盐)的反应为:
(一种硅酸盐)的反应为:
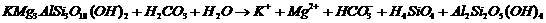 (未配平),回答下列问题:
(未配平),回答下列问题:
(1)把上述反应方程式配平的系数依次为
(2)上述反应发生的理由是 。
(3)地球化学中,通常用热重分析法研究矿物在受热时质量变化以确定其组成。加热黑云母到673K-1123K区间内分解为相应的氧化物,试计算黑云母失重的百分比为 (计算结果保留三位有效数字)
Ⅱ(10分)某化学反应的反应物和产物如下:
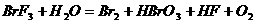
(4)该反应的氧化物是 。
(5)如果该反应方程式中HBrO3和O2的系数都是1,则
①HF的系数是 。
②在此方程式中,转移的电子数为 mol,被H2O还原的BrF3为 mol。
(6)如果没有对该方程式中的某些系数作限定,可能的配平系数有许多组。原因是
。
28.(共10分)有A、B、C、D、E、F、G,7瓶不同物质的溶液,它们各是Na2CO3、Na2SO4、
KCl、AgNO3、MgCl2、Ca(NO3)2和Ba(OH)2溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如表所示。表中“↓”表示生成沉淀或微溶化物,“-”表示观察不到明显变化,试回答下面问题。
(1)A的化学式是 ,G的化学式是 。判断理由是 。
(2)回答下列问题:
①写出B的电子式: 。
②写出C溶于水的电离方程式: 。
③写出用惰性电极电解F(熔融)在阳极的电极反应: 。
|
|
A |
B |
C |
D |
E |
F |
G |
|
A |
- |
- |
- |
- |
― |
- |
↓ |
|
B |
- |
- |
- |
- |
↓ |
↓ |
↓ |
|
C |
- |
- |
- |
↓ |
|
↓ |
↓ |
|
D |
- |
|
↓ |
- |
↓ |
↓ |
↓ |
|
E |
- |
↓ |
- |
↓ |
- |
↓ |
- |
|
F |
- |
↓ |
↓ |
↓ |
↓ |
- |
↓ |
|
G |
↓ |
↓ |
↓ |
↓ |
- |
↓ |
- |
27.(8分)将32.64g铜与140ml一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L。请回答:
(1)NO的体积为 L,NO2的体积为 L。
(2)待产生的气体全部释放后,向溶液加入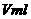 a mol·L-1的NaOH溶液,恰好使溶液中的
a mol·L-1的NaOH溶液,恰好使溶液中的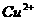 全部转化成沉淀,则远硝酸溶液的浓度为
mol/L。
全部转化成沉淀,则远硝酸溶液的浓度为
mol/L。
26.(10分)(1)把淀粉溶液溶于沸水中,制成淀粉胶体,回答下列问题。
①鉴别水溶液和胶体可以利用的方法是 。
②60℃左右时,在淀粉胶体中加入淀粉酶,充分反应。然后把反应后的全部液体装入半透膜袋里,系紧袋口,并把它悬挂在盛有蒸馏水的烧杯里。从半透膜里析出的物质是 ,该操作的名称是 。
(2)把少量的饱和氯化铁溶液滴入沸水中,制成Fe(OH)3胶体,回答下列问题。
③试写出上述反应的化学方程式 。
④向Fe(OH)3胶体中滴入硫酸直到过量,是描述此过程的实验现象
。
25.下列有机物互为同分异构体的有 ( )
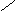
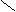
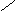
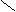 H
F
H
H
H
CH3
H
F
H
H
H
CH3
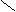
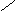
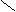
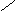
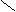
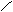 ① C === C ② C === C ③ C === C
① C === C ② C === C ③ C === C
H CH3 F CH3 H F
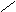
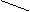
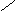
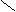
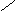
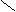 H3C
CH3
H3C F
F
CH3
H3C
CH3
H3C F
F
CH3
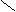
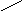
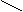
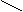
 ④ C === C ⑤ C === C ⑥ C === C
④ C === C ⑤ C === C ⑥ C === C
F F H3C F H3C F
A.①②③ B.④⑤⑥ C.①②③④⑤⑥ D.②③
第Ⅱ卷(非选择题,共80分)
24.已知t℃时,某物质的不饱和溶液a克中含溶质m克,若该溶液蒸发b克水并恢复到t℃
时,析出溶质m1克,若原溶液蒸发c克水并恢复到t℃时,则析出溶质m2克,用S表示
该物质在t℃时的溶解度,下式中正确的是 ( )
A. B.
B.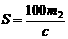
C.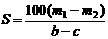 D.
D.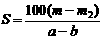
23.在下列离子方程式中正确的是 ( )
A.醋酸和小苏打溶液反应:H++HCO3-=CO2↑+H2O
B.硫氢化钠的水解:HS-+H2O = H3O++S2-
C.铁与三氯化铁溶液反应:Fe+Fe3+=2Fe2+
D.铝与氢氧化钠溶液反应:2Al+2OH-+2H2O=2AlO2-+3H2↑
22.如果定义有机物的同系一系列结构式符合A(W)NB(其中n=0,1,2,3……的化合物。
式中A、B是任意一种基因(或氢原子),W为2价有机基团,又称为该同系列的系差。
同系列化合物的性质往往呈现规律性变化。下列四组化合物中,不可称为同系列的是)
( )
A.CH3CH2CH2CH3 CH3CH2CH2CH2CH3 CH3CH2CH2CH2CH2CH3
B.CH3CH=CHCHO CH3CH=CHCH=CHCHO CH3 (CH=CH) 3CHO
C.CH3CH2CH3 CH3CHClCH2CH3 CH3CHClCH2CHClCH3
D.ClCH2CHClCCl3 ClCH2CHClCH2CHClCCl3 ClCH2CHClCH2CHClCH2CHClCCl3
20.向100mL含有等物质的量的NaCN、NaSCN和NaI混合液中滴入0.1mol液溴后,测得
有一半CN-已被氧化,则原溶液中NaSCN的物质的量浓度为多少? (已知①还原性
I->SCN->CN->Br- ②SCN- 和CN-的氧化产物为(SCN) 2和(CN) 2) ( )
A.4mol/L B.2mol/L C.1mol/L D.0.8mol/L
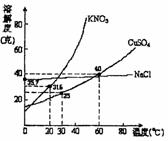 21.右图是几种盐的溶解度曲线,下列说法正确的是 ( )
21.右图是几种盐的溶解度曲线,下列说法正确的是 ( )
A.40℃时,将35克食盐溶于100克水中,
降温至0℃时,可析出氯化钠晶体
B.20℃时,硝酸钾饱和溶液的质量分数是31.6%
C.60℃时,200克水中溶解80克硫酸铜
达饱和,当降温至30℃时,可析出30
克硫酸铜晶体
D.30℃时,将35克硝酸钾和35克食盐
同时溶于100克水中,蒸发时,先析出的是氯化钠
19.已知Co2O3在酸性溶液中易被还原成Co2+、Co2O3、Cl2、FeCl3、I2的氧化性依次减弱。
下列反应在水溶液中不可能发生的是 ( )
A.3Cl2+6FeI2 ==== 2FeCl3+4FeI3
B.Cl2+FeI2 ==== FeCl2+I2
C.Co2O3+6HCl ==== 2CoCl2+Cl2↑3H2O
D.2Fe3++2I- ==== 2Fe2++I2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com