
题目列表(包括答案和解析)
7、NA为阿伏加德罗常数,下列叙述正确的为( )
A,标准状况下,22. 4LN2含共用电子对数为。
B,常温常压下,1molH2含共价键个数为NA。
C,常温常压下,18.0g重水(D2O)所含的电子数为10NA。
D,1molCH3CH2CH(CH3)2所含甲基个数为2NA。
6、城市大面积绿化既能美化城市,又能净化城市,还能控制温室效应,其控制温室
效应的化学依据是( )
A,某些绿色植物可以吸收SO2
B,植物根系发达可以防止水土流失
C,绿色植物可以吸收转化CO2气体,降低空气中CO2浓度
D,森林覆盖可以防起风,阻挡流沙作用
31.乙肝病毒的结构像汤丸,外有囊膜,内有较厚的蛋白质外壳,中心是双链DNA。乙肝病毒感染肝细胞以后,在肝细胞内可复制出许多病毒颗粒,从而损害肝细胞的机能,严重影响人体健康。回答有关问题:
(1)侵入人体肝细胞的是乙肝病毒的 。
(2)乙肝病毒的衣壳外面有囊膜包被,因此,当这些病毒侵入人体后,需要_________
细胞的处理,将内部的______暴露出来,才能刺激B淋巴细胞形成效应B细胞产生抗体。
(3)由乙肝病毒外壳蛋白颗粒制成的乙肝疫苗注射入人体后,不仅不会使人致病,还能诱发人体产生抵抗乙肝病毒感染的抗体,原因是_______________________ 。
(4)抗体在效应B细胞的_____上翻译出来后,进入_____中进行加工,如折叠、___、____等,才能成为比较成熟的蛋白质;在此过程中所需要的能量由_______提供。抗体与乙肝病毒特异性结合后,可以使乙肝病毒失去_____________的能力。
(5)氨基酸代谢中的氨基转换作用主要在肝脏进行,作为肝功检查指标的“转氨酶”主要是谷丙氨酸转氨酶(ALT)和天门冬氨酸转氨酶(AST)。这两种酶主要存在于( )
A.肝细胞细胞质
B.肝细胞周围的组织液
C.肝脏内的血液
D.胆汁
30. (20分)糖尿病是人类的常见病,发病率有上升的趋势。下图是人体内的血糖平衡调节示意图,请据图回答问题:
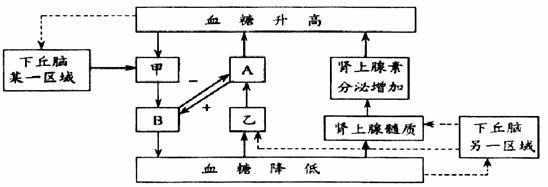
(1)糖尿病患者主要是图中[ ]_________细胞受损,使[ ]________分泌不足,______________________________________________发生障碍,使细胞内能量供应不足,导致__________、________分解加强,所以病人出现机体逐渐消瘦,体重减轻的症状。
(2)图中物质A的作用机理是促进________分解和__________的转化。
(3)在病理条件下,如果病人的血糖含量低于45mg/dl时,脑组织就会因得不到足够的能量供给而发生功能障碍,这时应及时给患者________。
(4)糖尿病人的“三多”症状中出现尿量多的原因是_________________________。
(5)体检时,测量血糖浓度应在空腹时进行,其生理学理由是________________。
29.(18分)有原子序数依次增大的4种短周期元素X、Y、Z、W,已知:
①X与Z、Y与W分别同主族;
②X、Z、W分别与Y都能形成两种常见的化合物;
③Y的阴离子与Z的阳离子的核外电子排布相同;
④这4种元素的单质中有一种易溶于CS2。
(1)这4种元素的单质由固态转变为液态时,有化学键被破坏的一种是(写化学式)____________。
(2)若把X2Y2看成二元弱酸,请写出常温下X2Y2与X2Y组成的混合物中存在的微粒:_________________________。
(3)写出由Y与Z形成的化合物Z2Y2的电子式________,其化学键类型有____________________。
(4)写出均由这4种元素组成的两种化合物在水溶液中发生反应的离子方程式:__________________________________ 。
(5)X、Y两种元素的单质已被应用于美国的阿波罗宇宙飞船的燃料电池中,如图所示,两个电极均由多孔性碳构成,通入的两种单质由孔隙逸出并在电极表面放电。
①a是电池的_________极;
②b电极上的电极反应式是:________________________。
③如果外电路中通过了4mol电子,则消耗X的体积为多少L(标况下)
28.(16分)为了测定已部分变质的过氧化钠样品的纯度,设计如图所示的实验装置,图中Q为弹性良好的气球,YC称取一定量的样品放入其中,按图安装好仪器,打开了漏斗的活塞,将稀硫酸滴入气球中。请填空:
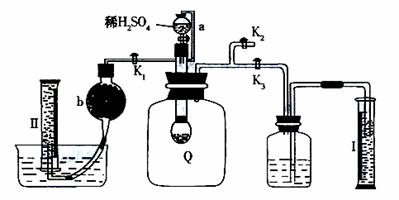
(1)Q内发生化学反应时,生成的气体是 。
(2)为了测定反应生成气体的总体积,滴加稀硫酸之前,K1、K2、K3中应当关闭的是
,应当打开的是 。
(3)当上述反应停止,将K1、K2、K3均处于关闭状态,然后先打开K2,再缓缓打开K1,这时可观察到的现象是: 。
(4)b中装的固体试剂是 ,为什么要缓缓打开K1?
(5)实验结束时,量筒I中有xmL水,量筒II中收集到ymL气体(已折算成标准状态)则过氧
化钠的纯度的数学表达式是 (化成最简表达式)。
27.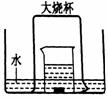 (10分)示的实验装置中,盛有足量水的水槽里放两个烧杯,小烧杯里放有少量铜片和过量浓硝酸,小烧杯外面倒扣一大烧杯,请回答下列问题:
(10分)示的实验装置中,盛有足量水的水槽里放两个烧杯,小烧杯里放有少量铜片和过量浓硝酸,小烧杯外面倒扣一大烧杯,请回答下列问题:
(1)实验过程中,观察到的主要现象是:
①___________________________________;
②___________________________________;
③___________________________________;
④___________________________________。
(2)用该装置做铜与浓硝酸反应的实验,最突出的优点是:
(3)若要验证最终得到的气体生成物,最简便的方法是:
26.(16分)下图A-J分别代表有关反应中的一种物质,它们均为中学化学中的常见物质.已知A-E和F-J中分别含有同一种元素.反应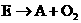 的条件未标出.
的条件未标出.
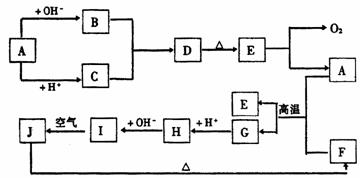
请填写下列空白:
(1)化合物H中的阳离子是_________;D的化学式为_________.
(2)A生成B反应的离子方程是_________________________________.
(3)B,C生成D的离子方程式是 .
(4)A和F的混合物叫做_________,发生反应的化学方程式是__________________.
(5) I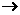 J反应的化学方程式是____________________________________,
J反应的化学方程式是____________________________________,
该反应过程中发生的现象是__________________________________________.
25.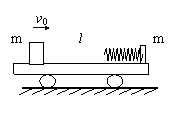 (21分)如图12所示,在光滑的水平面上有一质量为m、长度为l的小车,小车左端有一质量也是m可视为质点的物块。车子的右壁固定有一个处于锁定状态的压缩弹簧(弹簧长度与车长相比可忽略),物块与小车间动摩擦因素为μ,整个系统处于静止。现在给物块一个水平向右的初速度v0, 物块刚好能与小车右壁的弹簧接触,此时弹簧锁定瞬间解除,当物块再回到左端时,与小车相对静止。
(21分)如图12所示,在光滑的水平面上有一质量为m、长度为l的小车,小车左端有一质量也是m可视为质点的物块。车子的右壁固定有一个处于锁定状态的压缩弹簧(弹簧长度与车长相比可忽略),物块与小车间动摩擦因素为μ,整个系统处于静止。现在给物块一个水平向右的初速度v0, 物块刚好能与小车右壁的弹簧接触,此时弹簧锁定瞬间解除,当物块再回到左端时,与小车相对静止。
求:(1)物块的初速度;
(2)在上述整个过程中小车相对地面的位移。
24.(20分)如图所示,在竖直平面内建立xOy直角坐标系,Oy表示竖直向上的方向。已知该平面内存在沿x轴负方向的区域足够大的匀强电场,现有一个带电量为2.5×10-4C的小球从坐标原点O沿y轴正方向以0.4kg.m/s的初动量竖直向上抛出,它到达的最高点位置为图中的Q点,不计空气阻力,g取10m/s2.
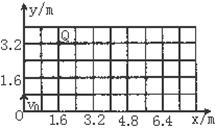 (1)指出小球带何种电荷;
(1)指出小球带何种电荷;
(2)求匀强电场的电场强度大小;
 (3)求小球从O点抛出到落回x轴的过程中电势能的改变量.
(3)求小球从O点抛出到落回x轴的过程中电势能的改变量.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com