
题目列表(包括答案和解析)
22.氯酸(HClO3) 是一种强酸,氯酸的浓度超过40%,就会迅速分解,产生比它的酸性更强的含氧酸,同时放出气体,该气体混合物经干燥后,平均相对分子质量为47.6,它可以使带火星的木条复燃,并可使润湿的淀粉一碘化钾试纸变蓝后又褪色。试完成下列各题:(已知有关物质的氧化性顺序为:Cl2>IO3->I2)
(1)该气体的组成是________________,气体混合物的物质的量比为 。
(2)写出氯酸分解方程式并配平

 该反应的还原产物是________________ (写化学式)
该反应的还原产物是________________ (写化学式)
(3)结合化学反应方程式解释,该气体使润湿的淀粉一碘化钾试纸变蓝后又褪色的原因:______________________________,___________________________________。
21. 据著名网站-网易报道,意大利科学家使用普通氧分子和带正电的氧化离子作用,制出
了新型的氧分子O4,它的结构很复杂,可能具有与S4相似的长方形结构。
(1)下列有关O4的说法正确的是
A.O4分子内存在极性共价键
B.合成O4的反应可看作核聚变反应,即不属于化学变化
C.O4与O3、O2都是氧的同素异形体
D.O4将来可用作更强有力的火箭推进的氧化剂
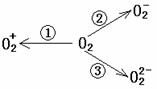 (2)制备O
(2)制备O 、O
、O 甚至O
甚至O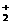 的化合物是可能存在的,通常它们是在氧分子进行下列各种反应时生成的:
的化合物是可能存在的,通常它们是在氧分子进行下列各种反应时生成的:
上述反应中, (填序号)相当于氧分子的氧化; (填序号)相当于氧分子的还原。
(3)写出O22-的电子式: 。
(4)O2[PtF6]是一种含有O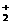 的化合物,请写出一种含有O
的化合物,请写出一种含有O 的氧化物的化学式:
的氧化物的化学式:
20. 设NA为阿伏加德罗常数。下列说法正确的是
①标准状况下,22.4 L SO3所含分子数为NA。 ②常温常压下,16 g O2和O3的混合气体所含氧原子数为NA。 ③12.5 mL 16 mol·L-1浓硫酸与足量铜反应,转移电子数为0.2 NA。 ④含1molFeCl3的溶液中,Fe3+离子的数目为NA。 ⑤7.8 g Na2O2含有的阴离子数目为0.1 NA。 ⑥0.05mol熔融的KHSO4中含有0.1NA个阳离子。 ⑦4 g重水(D2O)中所含质子数为2 NA。 ⑧电解精炼铜时转移0.1NA个电子时阳极溶解3.2g铜。
19.新浪网曾经报道,重庆开县发生特大井喷事故,造成大量人员牲畜伤亡。其中罪魁祸首是喷出大量的有毒气体H2S,为了解毒,政府采用了点燃的方法,写出完全燃烧的化学方程式 ,但是会造成空气污染,易形成________。
18.在含大量I-的溶液中,因发生氧化还原反应而不能大量共存的时是( )
A.Mg2+、Ag+、HCO3-、Cl- B.H+、AlO2-、Cl-、SO42-
C.K+、Fe3+、SO42-、Br- D.H3O+、Ca2+、Cl-、NO3-
第Ⅱ卷(共56分)
17.由一种阳离子与两种酸根离子组成的盐称为混盐。混盐CaOCl2在酸性条件下可以产生
Cl2。下列关于混盐CaOCl2的有关判断不正确的是( )
A.该混盐与硫酸反应产生1 mol C12时转移2NA个电子
B.该混盐的水溶液呈中性
C.该混盐具有较强的氧化性
D.该混盐中的氯元素的化合价为+1和-1
16.下列实验过程中产生的现象与对应的图形相符合的是 ( )
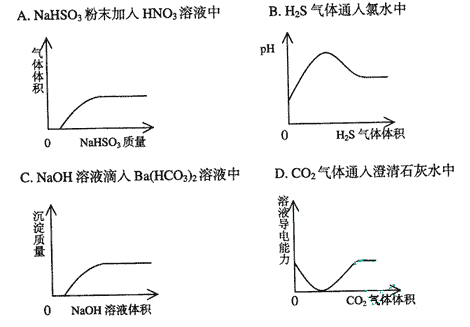
15.常温下跟镁粉、溴水、臭氧、硝酸都能发生氧化还原反应的是( )
A.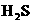 溶液 B.
溶液 B. 溶液 C.
溶液 C.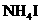 溶液 D.NaOH溶液
溶液 D.NaOH溶液
14.
 下列有关气体体积的叙述中,正确的是( )
下列有关气体体积的叙述中,正确的是( )
A.在一定的温度和压强下,各种气态物质体积大小由构成气体分子大小决定
B.在一定的温度和压强下,各种气态物质体积的大小由构成气体的分子数决定
C.不同的气体,若体积不同,则它们所含的分子数一定不同
D.气体摩尔体积是指1 mol任何气体所占的体积约为22.4L
13.关于某无色溶液中所含离子的鉴别,下列判断正确的是( )
A.加入AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有Cl-存在
B.加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有SO42-存在
C.通入Cl2后,溶液变为黄色,加入淀粉溶液后溶液变蓝,可确定有I-存在
D.加入盐酸,生成的气体能使澄清石灰水变浑浊,则原溶液中一定有大量CO32-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com