
题目列表(包括答案和解析)
13、物质X(□)和物质Y(〇)的反应中微粒之间的关系如下图所示,对该反应的描述,下列反应方程式正确的是 ( )
 A. 3X+8Y→X3Y8
A. 3X+8Y→X3Y8
B. 3X+8Y→3XY2+2Y
C. 3X+6Y→X3Y6
D. X+2Y→XY2
12、在周期表主族元素中,X元素位于第二周期,且分别与Y、Z、W三元素相邻,X、Y的原子序数之和等于Z的原子序数;这四种元素原子的最外层电子数之和为20。下列判断正确的是
A.原子序数:Z>Y>X>W
B.X、Y、Z、W形成的单质最多有6种
C.X元素最高价氧化物对应水化物的化学式为:H3XO4
D.四种元素的气态氢化物中,W的气态氢化物最稳定
11、甲醇(CH3OH)燃料电池可用于笔记本电脑、汽车等,一极通入甲醇,另一极通入氧气,电池工作时,H+由负极移向正极。下列叙述正确的是
A.氧气为负极 B.甲醇为负极
C.正极反应为:O2+4H++4e-== 2H2O D.负极反应为:CH3OH+H2O+6e- == CO2↑+ 6H+
10、某温度下,已知反应mX(g)+ nY(g)  qZ(g) △H>0,m+ n>q,在体积一定的密闭容器中达到平衡,下列叙述正确的是
qZ(g) △H>0,m+ n>q,在体积一定的密闭容器中达到平衡,下列叙述正确的是
A.反应速率υ正(X) =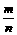 υ逆(Y) B.加入X,反应的△H增大
υ逆(Y) B.加入X,反应的△H增大
C.增加Y的物质的量,X的转化率增大 D.降低温度,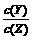 的值变小
的值变小
9、下列化学反应的离子方程式正确的是
A.氢氧化镁中滴加盐酸: H+ + OH-== H2O
B.碳酸氢钙溶液中加入氢氧化钠溶液: HCO3- + OH-== CO32- + H2O
C.金属铝溶于氢氧化钠溶液: 2Al + 6OH- == 2AlO2- + 3H2↑
D.用FeCl3溶液腐蚀铜电路板: 2Fe3++ Cu == 2Fe2++ Cu2+
24、(7分)某结晶水合物含有两种阳离子和一种阴离子。称取两份质量均为1.96g的该结晶水合物,分别制成溶液。一份加入足量Ba(OH)2溶液,生成白色沉淀,随即沉淀变为灰绿色,最后带有红褐色;加热上述所得液体,逸出能使湿润的红色石蕊试纸变蓝的气体;用足量稀盐酸处理沉淀物,经洗涤和干燥,得到白色固体2.33g。另一份加入含0.001mol KMnO4的酸性溶液,MnO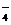 恰好完全被还原为Mn2+。请回答以下问题:
恰好完全被还原为Mn2+。请回答以下问题:
(1)该结晶水合物中含有的两种阳离子是 和 ,阴离子是
(2)该结晶水合物的化学式为
(3)取该结晶水合物溶于水配成浓度为A mol/L的溶液,另有浓度为B mol/L的(NH4)2SO4溶液及C mol/L的(NH4)2CO3溶液,欲使三份溶液的NH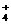 浓度相等,A、B、C的相对大小关系为
。
浓度相等,A、B、C的相对大小关系为
。
23、(14分) 已知:①一定条件下,R1-Cl+2Na+R2-Cl→R1-R2+2NaCl;②醛和醇可以发生氧化反应,相关物质被氧化的难易次序是:RCHO最易,R-CH2OH次,R1-(CHOH)-R2最难。已知A为卤代烃,含碳的质量分数为45.86%,含氢元素的质量分数为8.91%,其余为卤元素;B与氯气反应生成的一氯代物有两种,有关的转化关系如图所示(部分产物及条件已略去)

|
|
|
|
|
|
|
|
|




 氧化
氧化
△
氧化
氧化
△
|
|
|
|
|


 浓H2SO4
浓H2SO4
请回答下列问题;
(1)B的结构简式 F的结构简式
(2)I中含有的官能团 (写名称)
(3)反应方程式:H→I ,J→K
(4)请写出D的同分异构体中属于羧酸具有2个-CH3的结构简式
21. (12分)A、B、C、D、E为含同一种元素的常见物质。C物质只由一种元素组成,在每一个C分子中形成共价键的电子数与分子中所含电子数之比为3:7。C和E均可与氧气在一定条件下反应生成A。F是一种常见的还原剂,却是一种能被浓硫酸干燥的气体,请回答以下问题:
(1)常温下将气体B通入水中发生反应,生成A和D,则D为 。
(2)E分子的空间构型是 ;写出E与氧气反应生成A的化学方程式
(3)用电子式表示E的形成过程
(4)D和E生成的化合物在某温度下加热分解,只生成两种氧化物,且在此过程中,若有0.5mol该化合物完全反应,转移电子数2mol。写出该反应的化学方程式:
(5) 某温度下,向某恒压密闭容器中加入相对平均分子质量为8.5的混合气体C和F共4mol使之反应合成E,达平衡后测得E的体积分数为m.保持外界条件不变,只改变起始物质的加入量使反应重新达到平衡后,E的体积分数仍为m.
①若C物质、F物质、E物质的加入量分别用X、Y、W表示,则X、Y、W应满足的关系是
②若使该反应向生成E的方向移动,可采取的措施有(填字母符号)
A、升高温度 B、增大压强 C、使用催化剂 D、液化分离E
|
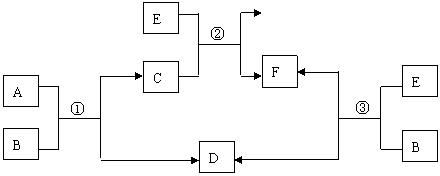
(1) 若反应①、②、③均为水溶液中的置换反应, A、D、E为卤素单质,则A、D、E的氧化性由强到弱的顺序为 (用字母表示),A的化学式是 。
(2)若B是水,C是一种有磁性的化合物,E是一种无色、无味的有毒气体,则反应②的化学方程式是 。
(3)若B为一种淡黄色固体,绿色植物的光合作用和呼吸作用可实现自然界中D和E的循环。反应①的离子方程式是 .在反应③中,若生成1molD,则转移电子数目为 .
20、(10分)图中表示了另一种将CO2转化为O2的实验设想:
|
|

|

|
|
 CO2
CO2

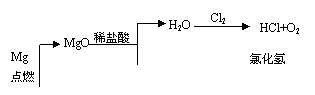
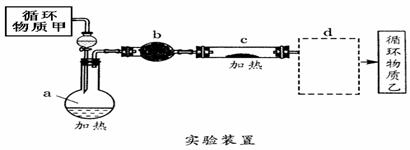 其中,由MgCl2•6H2O制取无水MgCl2的部分装置(铁架台、酒精灯已略)如图所示:
其中,由MgCl2•6H2O制取无水MgCl2的部分装置(铁架台、酒精灯已略)如图所示:

①图中,装置a由 、 双孔塞和导管组成;
②循环物质的名称是 ;
③制取无水氯化镁必须在氯化氢存在的条件下进行,原因是 ;
④装置b中填充的物质可能是 (填入编号)。
A、五氧化二磷 B. 碱石灰 C.无水氯化钙 D.浓硫酸
⑤设计d装置要注意防止倒吸,请在方框中画出d装置的简图,并要求与装置c的出口处相连(铁架台不必画出).
19、(3分)下列实验操作正确的是
(1)将未经湿润的PH试纸浸到某溶液中,过一会取出与标准比色卡比较测得该溶液的PH值。
(2)使用酸式滴定管盛装KMnO4溶液滴定Na2SO3溶液
(3)将3滴90%浓硫酸滴入蓬松的脱脂棉中搅拌加热,稍冷,再向其中加入2%CuSO4溶液,再加入过量的10%NaOH溶液,并加热至沸腾,可证明纤维素的水解。
(4)直接加热乙醛和银氨溶液的混合液做乙醛的银镜实验.
(5)向蛋白质溶液中加入无机盐(如Na2SO4、(NH4)2SO4)浓溶液,可使蛋白质盐析而分离提纯.
(6)实验室制肥皂时,将适量植物油、乙醇和NaOH溶液混合,并不断搅拌、加热,直到混合物变稠,再经过盐析、分液……等几步处理即可得到肥皂。
(7)配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加浓硫酸.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com