
题目列表(包括答案和解析)
11. 25℃时,将pH=x的H2SO4溶液与pH=y的NaOH溶液按体积比1∶100混合,反应后所得溶液pH=7。若x=y/3,则x的值为(B)
A.2 B.3 C.4 D.5
10.用1.0 mol·L-1的NaOH溶液滴定某浓度的硫酸,下列操作会使测定结果偏低的是(B)
A.滴定开始时,碱式滴定管内有气泡,滴定过程中气泡消失
B.起始读数仰视
C.滴定结束时,还有1滴NaOH溶液挂在尖嘴上
D.用蒸馏水将锥形瓶瓶壁的H2SO4冲下
9. 100 mL浓度为2 mol/L的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成的氢气的总量,可采用的方法是 (B)
A.加入适量的6mo1/L的盐酸 B.加入数滴氯化铜溶液
C.加入适量蒸馏水 D.加入适量的氯化钠溶液
8.某酸式盐NaHY的水溶液显碱性,下列叙述错误的是(A)
A. H2Y的电离方程式:H2Y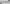 2H++Y2-
2H++Y2-
B. HY-水解的离子方程式:HY‑ + H2O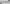 H2Y+OH-
H2Y+OH-
C.该酸式盐溶液中离子浓度大小关系:c(Na+)>c(HY-)>c(OH‑)>c(H+)
D.该酸式盐溶液中离子浓度关系:c(H+)+c(H2Y)-c(Y2-)=c(OH-)
[解析] NaHY的水溶液显碱性,HY-的水解大于电离,又HY-电离的存在,根据质子守恒有:c(H+)+c(H2Y)=c(OH-)+c(Y2-)
7.下列事实用勒夏特列原理不能解释的是(C)
A.实验室制取乙酸乙脂时,边加热边蒸馏以提高乙酸乙脂的产率
B.实验用排水法收集Cl2时,用饱和食盐水代替水以减少Cl2的溶解
C.实验室保存FeSO4溶液时,加入几枚铁钉以防止变质
D.工业生产硫酸时,通入过量的空气以提高SO2的利用率
6.下列物质发生反应时其离子方程式错误的是(D)
A.铁与三氯化铁溶液反应:Fe+2Fe3+=3Fe2+
B.足量的氯气通人嗅化亚铁溶液中2Fe2++4Br-+3Cl2=2Fe3+ +2Br2+6C1-
C. Fe(OH)3跟盐酸反应:Fe(OH)3+3H+=Fe3++3H2O
D. FeS跟稀硝酸反应:FeS+2H+=Fe2++H2S↑
5.将NH4NO3溶解于水中,为了使该溶液中的NH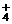 和NO
和NO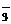 离子的物质的量浓度之比等于1∶1,可以采取的正确措施为(B)
离子的物质的量浓度之比等于1∶1,可以采取的正确措施为(B)
A.加入适量的硝酸,抑制NH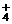 的水解
的水解
B.加入适量的氨水溶液,使溶液的pH=7
C.加入适量的NaOH溶液,使溶液的pH=7
D.加入适量的NaNO3溶液,抑制NH4NO3的电离
4.若溶液中由水电离产生的c(OH-)=1 X 10-14mol·L-1,满足此条件的溶液中一定可以大量共存的离子组是(B)
A.Al3+ Na+ NO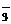 Cl- B. K+ Na+ Cl- NO
Cl- B. K+ Na+ Cl- NO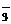
C.K+ Na+ Cl- AlO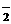 D.
K+ NH
D.
K+ NH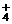 SO
SO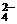 NO
NO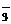
3.把1L pH=3的醋酸溶液加水稀释至10 L后,下列叙述中正确的是(A)
A电离程度增大 B.c(H+)增大
C.导电能力增强 D.c(CH3COO-)增大
2.能说明镁比铝还原性强的事实是(B)
A. Mg的价电子比铝少
B.镁带在空气中和CO2中能燃烧,而铝不能
C. Mg遇浓硫酸不钝化,而铝钝化
D.铝的硬度、延展性、熔点均比镁大、好、高
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com