
题目列表(包括答案和解析)
23.(8分)北京东方化工厂生产的某产品只含C、H、O三种元素,其分子模型如下图所示
 (图中球与球之间的连线代表化学键,如单键、双键等)。
(图中球与球之间的连线代表化学键,如单键、双键等)。
(1)该产品的结构简式为 ,
分子式为 。
(2)下列物质中,与该产品互为同分异构体的是
(填序号),与该产品互为同系物的是
(填序号)。
①CH3CH=CHCOOH ②CH2=CHCOOCH3
③CH3CH2CH=CHCOOH ④CH3CH(CH3)COOH
(3)在一定条件下,该产品跟乙二醇反应可得到分子式为C6H10O3的物质,该物质发生加聚反应可得到用来制作隐形眼镜的高分子材料,这种高聚物的结构简式为 。
22.(10分)A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略
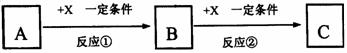 去)。
去)。
试回答:
(1)若X是强氧化性单质,则A不可能是 。
a.S b.N2 c.Na d.Mg e.Al
(2)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的化学式为 ;C溶液在贮存时应加入少量X,理由是(用必要的文字和离子方程式表示) ,检验此C溶液中金属元素价态的操作方法是 。
(3)若A、B、C为含金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式为 ,X的化学式可能为(写出不同类物质) 或 ,反应①的离子方程式为 或 。
21.(10分)A、B、C、D、E为短周期元素,原子序数依次增大。其中A与E同主族,B的最外层电子数是次外层电子数的2倍,C的最高价氧化物对应的水化物与其氢化物反应生成一种盐X。A、B、D、E可组成化合物A2D2、B2A2、E2D2,它们都含有非极性共价键。
(1)C元素在周期表中的位置是 ,写出B的最高价氧化物的电子式 。
(2)X的水溶液显 (填“酸”、“碱”或“中”)性,理由是(用离子方程式表示) ,溶液中各种离子浓度由大到小的顺序为 。
(3)A、B、D、E四种元素组成的化合物中原子个数最少的化合物的化学式为 。
(4)炎箭推进器中装有液态的C2A4和液态A2D2,它们发生化学反应时生成气态C单质和水蒸气,并放出大量热。已知0.4mol液态C2A4跟液态A2D2完全反应时,放出256.6kJ热量,该反应的热化方程式为 。
20.(6分)目前世界上比较先进的电解制碱技术是离子交换膜法。
(1)电解法制烧碱的主要原料是饱和食盐水。由于粗盐水中含有泥沙、Ca2+、Mg2+、Fe3+、SO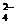 等杂质,因此必须经过精致才能进行电解。除去这些杂质时,不应选用的试剂是
(填序号)。
等杂质,因此必须经过精致才能进行电解。除去这些杂质时,不应选用的试剂是
(填序号)。
a.BaCl2 b.Na2CO3 c.NaOH d.盐酸 e.KOH
(2)现有200mL食盐水,用石墨电极电解。当阴极产生气体的体积为0.224L(标准状况)时停止电解,阳极的电极反应式为 ,电解后,溶液在常温下的pH约为 (忽略体积变化)。
19.(4分)铁酸钠(化学式为Na2FeO4)是一种新型净水剂,工业上常通过如下化学反应制取:Fe2O3+3NaNO3+4NaOH=2Na2FeO4+3NaNO2+2H2O。
(1)反庆中,氧化剂为 。
(2)当生成4mol Na2FeO4时,电子转移总数为 mol。
18.某温度下,向50g水中加入m g CuSO4或加入n g CuSO4·5H2O,均可使溶液恰好达到饱和,则m与n的关系为 ( )
A.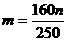 B.
B.
C.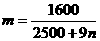 D.
D.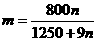
|
17.25℃时,某溶液中由水电离产生的c(H+)和c(OH-)的乘积为1×10-18,下列说法正确的是 ( )
A.该溶液的pH可能是7 B.此溶液不存在
C.该溶液的pH一定是9 D.该溶液可能pH=5
16.右图为实验室制取少量乙酸乙酯的装置图。下列关于该实验的叙述中,不正确的是( )
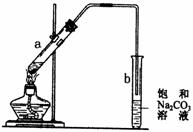 A.向a试管中先加入浓硫酸,然后边摇动试管
A.向a试管中先加入浓硫酸,然后边摇动试管
边慢慢加入乙醇,再冰醋酸
B.试管b中导气管下端管口不能浸入液面的目
的是防止实验过程中产生倒吸现象
C.实验时加入试管a的目的之一是及时将乙酸
乙酯蒸出,使平衡向生成乙酸乙酯的方向移动
D.试管b中饱和Na2CO3溶液的作用是吸收随乙
酸乙酯蒸出的少量乙酸和乙醇
15.元素周期表中的短周期元素X和Y,可组成化合物XY3,下列说法正确的是 ( )
A.XY3一定是离子化合物
B.若Y的原子序数为m,则X的原子序数一定为m±4
C.X和Y可属同一周期,也可属不同周期
D.X和Y一定不属于同一主族
14.向含Fe3+、Fe2+、Mg2+、NH4+的水溶液中,加入足量的Na2O2固体,充分反应后再加入过量的稀盐酸,上述离子数目没有变化的是 ( )
A.Fe2+ B.NH4+ C.Fe3+ D.Mg2+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com