
题目列表(包括答案和解析)
20.(6分)实验室为验证同主族元素性质递变规律,准备了如下药品:
①AgNO3溶液 ②K ③Br2水 ④I2水 ⑤NaOH溶液
⑥NaCl溶液 ⑦NaBr溶液 ⑧H2O ⑨Na ⑩Mg
(1) 你准备选用的药品是(用编号表示)____________
(2) 你所做的实验是什么?(用方程式表示)判断依据是什么?
_________________________________________________________________
__ _
班别 姓名 考号
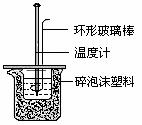
19.(10分)实验室用50 mL0.50 mol/L盐酸、50 mL0.55 mol/LNaOH溶液和下图所示装置进行测定中和热的实验,得到表中的数据:
|
实验次数 |
起始温度t1/℃ |
 终止温度 终止温度t2/℃ |
|
|
盐酸 |
NaOH溶液 |
||
|
1 |
20.2 |
20.3 |
23.7 |
|
2 |
20.3 |
20.5 |
23.8 |
|
3 |
21.5 |
21.6 |
24.9 |
试回答下列问题: (1)实验时用环形玻璃棒搅拌溶液的方法是_____________________________,
不能用铜丝搅拌棒代替环形玻璃棒的理由是_______________________。
(2)经数据处理,t2-t1=3.4 ℃。则该实验测得的中和热ΔH = ________________ [盐酸和NaOH溶液的密度按1 g/cm3计算,反应后混合溶液的比热容(c)按4.18 J/(g•℃)计算]。
(3)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热为ΔH1,则ΔH1与ΔH的关系为:ΔH1____________ΔH(填“<”、“>”或“=”=,理由是____________________________________________________。
18. (16分)已知A、B、C、D、E、F六种物质之间有如图所示的转化关系,其中固体X是E受热分解反应的催化剂。

(1)试写出各物质的化学式
A B C D E F
(2)a mol A无论按途径(Ⅰ),还是按途径(Ⅱ),只要完全反应,最终产生F的物质的量均为 mol,请从得失电子守恒的角度分析其原因
17.(12分)有A、B、C、D四种元素。常温下A的单质是深红棕色的液体。B、C.D是短周期元素。D元素原子K层的电子数是B元素原子核外电子数的两倍。C、D元素原子最外层电子数相同,C元素原子核内质子数是D元素原子核内质子数的1/2。
(1)各元素的符号是A: 、B: 、C: 、D: 。
(2)由上述元素组成的单质或化合物相互反应生成沉淀的两个反应方程式是
16.有一未知浓度的盐酸溶液25mL,在加入0.5 mol·L-1 AgNO3溶液25 mL后,改加NaOH溶液,结果用去0.1 mol·L-1NaOH溶液25mL,恰好完全中和,则盐酸的物质的量浓度为( )
A.0.2 mol·L-1 B.0.5 mol·L-1
C.0.1 mol·L-1 D.0.25 mol·L-1
第Ⅱ卷 (非选择题44分)
15.X、Y、Z均为短周期元素,它们在周期表中位置如图所示。若Y原子的最外层电子数是内层电子数的3倍,下列说法正确的是( )
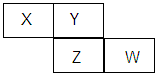
A.原子半径:W>Z>Y>X
B.最高价氧化物对应水化物的酸性:Z>W>X
C.相同状况下,等物质的量浓度的气态氢化物水溶液的pH:X>Z>W
D.Z的氢化物比Y的氢化物熔、沸点高
14.下列实验操作中,先后顺序正确的是( )
A 稀释浓硫酸时,先在烧杯中加入一定体积的浓硫酸,后注入蒸馏水
B 为测定硫酸铜晶体的结晶水含量,称样时,先称取一定量的晶体,后放入坩埚
C 为检验酸性溶液中的Cl-和SO42-,先加硝酸银溶液,滤去沉淀后硝酸钡溶液
D 在制取干燥纯净的氯气时,先使氯气通过水(或饱和食盐水),后通过浓硫酸
13.已知Fe3+的氧化性与Ag+不相上下。在含有Cu(NO3)2、Fe(NO3)3和AgN03的溶
液中加人少量铁粉,首先被置换的是( )
A.Cu B.Ag C.Fe D.Fe和Ag
12.将0.01mol Cl2通入含0.03mol Br-和0.03mol I-的混合液中,再加CCl4振荡,则CCl4层的颜色是( )
A、紫色 B、橙红色 C、棕色 D、黄绿色
11.氢气是人类最理想的能源。已知在25℃、101kPa下,1g氢气完全燃烧生成液态水时放出热量142.9kJ,则下列热化学方程式书写正确的是( )
A.2H2+O2 = 2H2O;△H =142.9kJ/mol
B.2H2(g)+O2(g) = 2H2O(l);△H =-142.9kJ/mol
C.2H2(g)+O2(g) = 2H2O(l);△H =-571.6kJ/mol
D.2H2(g)+O2(g) = 2H2O(l);△H = +571.6kJ/mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com