
题目列表(包括答案和解析)
10.下列离子方程式正确的是
A.次氯酸钙溶液中通入过量二氧化碳 Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO
B.常温时偏铝酸钠溶液pH>7 AlO2-+2H2O=Al(OH)3↓+OH-
C.等物质的量浓度的FeI2溶液与溴水等体积混合2Fe2++2I-+2Br2=2Fe3++I2+4Br-
D.向硫酸氢钠溶液中滴加Ba(OH)2溶液恰好至中性2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
9.中学化学课本中有大量的数据材料,下面是某学生对数据的利用,其中不正确的是
A.利用溶解度数据可判断煮沸Mg(HCO3)2溶液时,得到的产物是Mg(OH)2而不是MgCO3。
B.利用密度数据可判断液态物质挥发性的大小。
C.原子(或离子)半径数据可作为判断某些原子(或离子)的氧化性或还原性的依据。
D.利用沸点数据可判断液态物质挥发性的大小。
8.用铁作阴极,石墨作阳极电解含Mg2+、Ca2+、SO42-杂质的饱和食盐水,通电一段时间后,发现某电极附近食盐水变浑浊,对造成浑浊的原因叙述正确的是
A.由于H+放电,故生成Mg(OH)2 B.由于Cl-放电,故生成Mg(OH)2
C.由于铁溶解生成Fe(OH)2 D.由于H+放电,故生成Ca(OH)2
7.18g18O22-微粒中含有
A.1mol离子 B.9mol中子 C.9mol电子 D.10mol质子
6.在实验中不慎手被玻璃划破,可用FeCl3溶液应急止血,其主要原因是
A.FeCl3溶液具有杀菌消毒作用 B.FeCl3溶液能使血液凝聚
C.FeCl3溶液能产生Fe(OH)3沉淀堵住伤口 D.FeCl3能使血液发生化学作用
23.(8分)有一硫酸与硝酸的混合溶液,取出10mL加入足量BaCl2溶液,过滤、洗涤、烘干后得到9.32g的沉淀;滤液与4.0mol·L-1NaOH溶液反应,用去35mL碱液时恰好完全中和。试求:
(1)混合液中H2SO4、HNO3的物质的量浓度各是多少?
(2)另取10mL原混合液,加入3.2g铜粉共热时,在标准状况下收集到气体的体积约为多少毫升?
(3)若上述10mL混合溶液中的硫酸,是工业上以黄铁矿为原料制备得来的,则需含FeS2质量分数为50%的黄铁矿多少克(设FeS2的转化率为96.0%)?
22. (14分)已知A、B、C、D分别代表中学化学常见物质(或粒子),
(14分)已知A、B、C、D分别代表中学化学常见物质(或粒子),
其中A、B均为两种元素组成的化合物(或粒子),相互转化关系如
右图(有关反应条件已略去)。请根据题目要求回答下列问题:
(1)若A、B两化合物相互反应得到气体单质C和化合物D,则
化学方程式为(只写一个): ;
(2)若A、B两化合物相互反应生成非金属固体单质C和化合物D,且A的相对分子质量大于B,则A、B的化学式分别为:A 、B ,该反应中氧化产物与还原产物的质量之比为 ;
(3)若A是含5个原子核构成的粒子,且A、B均为10电子粒子,含适量A、B粒子的溶液在加热条件下反应生成气体C和化合物D,则A粒子的电子式为 ,C分子的空间构型为 ,含A、B粒子的溶液转化为C、D的离子方程式为 。
21.(8分)铁与HNO3作用时,还原产物除了与HNO3浓度有关外,还与温度有关。已知在与冷稀HNO3反应时,主要还原产物为NO气体;在与热稀HNO3作用时,主要还原产物为N2O气体;当HNO3更稀时,其重要还原产物是NH4+。现有铁与稀HNO3作用,请分析下图,回答有关问题。
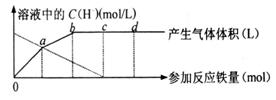
假设曲线的各段内只有一种还原产物。
(1)0点到a点的还原产物是 ;
(2)a点到b点的还原产物是 ,其原因是 ;
(3)试完成b点到c点的反应方程式:
 Fe+ HNO3===?Fe(NO3)3+
+ H2O
Fe+ HNO3===?Fe(NO3)3+
+ H2O
20.(10分)工业生产红矾钠(重铬酸钠Na2Cr2O7)及铬酸酐(CrO3)的工艺流程如下:①将铬铁矿(可视为FeO · Cr2O3,还含有Al2O3和SiO2)、纯碱混合通过空气焙烧(使铬转化为+6价的化合物);②焙烧产物加水,过滤并用硫酸调成弱酸性;③再过滤,滤液继续加硫酸酸化,浓缩、结晶成红矾钠;④红矾钠加浓硫酸熔化反应。反应完毕后趁热分液,冷却压片,即得片状铬酸酐。
(1)完成下列化学反应方程式:
|
|
②SiO2 + Na2CO3 ___ ____;③Al2O3 + Na2CO3
___ ____。
(2)用水浸取燃烧产物,并用硫酸调成弱酸性的目的是(写出有关反应的离子方程式)_______________________,______________ ___。
(3)过滤,除去杂质,滤液继续加硫酸酸化,浓缩结晶生成红矾钠的化学方程式是:
_________ ___。
19.(14分)(1)利用如图所示的装置和其它必要的仪器用品,完成下列实验。
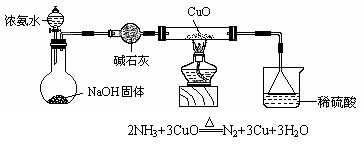
证明氨气具有还原性。已知:
① 碱石灰的作用是________________,稀硫酸的作用是_________________;
② 浓氨水与固体NaOH接触,为什么会逸出大量氨气? ______________________________________________________________ ;
③ 证明NH3具有还原性的实验现象是: 。
(2)水蒸气通过灼热的煤所产生的混合气体,其主要成分是CO、H2,还含有少量CO2和水蒸气。请用下图装置设计一个实验,以确认上述混合气中含有CO和H2。
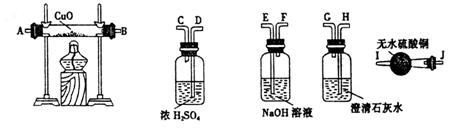
①连接上图装置的正确顺序是(填各接口代码字母):(已知洗气瓶中的溶液均足量)
混合气→( )( )接( )( )接( )( )接( )( )接( )( )。
②确认混合气中含有H2的实验现象是 ;
③确认混合气中含有CO的有关反应的化学方程为 ; 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com