
题目列表(包括答案和解析)
3、化学平衡的特点:“_、__ 、__ ”
a.反应物与生成物处于动态平衡,在化学平衡状态,可逆反应的正反应和逆反应都还在不断的进行着,只是此时V正=V逆(且都大于0)。而不是停止了化学反应。
b.在化学平衡状态,任何反应物与生成物浓度保持一定,百分组成保持一定;(或说反应物与生成物的含量保持一定)
c.影响平衡的外界条件改变,平衡状态即被破坏,发生平衡移动。
2、 当一个可逆反应的__________________相等时,________________不再改变,达到一种“平衡状态”,这就是这个反应所能达到的限度。
任何化学反应都有一定的限度,有的反应限度较大,反应进行的比较彻底,反应物转化为生成物的转化率较大;有的反应限度较小,反应物转化为生成物的转化率较小。
1、可逆反应:能同时向________________________进行的化学反应叫做可逆反应。理解可逆反应需注意三同:同__、同__、同____。
3、应用化学反应速率需注意以下问题:
(1)化学反应速率是标量,只有___而没有___;
(2)一般计算出来的化学反应速率是一段时间内的___速率,不同时刻的化学反应速率
是不相同的;
(3)固体或气体反应中的液体物质,反应在其表面进行,它们的“浓度”是___变的,
因此一般___用固体、纯液体表示化学反应速率;
(4)对于同一化学反应,用不同的物质表示其化学反应速率可能___相同,但其化学反应速率之比等于__________之比。
2、影响化学反应速率的因素:
|
影响化学反应速率的因素 |
规律 |
|
|
内因 |
反应物的性质 |
|
|
外 因 |
催化剂 |
|
|
反应物的温度 |
|
|
|
反应物的浓度 |
|
|
|
气态反应物的压强 |
|
|
|
固体反应物的表面积 |
|
|
|
其他 |
|
1、化学反应速率的表示方法
化学反应速率通常用__________________来表示。表达式:_______,其常用的单位是 或 。
例如:某反应的反应物浓度在5min内由6mol/L变成了2mol/L,则以该反应物浓度的变化表示的该反应在这段时间内的平均反应速率为:__________。
29. (16分)某芳香族化合物A,苯环上只有一个取代基,完全燃烧只生成二氧化碳和水,一定条件下存在如下图所示的转化关系:
(16分)某芳香族化合物A,苯环上只有一个取代基,完全燃烧只生成二氧化碳和水,一定条件下存在如下图所示的转化关系:
请回答下列问题:
⑴A的摩尔质量为___________,在一定条件下B可能发生的化学反应的类型有_______(填序号)。
①水解反应。②取代反应。③加成反应。④消去反应。⑤加聚反应。
⑵C的结构简式为_______________,E的结构简式为_________________。
⑶写出下列转化的化学方程式:
①A→B:______________________________________________________________。
②D→F:______________________________________________________________。
⑷符合下列三个条件的A的同分异构体的数目有____个
①含有二取代苯环结构。②与A有相同的官能团。③能与FeCl3溶液发生显色反应。
高三年级第二次模拟考试
28.(14分)某学生课外活动小组为了证明和比较二氧化硫和氯气的漂白性,设计了如下图所示的实验装置。
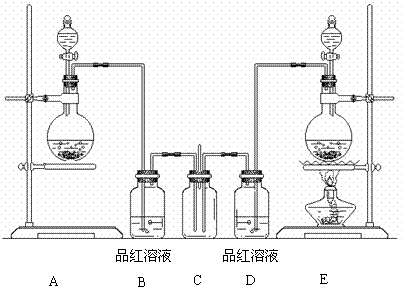
请回答下列问题:
⑴实验室制取氯气的化学方程式为________________________________________。
⑵实验室常用浓硫酸与亚硫酸钠固体反应制取二氧化硫,则其反应装置为上图中的____(填写字母代号),不用稀硫酸与亚硫酸钠溶液制取二氧化硫的理由是________________________
____________________________。
⑶装置C中试剂的名称及作用是____________________________________________。
⑷反应开始后,发现B、D两个装置中的品红溶液都褪色。请设计一个简单实验,证明二氧化硫和氯气漂白品红溶液的原理不同,实验方法、预期的现象和结论为________________
_____________________________________________________________________________
__________________________________________。
⑸若将B、D装置中的品红溶液换为滴有酚酞的氢氧化钠溶液,反应一段时间后,B、D中的现象是_____________________________________________________________________。
⑹实验结束后,经检验,发现装置C中的溶液呈碱性,并且含有SO2- 4。试写出C中生成
SO2- 4的离子方程式(有多种可能,只写出一个即可)______________________________。
27.(15分)A、B、C、D、E5瓶溶液,分别是AlCl3、BaCl2、NaHSO4、K2CO3、AgNO3中的一种。已知:
①A与B反应有气体产生 ②B与C反应有沉淀生成
③C与D反应有沉淀生成 ④D与E反应有沉淀生成
⑤A与E反应有气体生成 ⑥在②和③发反应中生成的沉淀是同一物质
请填写下列空白:
⑴A是____________,B是____________,D是______________。
⑵向C溶液中逐滴滴加过量稀氨水,在整个过程中出现的现象是___________________。
⑶将0.1mol/L的E溶液与0.1mol/L的Ba(OH)2溶液按下表中甲、乙、丙、丁、戊不同方式混合:
|
|
甲 |
乙 |
丙 |
丁 |
戊 |
|
0.1mol/L的Ba(OH)2溶液的体积/mL |
10 |
10 |
10 |
10 |
10 |
|
0.1mol/L的E溶液的体积/mL |
5 |
10 |
15 |
20 |
25 |
①按丁方式混合后,所得溶液显________(填“酸”、“碱”、“中”)性。
②写出按乙方式混合时,反应的离子方程式为________________________________。
③25℃时,按甲方式混合后,所得溶液的pH为________。
26.(15分)A、B、C、D、E5种短周期元素,原子序数依次增大。已知:
①A与B可形成原子个数比为1:1、2:1、3:1等多种气态化合物;
②B和D可形成BD2- 3或B2D2- 4;
③E的二价阳离子与D的阴离子具有相同的电子层结构。
请回答下列问题:
⑴A元素的名称是_____,C元素的元素符号为_______。
⑵A和D可形成两种化合物的化学式分别为__________和__________。
⑶E的单质与BD2发生反应的化学方程式为____________________________________。
⑷将CD2放入一密闭容器,在一定条件下测定其相对分子质量,结果发现测得的数值总是比按CD2化学式计算所得的数值大幅偏高,其原因是____________________________________
__________________________________________________________________。
⑸B单质的一种同素异形体呈空间网状结构,则该晶体结构中最小环上含有___个B原子。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com