
题目列表(包括答案和解析)
13、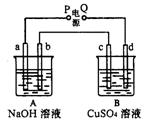 按右图装置实验,A、B两烧杯分别盛放200g10%NaOH和足量CuSO4溶液。通电一 段时间后,c极上有Cu析出;又测得A杯中溶液的质量减少4.5 g (不考虑水的蒸发)。 则下列叙述中正确的是
按右图装置实验,A、B两烧杯分别盛放200g10%NaOH和足量CuSO4溶液。通电一 段时间后,c极上有Cu析出;又测得A杯中溶液的质量减少4.5 g (不考虑水的蒸发)。 则下列叙述中正确的是
A.电源P极为负极
B.标准状况下,b极产生气体的体积为5.6 L
C.c极上析出固体的质量为16 g
D.a极上所发生的电极反应式为40H--4e-= 2H2O+O2↑
12、已知蓄电池在充电时作电解池,放电时作原电池。铅蓄电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“-”。关于标有“+”的接线柱,下列说法中正确的是 A.充电时作阳极,放电时作正极 B.充电时作阳极,放电时作负极
C.充电时作阴极,放电时作负极 D.充电时作阴极,放电时作正极
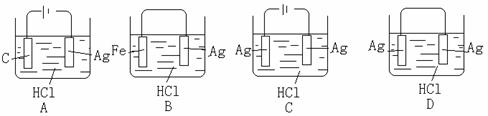
11、某学生欲完成2HCl+2Ag=2AgCl↓+H2↑反应,设计了下列四个实验,你认为可行的是:
10.用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.1mol Cu(OH)2后恰好恢复到电解前的浓度和PH。则电解过程中转移的电子数为( ) A、0.1mol B、0.2mol C、0.3mol D、0.4mol
9、高铁电池是一种新型可充电电池,与普通高能电池相比,
该电池能长时间保持稳定的放电电压。高铁电池的总反应为:
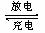 3Zn + 2K2FeO4 + 8H2O 3Zn(OH)2 + 2Fe(OH)3
+ 4KOH
3Zn + 2K2FeO4 + 8H2O 3Zn(OH)2 + 2Fe(OH)3
+ 4KOH
下列叙述不正确的是:A.放电时负极反应为:Zn - 2e- + 2OH- == Zn(OH)2
B.充电时阳极反应为:Fe(OH)3 - 3e- + 5OH- == FeO42- + 4H2O
C.放电时每转移3moL电子,正极有1 mol K2FeO4被氧化
D.放电时正极附近溶液的碱性增强
8、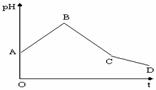 将等物质的量浓度的CuSO4和NaCl等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如右,则上列说法正确的是:
将等物质的量浓度的CuSO4和NaCl等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如右,则上列说法正确的是:
A.阳极产物一定是Cl2,阴极产物一定是Cu
B.BC段表示在阴极上是H+放电产生了H2
C.整个过程中阳极先产生Cl2,后产生O2
D.CD段表示阳极上OH-放电破坏了水的电离平衡,产生了H+
7.如右图所示装置,两玻璃管中盛满滴有酚酞溶液的NaCl饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。接通S后,C (Ⅱ)附近溶液变红,两玻璃管中有气体生成。下列说法正确的是
A.C(Ⅰ)的电极名称是阴极
B. C(Ⅱ)的电极反应式是2Cl--2e-=Cl2↑
C. 电子从电源的负极沿导线流向C(Ⅱ)
D.电解过程中,C(Ⅰ)、C(Ⅱ)两极产生的气体质量相等
6.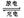 我国镍氢电池居世界先进水平,我军潜艇将装备国产大功率镍氢动力电池,常见镍氢电池的某极是储氢合金LaNi5H6(LaNi5H6中各元素化合价均为零),电池反应通常表示为
我国镍氢电池居世界先进水平,我军潜艇将装备国产大功率镍氢动力电池,常见镍氢电池的某极是储氢合金LaNi5H6(LaNi5H6中各元素化合价均为零),电池反应通常表示为
LaNi5H6+6NiO(OH) LaNi5+6Ni(OH)2
下列说法正确的是
A.放电时储氢合金作正极 B.放电时负极反应:LaNi5H6+6OH--6e- = LaNi5+6H2O
 C.充电时阳极周围c(OH-)增大 D.充电时储氢合金作负极
C.充电时阳极周围c(OH-)增大 D.充电时储氢合金作负极
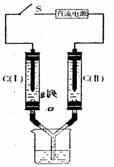
5. 如图所示,E是用CuCl2溶液和品红试液的混合液湿润的滤纸,用石墨作电极,通电后发
 现乙周围滤纸褪为无色,则下列判断正确的是 ( )
现乙周围滤纸褪为无色,则下列判断正确的是 ( )
A、b是阳极,a是阴极
B、a是正极,b是负极
C、乙是正极,甲是负极
D、乙是阳极,甲是阴极
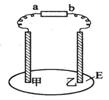
4. 有机电解制备的金属醇盐,可直接作为制备纳米材料的前体。以下是一种电化学合成金属醇盐的主要装置。在电解过程中,已知乙醇和乙酰丙酮(CH3COCH2COCH3)在阴极发生的电极反应为:
有机电解制备的金属醇盐,可直接作为制备纳米材料的前体。以下是一种电化学合成金属醇盐的主要装置。在电解过程中,已知乙醇和乙酰丙酮(CH3COCH2COCH3)在阴极发生的电极反应为:
2CH3CH2OH+2e-=2CH3CH2O-+H2↑
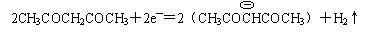
下列说法正确的是
A.阳极Pb失去电子,发生还原反应
B.当阳极失去2 mol e- 时,阴极产生2 mol氢气
C.电解过程中,阳离子向阴极移动
D.已知Pb-4e-=Pb4+,当消耗Pb的质量为103.5 g时,则转移电子2 mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com