
题目列表(包括答案和解析)
23.(05年扬州市三模,12)生物体中细胞膜内的葡萄糖与细胞膜外的富氧体液及细胞膜构成原电池,下列有关电极反应及产物的判断正确的是
A.负极反应可能是O2+2H2O+4e→4OH--
B.负极反应的产物主要是C6H12O6被氧化成CO32-- HCO3--和H2O
C.正极反应可能是C6H12O6+24OH---24e→6 CO2↑+18H2O
D.正极反应的产物主要是葡萄糖生成的CO2 HCO3--和H2O
22.(05年江苏宿迁市二模,17)据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为: 则下列说法正确的是 A.放电时CH3OH参与反应的电极为正极
则下列说法正确的是 A.放电时CH3OH参与反应的电极为正极
B.放电时负极的电极反应为:
C.标准状况下,通人5.6LO2并完全反应后,有O.5mol电子转移
D.放电一段时间后,通人O2的电极附近溶液的pH降低
21. 2004年美国圣路易斯大学科学家研制了一种新型的乙醇电池(DEFC),它用磺酸类质子溶剂,在200oC左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全。电池总反应为:C2H5OH +3O2 2CO2
+3H2O,电池示意如右图。下列说法不正确的是 A.a极为电池的正极
2004年美国圣路易斯大学科学家研制了一种新型的乙醇电池(DEFC),它用磺酸类质子溶剂,在200oC左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全。电池总反应为:C2H5OH +3O2 2CO2
+3H2O,电池示意如右图。下列说法不正确的是 A.a极为电池的正极
B.电池工作时电流由b极沿导线经灯泡再到a极
C.电池正极的电极反应为:4H+ +O2 +4e- = 2H2O
D.设每个电子所带电量为q库仑,则1mol乙醇被氧化产生6NAq库仑的电量
20.当电解质溶液为氢氧化钾水溶液的氢氧燃料电池电解饱和碳酸钠溶液一段时间,假设电解时温度不变且用惰性电极,下列说法正确的是
A.当电池负极消耗mg气体时,电解池阳极同时有mg气体生成
B.电池的正极反应式为:O2十2H2O十4e-==4OH-
C.电解后c(Na2CO3)不变,且溶液中有晶体析出
 D.电池中c(KOH)不变;电解池中溶液pH变大
D.电池中c(KOH)不变;电解池中溶液pH变大
19.近年来,加“碘”食盐较多使用了碘酸钾,KIO3在工业上可
用电解法制取,以石墨和铁为电极,以KI溶液为电解液在一定条件下电解,反应式为
KI+H2O→KIO3+H2↑。下列有关说法中,正确的是
A.电解时,石墨做阳极,铁作阴极 B.电解时,在阳极上产生氢气
C.电解后得到KIO3产品的步骤有:过滤→浓缩→结晶→灼烧
D.电解中,每转移0.6mol电子,理论上可得到0.1mol无水KIO3晶体
18.汽车的启动电源常用铅蓄电池,放电时的电池反应如下:
PbO2+Pb+2H2SO4=2PbSO4↓+2H2O,根据此反应判断下列叙述中正确的是
A.Pb O2是电池的负极 B.负极的电极反应式为:Pb+SO42--2e-=PbSO4 ↓
C.电池放电时,PbO2得电子,被氧化 D.电池放电时,溶液酸性增强
17. 按右图装置实验,A、B两烧杯分别盛放200g10%NaOH和足
按右图装置实验,A、B两烧杯分别盛放200g10%NaOH和足
量CuSO4溶液。通电- 段时间后,c极上有Cu析出;又测得A杯中
溶液的质量减少4.5 g (不
考虑水的蒸发)。 则下列叙述中正确的是
A.电源P极为负极 B.标准状况下,b极产生气体的体积为5.6 L
C.c极上析出固体的质量为16 g
D.a极上所发生的电极反应式为4OH--4e-= 2H2O+O2↑
16.将1L一定浓度的CuSO4溶液,用a,b两个石墨作电极电解,当a极上产生22.4L(标准状况)气体时,b极上有金属析出,然后将a,b极电源反接,继续通直流电,当b极上又产生22.4L(标准状况)气体时,溶液质量共减少227g。则下列说法正确的是:
A 、a极上产生22.4L(标准状况)气体时,b极增加的质量为128g
B、原CuSO4溶液的物质的量浓度为2.5mol/L C、电源反接后b极上产生的气体是氢气
D、电源反接后继续通直流电使溶液质量减少量达到227g的过程中不可能有H2 析出
15. 用下图装置进行电解实验:A极是铜锌(均匀)合金,B极为纯铜,电解质溶液中含有足量的铜离子。通电一段时间后,若A极恰好全部溶解,
用下图装置进行电解实验:A极是铜锌(均匀)合金,B极为纯铜,电解质溶液中含有足量的铜离子。通电一段时间后,若A极恰好全部溶解,
此时B极质量增加7.68克,溶液质量增加0.03克。
则下列说法不正确的是:
A、电解实验时阳极反应为 Zn-2e-=== Zn2+ Cu-2e-==Cu2+
B、电解实验时阴极反应为 Cu2++e-==Cu C、电极B上增加的7.68克物质均为铜
D、电极合金中Cu、Zn原子个数比为3∶1
14、工业上电解质量分数为23.4%的精制食盐水a kg,电解后残液的密度为ρ kg/L。将产生的H2、Cl2在一定条件下反应制成质量分数为36.5%的盐酸b kg,已知H2、C12的利用率均为c%。则下列说法不正确的是:
A.电解食盐水反应的离子方程式为2Cl―+2H2O Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
B.电解后残液中氯化钠的质量分数为w(NaCl)=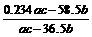 ×100%
×100%
C.电解后残液中NaOH的物质的量浓度为c(NaOH)= mol/L
mol/L
D.电解时阳极上所发生的电极反应式为40H--4e-= 2H2O+O2↑
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com