
题目列表(包括答案和解析)
13.锌与某浓度的硝酸完全反应,消耗的Zn与HNO3的物质的量之比为5:12,若还原产物只有一种,则其为
A.N2 B.N2O C.NO D.NO2
12.下列离子方程式书写不正确的是
A.二氧化硅溶于氢氧化钠溶液:SiO2+2OH-===SiO +H2O
+H2O
B.硫酸亚铁溶于稀硝酸:3Fe2++NO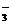 +4H+===3Fe3++NO↑+2H2O
+4H+===3Fe3++NO↑+2H2O
C.亚硫酸钠溶液与双氧水混合:SO +2H2O2===SO
+2H2O2===SO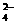 +2H2O+O2↑
+2H2O+O2↑
D.亚硫酸铵溶液与氢氧化钡溶液混合:SO +2NH
+2NH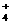 +Ba2++2OH-===BaSO3↓+2NH3·H2O
+Ba2++2OH-===BaSO3↓+2NH3·H2O
11.常温下四只容积相同的抽空的密闭容器,分别注入下列各气体(先注入一种然后再注入另一种),全部气体注入完毕后,容器内压强从大到小的顺序是
①2molH2和1molO2 ②2molH2S和1molSO2
③2molNO和1molO2 ④2molNH3和1molHCl
A.①=②=③=④ B.①>③>④>②
C. ③>④>②=① D.①>②=③>④
10.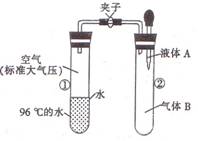 如图所示,夹子开始处于关闭状态,将液体A滴人试
如图所示,夹子开始处于关闭状态,将液体A滴人试
管②与气体B充分反应,打开夹子,可发现试管①内
的水立刻沸腾了。则液体A和气体B的组合不可能
是下列的
A.氢氧化钠溶液、二氧化碳
B.水、氨气
C.氢氧化钠溶液、一氧化氮
D.水、二氧化氮
9.北京大学和中国科学院的化学工作者合作,已成功研制出碱金属与C60形成的球碳盐K3C60。实验测知该物质属于离子晶体,具有良好的超导性。下列关于K3C60的组成和结构的分析中正确的是
A.K3C60中既有离子键,又有极性键
B.1 molK3C60中含有的离子数目为63×6.02×1023
C.该晶体在熔融状态下能导电
D.该物质的化学式可写为KC20
8.下列单质中,最难与H2化合的是
A.Cl2 B.C
C.N2 D.O2
7. A、B、C、D四个集气瓶中分别盛有Cl2、H2、HCl、HBr中的一种,A 和D混合后见光爆炸,A 和B混合后瓶壁上有棕红色小液滴析出,则C 瓶所盛气体是
A.HCl B.Cl2
C.H2 D.HBr
6.某蓄电池放电和充电时的反应为: Fe + Ni2O3 +3H2O -----→ Fe(OH)2 + 2Ni(OH)2
下列推断中正确的是
①、放电时Fe为正极, Ni2O3为负极;
②、充电时阴极上的电极反应式为: Fe(OH)2+2e- = Fe + 2OH-
③、充电时Ni(OH)2为阳极;
④、蓄电池的电极必须是浸在某种碱性电解质溶液中;
A.①②③ B.①②④
C.①③④ D.②③④
5.下列关于二氧化硫性质的叙述中,错误的是
A.二氧化硫能漂白某些物质,说明它具有氧化性
B.二氧化硫的水溶液能使紫色石蕊试液变红,说明它能和水反应生成H2SO3
C.将足量二氧化硫通入酸性高锰酸钾试液中,溶液褪色,说明二氧化硫具有还原性
D.实验室可用浓硫酸干燥二氧化硫
4.碱金属与卤素所形成的化合物在都具有的性质是
①高沸点 ②能溶于水 ③水溶液能导电 ④低熔点 ⑤熔融状态不导电
A.①②③ B.③④⑤ C.①④⑤ D.②③⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com