
题目列表(包括答案和解析)
2.(2005年江苏高考化学试题)某溶液既能溶解AI(OH)3,又能溶解H2SiO3,在该溶液中可以大量共存的离子组是( )
A.K+、Na+、HCO3-、NO3- B.Na+、SO42-、Cl-、ClO-
C.H+、Mg2+、SO42-、NO3- D.Ag+、K+、NO3- 、Na+
1.(2003·江苏)若溶液中由水电离产生的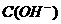 =1×10-14mol·L-1,满足此条件的溶液中一定可以大量共存的离子组是( )
=1×10-14mol·L-1,满足此条件的溶液中一定可以大量共存的离子组是( )
A. Al3+ 、Na+ 、NO3-、Cl- B. K+ 、Na+、Cl-、NO3-
C. K+ 、Na+ 、Cl-、AlO2- D. K+ 、 NH4+、SO32-、NO3-
3.命题趋向。
(1)离子共存问题是高考中的常见题型,是每年必考的题型。今后命题的发展趋势是:
①增加限制条件,如强酸性、无色透明、碱性、pH=1、甲基橙呈红色、发生氧化还原反应等;
②定性中有定量,如“由水电离出的c(H+)=1×10-14 mol·L-1的溶液中,……”
(2)离子方程式的书写正误也是历年高考必出的试题。从命题的内容看,存在着三种特点:
①所考查的化学反应均为中学化学教材中的基本反应;错因大都属于化学式能否拆分、处理不当,电荷未配平,产物不合理和漏掉部分反应等;
②所涉及的化学反应类型以复分解反应为主,而溶液中的氧化还牟反应约占15%;
③一些重要的离子反应方程式,在历年考卷中多次重复。如Na与H2O的反应、Fe与盐酸升稀H2SO4的反应自1992年以来分别考过多次。
考查离子方程式的目的主要是了解学生使用化学用语的准确程度和熟练程度,具有一定的综合性,预计今后的考题还会保留。
[课堂训练]
2.解题注意点:
离子反应在高考中的考查难度一般不大,主要立足基础知识的考查。解题关键要严密审题,看清设问中“正”与“误”;条件中量的“多”与“少”,滴加顺序的“先”与“后”;挖掘离子共存中的隐含条件。
1.方法与技巧
(1)离子反应是中学化学一类主要反应,它的涉及面广,要结合元素化合物、电解质理论、氧化还原反应等,应理解离子反应的发生条件,并运用于实际问题的解决之中。
(2)离子方程式的书写与正误判断,是高考中常考题型,要在掌握离子反应的的发生条件与离子方程式的书写规则的基础上,加强练习,练出“火眼金睛”。、
(3)如何解答离子共存题。
解答离子共存问题时,一方面要掌握离子共存的基本原理,另一方面要注意审题,挖掘出隐含条件,如:
①某无色溶液,表明不存在Cu2+. Fe2+. Fe3+. MnO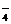 等有颜色离子。
等有颜色离子。
②某强酸性溶液,表明有大量H+存在。
③某强碱性溶液,表明有大量OH-存在。
④某溶液中由水本身电离出的c(OH-)=1×10-12mol/L,表明溶液的pH可能等于2或12,即可能有大量H+存在,也可能有大量OH-存在。
⑤某溶液与Al反应产生H2,表明该溶液可能是强酸性溶液,也可能是强碱性溶液,且强酸性溶液中不可能存在NO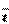 。
。
2.正确书官吏离子方程式。依据题目所给信息,运用书写典型反应的离子方程式;或结合个体反应,依据书写规则对离子方程式进行正误判断。
[典型例析]
[例1]若在加入铝粉能放出氢气的溶液中,分别加入下列各组离子,可能共存的是( )
A.
NH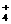 NO
NO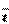 CO
CO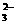 Na+ B.
Na+ Ba2+ Mg2+ HCO
Na+ B.
Na+ Ba2+ Mg2+ HCO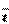
C.
NO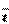 K+ AlO
K+ AlO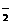 OH- D.
NO
OH- D.
NO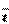 Ca2+
K+ Cl-
Ca2+
K+ Cl-
[解析]加铝粉能放出氢气的溶液,除了酸以外,还可能为碱液,所以A中NH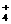 不能与OH共存,CO
不能与OH共存,CO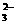 与H+不能共存;B中HCO
与H+不能共存;B中HCO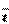 与H+和OH-都不能共存;C中离子在碱液中可共存,D中离子无论在酸还是碱中均能共存。
与H+和OH-都不能共存;C中离子在碱液中可共存,D中离子无论在酸还是碱中均能共存。
[答案]C、D
[点评]离子共存是传统题型,已由最初的单纯共存问题发展到指定条件下(诸如:酸性、碱性、有无颜色)是否发生氧化还原,是否有双水解、络离子的生成等多种变化,需要同学们在解题中加以认真审题,全面思考才可。
[例2](1995-2005年全国高考题)能正确表示下列反应离子方程式的是( )
(1)碳酸氢钙溶液中加稀HNO3: HCO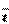 +H+=H2O+CO2↑
+H+=H2O+CO2↑
(2)向饱和碳酸氢钙溶液中加入饱和Ca(OH)2溶液
Ca2++
HCO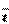 +OH-=CaCO3↓+H2O
+OH-=CaCO3↓+H2O
(3)把金属铁放入稀H2SO4中 2Fe+6H+=2Fe3++3H2↑
(4)金属钠投入到水中 Na+2H2O=Na++2OH-+H2↑
(5)铜片与稀硝酸反应:Cu+NO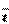 +4H+=Cu2++NO↑+2H2O
+4H+=Cu2++NO↑+2H2O
(6)金属铝溶于氢氧化钠溶液:Al+2OH-=AlO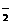 +H2↑
+H2↑
(7)向氯化亚铁溶液中通过氯气:Fe2++Cl2=Fe3++2Cl-
(8)硫酸亚铁溶液中加入H2O2溶液:Fe2++2H2O2+4H+=Fe3++4H2O
(9)三氯化铁溶液跟过量氨水反应:Fe3++3NH3·H2O=Fe(OH)3↓+3NH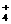
(10)Fe2(SO4)3的酸性溶液中通过入足量硫化氢:Fe3++H2S=Fe2++S↓+2H+
(11)用氨水吸收少量二氧化硫:NH3·H2O+SO2=NH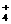 +HSO
+HSO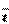
(12)饱和石灰水跟稀HNO3反应:Ca(OH)2+2H+=Ca2++2H2O
(13)用NaOH溶液吸收少量CO2 2OH-+CO2=CO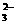 +H2O
+H2O
(14)次氯酸钙溶液中通入过量CO2:Ca2++2ClO-+H2+CO2=CaCO3↓+2Hco
(15)硫化钠水解:S2-+2H2O H2S+2OH-
H2S+2OH-
(16)氯气通入水中:Cl2+H2O=2H++Cl-+ClO-
(17)碳酸氢钠溶液与少量石水反应 HCO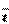 +Ca2++OH-=CaCO3↓+H2O
+Ca2++OH-=CaCO3↓+H2O
(18)氯化铵与氢氧化钠两种浓溶液混合加热 OH-+NH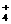 H2O+NH3↑
H2O+NH3↑
(19)电解饱和食盐水 2Cl-+2H2OH2↑+Cl2↑+2OH-
(20)硫酸铝溶液中加入过量氨水 Al3++3OH-====Al(OH)3↓
[解析]有关离子方程式判断正误,应当采用正向思维,根据书官吏要求进行分析,每一个离子方程式都应与其化学方程式及实际情况相吻合,不能随意臆造,综合分析知:(1)(2)正确,(3)H+不能将Fe氧化为Fe3+,
(4)(5)电荷不守恒,(6)得失电子不相等,(7)(8)电荷不守恒,(9)正确,(10)电荷不守恒,(11)少量SO2时,不可能生成HSO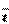 ,只能生成SO
,只能生成SO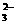 ,(12)石灰水中Ca(OH)2应以Ca2+、OH-形式书写,(13)正确,(14)在通入过量CO2时应写成Ca(HCO3)2,(15)反应没有分步,(16)HclO分子不可改写,因为HclO是弱酸,(17)Ca(OH)2少量时,OH-与HCO
,(12)石灰水中Ca(OH)2应以Ca2+、OH-形式书写,(13)正确,(14)在通入过量CO2时应写成Ca(HCO3)2,(15)反应没有分步,(16)HclO分子不可改写,因为HclO是弱酸,(17)Ca(OH)2少量时,OH-与HCO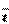 完全转化成CO
完全转化成CO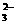 ,无OH-剩余,(20)未考虑NH3·H2O是弱碱。
,无OH-剩余,(20)未考虑NH3·H2O是弱碱。
[答案](1)(2)(9)(13)(18)(19)
[点评]书写离子方程式是中学化学中要求学生掌握的一种基本功,命题的意图在于考查,学生书写离子方程式的基本技能,并透过这些书写来检验学生认识弱电解质、物质的溶解性、离子反应发生的条件等方面的情况,判断离子方程方程式的对错主要从以下几个方面考虑:
①产物对不对;(1)Fe的氧化物,(2)量不同时的产物,(3)滴加顺序的不同等
②两边平不平:(1)原子是否守恒,(2)电荷是否守恒,(3)氧化还原反应电子是否守恒;
③物质拆不拆:(1)强拆弱不拆,(2)易溶拆不溶不拆,(3)微溶物清拆浊不拆,(4)浓H2SO4不拆,浓HCl、浓HNO3拆,(5)单质、氧化物不拆。
[例3]某溶液中可能含有HN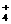 、Ba2+、Fe2+、Ag+、OH-、SO
、Ba2+、Fe2+、Ag+、OH-、SO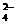 、CO
、CO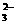 中的某几种,现用该溶液做以下实验:
中的某几种,现用该溶液做以下实验:
①取此溶液少许,加足量盐酸无明显现象;
②另取少许加入足量浓NaOH溶液,有白色沉淀生成;
③将②中沉淀过滤,取滤液微热,有无色刺激性气体放出,该气体能使湿润红色石蕊试纸变蓝。
由此推断,该溶液中肯定有 离子,肯定无 离子。
[解析]解此类题的关键是分析清楚每个实验的现象,同时要注意离子共存问题,若肯定有某种离子存在,则与其不共存的离子均可排除掉。本题由①可排除Ag+、CO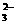 (Ag+与Cl-生成AgCl白色沉淀,CO
(Ag+与Cl-生成AgCl白色沉淀,CO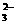 与H+生成CO2)。由②肯定了Fe2+( 生成Fe(OH)2白色沉淀),则与Fe2+不共存的OH-即被排除。由于溶液呈电中性,则必有SO
与H+生成CO2)。由②肯定了Fe2+( 生成Fe(OH)2白色沉淀),则与Fe2+不共存的OH-即被排除。由于溶液呈电中性,则必有SO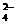 存在,进一步又可排除与S O
存在,进一步又可排除与S O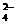 不共存的Ba2+。由③可知肯定有NH
不共存的Ba2+。由③可知肯定有NH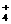 存在(因NH3可使湿润红色石蕊试纸变蓝。
存在(因NH3可使湿润红色石蕊试纸变蓝。
[答案]肯定有NH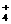 、Fe2+、SO
、Fe2+、SO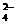 肯定无Ba2+、Ag+、OH-、CO
肯定无Ba2+、Ag+、OH-、CO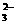 。
。
[方法归纳]
1.离子反应,此类试题考查的主要内容有:
(1)理解离子反应的概念,
(2)掌握离子反应发生的条件,
(3)会判断离子在溶液中能否大量共存。
命题主要以选择题的形式出现,是高考中常见题型和必考知识点。
32.抗击“非典”期间,过氧乙酸CH3C-O-OH是广为使用的消毒剂。它可由H2O2和冰醋酸反应制取,所以在过氧乙酸中常含有残留的H2O2。测定产品中过氧乙酸浓度c0。涉及下列反应:





 ① MnO4-+ H2O2+ H+= Mn2++ O2+ H2O
① MnO4-+ H2O2+ H+= Mn2++ O2+ H2O
|
③CH3C-O-OH+2I-+2H+=CH3COOH+I2+H2O
④2Na2S2O3+I2=2NaI+Na2S4O6





 (1)① Mn4-+ H2O2+ H+= Mn2++ O2+ H2O
(1)① Mn4-+ H2O2+ H+= Mn2++ O2+ H2O
(2)用Na2S2O3标准溶液滴定I2时(反应④)选用的指示剂是 。
(3)取b0mL待测液,用硫酸使溶液酸化,再用浓度为a1mol·L-1的KMnO4标准溶液滴定其中的H2O2,耗用的KMnO4体积为b1mL(反应①,滴定过程中KMnO4不与过氧乙酸反应)。
另取b0mL待测液,加入过量的KI,并用硫酸使溶液酸化,此时过氧乙酸和残留的H2O2都能跟KI反应生成I2(反应②和③)。再用浓度为a2mol·L-1的Na2S2O3标准溶液滴定生成的I2,耗用Na2S2O3溶液体积为b2mL。
请根据上述实验数据计算过氧乙酸的浓度(用含a1、a2、b0、b1、b2的代数式表示)
c0= 。
(4)为计算待测液中过氧乙酸的浓度c0,加入的KI的质量已过量但没有准确称量,是否影响测定结果 (填是或否)
31.向20mL 0.2mol/L NaOH溶液中缓慢通入一定量CO2气体,将溶液在一定条件下蒸干,若得到白色固体是纯净物,则通入CO2的体积应为 (标准状况)。
写出有关的离子方程式 。
将上述白色固体加水溶液解,加盐酸至pH=7,再蒸干,得到白色固体体的质量应为
。
写出有关计算过程。
|
28.亚硫酸钠中+4价的硫,它既有氧化性又有还原性,现在有试剂:溴水、硫化钠溶液,NaOH溶液、氯化钡溶液、稀硫酸。
(1)要证明亚硫酸钠具有还原性,除亚硫酸钠外还应选用的试剂有 ,看到的现象是 ,反应的离子方程式 。
(2)要证明亚硫酸钠具有氧化性,除亚硫酸钠外还应选用的试剂有 ,看到的现象是 ,反应的离子方程式 。
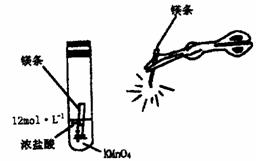 29.高锰酸钾可将浓盐酸氧化成氯气。现将0.05g高锰酸钾和一段镁条放入同一试管中,加入1.5mL浓盐酸后立即塞上软木塞,并用一根燃着的镁条在试管附近进行强光照射,如下图所示。请回答下列问题:
29.高锰酸钾可将浓盐酸氧化成氯气。现将0.05g高锰酸钾和一段镁条放入同一试管中,加入1.5mL浓盐酸后立即塞上软木塞,并用一根燃着的镁条在试管附近进行强光照射,如下图所示。请回答下列问题:
(1)点燃镁条强光照射后可观察最为明显的现象是 。
(2)写出试管内可能发生反应的化学方程式 。
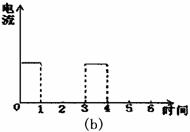
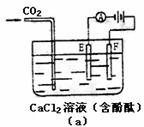 30.如下图(a)为持续电解饱和CaCl2水溶液的装置(以铂为电极,A为电流表),电解一段时间后,从图(b)1小时起将CO2连续通入电解液中,请在图(b)中完成实验(a)中电流对时间的变化关系图,并回答有关问题。
30.如下图(a)为持续电解饱和CaCl2水溶液的装置(以铂为电极,A为电流表),电解一段时间后,从图(b)1小时起将CO2连续通入电解液中,请在图(b)中完成实验(a)中电流对时间的变化关系图,并回答有关问题。
(1)完成实验(a)中电流对时间的变化关系图。
(2)电解时F极发生 反应,电极反应式为 ;E极发生
反应,电极反应式为 ;电解总方程式为
。
(3)电解池中产生的现象:① ② ③ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com