
题目列表(包括答案和解析)
2、稀硝酸与铜的反应的化学方程式 。
1、浓硝酸与铜的反应的化学方程式 。
3、浓硫酸的强氧化性
(1)浓硫酸与金属铜反应探究
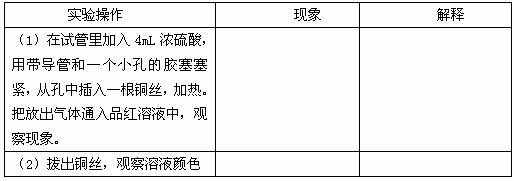
[探讨 1]根据反应的现象,你能分步写出铜与浓硫酸反应的化学方程式吗?
[探讨2]上述反应中氧化剂、还原剂各是什么物质?被氧化与被还原的元素各是什么?还原剂与氧化剂物质的量之比是多少?浓硫酸的作用是什么?
[探讨3]考虑本实验的产物为有毒气体,请你想一想如何改进实验装置?若想同时证明SO2 溶液显酸性,如何改进实验装置?画出简图。
(2)浓硫酸与非金属(如C)的反应
[思考]根据氧化还原反应的规律,结合在蔗糖中加入浓硫酸的现象,写出浓硫酸与木炭反应的化学方程式吗?指出氧化剂、还原剂、氧化产物、还原产物吗?
(3)常温下,浓硫酸使铁、铝钝化
[浓硫酸、稀硫酸的组成及氧化性的比较]
 二、硝酸的氧化性
二、硝酸的氧化性
2、浓硫酸的脱水性:在蔗糖中加入浓硫酸现象①_____②_____③____。
蔗糖变黑的本质:
[思考]如果浓硫酸不慎沾到皮肤上,怎么办?
[比较]
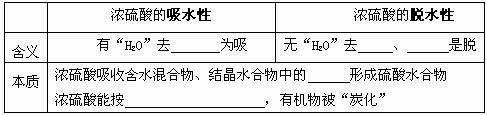
1、浓硫酸的吸水性:在盛有少量硫酸铜晶体的试管里注入浓硫酸,现象___________ ,结论____________。
[思考]实验室为什么常用浓硫酸干燥气体?
20. (1)S; 2S2-+SO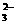 +6H+=3S↓+3H2O
+6H+=3S↓+3H2O
(2)Al(OH)3; Al3++3HCO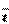 =Al(OH)3↓+3CO2↑
=Al(OH)3↓+3CO2↑
(3)BaCO3, 可能有BaSO4;
在沉淀丙中加入足量盐酸,若沉淀不能全部溶解,说明除BaCO3 外还有BaSO4;若全部溶解,则仅有BaCO3.
(4)①CO2 ②H2S ③SO2 ④CO2 H2S ⑤CO2 SO2
(5)S2-、SO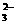 、AlO
、AlO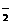
19. (1) Al3++2SO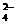 + NH
+ NH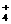 +2Ba2++4OH-=Al(OH)3↓+2BaSO4↓+NH3·H2O
+2Ba2++4OH-=Al(OH)3↓+2BaSO4↓+NH3·H2O
(2)B 600ml C. 750ml
18. (1)Cl2+2I-=2Cl-+I2
(2) 2Cl2+2Fe2++2I-=4Cl-+I2+2Fe3+
(3)6Cl2+2Fe2++10I-=12Cl-+2Fe3++5I2
17. (1)Fe3+. S2-. HCO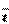 . SO
. SO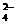 ; Cl-. K+
; Cl-. K+
(2)Ag++ H2SO4(浓)=== HNO3+2NO2 ↑+2H2O
14. D 15. D 16. D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com