
题目列表(包括答案和解析)
2.下列关于电解质的有关叙说正确的是
A.电解质溶液的浓度越大,其导电性能一定越强
B.强酸和强碱一定是强电解质,不管其水溶液浓度的大小,能完全电离
C.强极性共价化合物不一定都是强电解质。
D.多元酸、多元碱的导电性一定比一元酸、一元碱的导电能力强
1.漂白粉在溶液中存在下列平衡ClO-+H2O  HClO+OH-,下列措施能提高其漂白效益的是( )
HClO+OH-,下列措施能提高其漂白效益的是( )
A.加水稀释 B.通入CO2 C.加适量盐酸 D.加少量NaOH
12.实验室常用邻苯二甲酸氢钾(KHC8H4O4)来滴定氢氧化钠的的浓度,若氢氧化 钠的溶液浓度为0.1mol/l,到达终点时,溶液的PH约为9.1.
⑴为标定氢氧化钠溶液的浓度,应选 用作指示剂
⑵在测定氢氧化钠溶液浓度时,有下列操作:①向溶液中加入1-2滴酚酞指示剂 ②向锥形瓶中加20-30ml蒸馏水溶解 ③用氢氧化钠溶液滴定到溶液呈粉红色,半分钟不褪色④重复以上操作 ⑤准确称取0.4-0.5g邻苯二甲酸氢钾加入250ml锥形瓶中
⑥根据两次实验数据计算氢氧化钠的物质的量浓度.以上各步中,正确的(填序号)操作顺序是
⑶上述操作中,将邻苯二甲酸氢钾直接放到锥形瓶中溶解,对实验是否有影响?并说明理由:
⑷滴定前,用蒸馏水洗净碱式滴定管,然后加待测定的氢氧化钠溶液滴定,此操作对实验结果 (填<偏大><偏小>或<无影响>)
20(1)酚酞;
(2)⑤②①③④⑥
(3)无影响;因为是否加入不影响邻苯二甲酸氢钾的物质的量
(4)偏小
课后训练
11.⑴取0.2mol/LHCl溶液与0.2mol/LMOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答以下问题:
①混合溶液中由水电离出的c(H+) 0.2mol/LHCl溶液中由水电离出的c(H+);
(填“>”、“<”、或“=”)
②求出混合物中下列算式的精确计算结果(填具体数字):
c(Cl-)- c(M+)= mol/L,
c(H+)- c(MOH)= mol/L。
⑵如果取0.2mol/LMOH溶液与0.1mol/LHCl溶液等体积混合,测得混合溶液的PH<7,则说明MOH的电离程度 MCl的水解程度。(填“>”、“<”、或“=”)
答案:> 9.9*10-7 10-8 <
10.已知NaHSO4在水中的电离方程式为:NaHSO4===Na++H++SO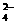 。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,不正确的是( )
。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,不正确的是( )
A.该温度高于25℃
B.由水电离出来的H+的浓度是1.0×10-10mol·L-1
C.NaHSO4晶体的加入抑制了水的电离
D.该温度下加入等体积pH为12的NaOH溶液可使该溶液恰好呈中性
9、物质的量浓度相同的下列物质的溶液①NH4Cl ②NH4HSO4 ③(NH4)2Fe(SO4)2 ④ (NH4)2SO4 ⑤(NH4)2CO3 ⑥CH3COONH4中[NH4+]由小到大的顺序是:
A、④②③①⑤⑥ B、⑤①③②④⑥ C、⑥③①②④⑤ D、⑥①②⑤④③
8.下列溶液一定是中性的是
A.将pH=5的盐酸稀释100倍所得溶液
B.c(H+)=c(OH-) =1×10-6mol·L-1的溶液
C.由强酸、强碱等物质的量反应得到的溶液
D.非电解质溶于水得到的溶液
7.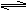 某二元酸(H2A)按下式发生电离:H2A=H++HA-;HA- H++A2-。关于下列四种
某二元酸(H2A)按下式发生电离:H2A=H++HA-;HA- H++A2-。关于下列四种
溶液的说法正确的是 ( )
①0.01mol/L的H2A溶液 ②0.01mol/L的NaHA溶液
③0.02mol/L的HCl溶液与0.04mol/L的NaHA溶液等体积混合
④0.02mol/L的NaOH溶液与0.02mol/L的NaHA溶液等体积混合
A.四种溶液中c(HA-)浓度大小:③>①>②>④
B.溶液①中一定不存在OH-
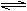 C.溶液②中存在水解平衡:HA-+H2O H2A+OH-
C.溶液②中存在水解平衡:HA-+H2O H2A+OH-
D.溶液③中有关离子浓度关系:c(HA-)+c(A2-)=c(Na+)
6.(2005江苏)常温下将稀NaOH溶液与稀CH3COOH溶液混合,不可能出现的结果是
A.pH > 7,且c(OH-) > c(Na+) > c(H+) > c(CH3COO-)
B.pH > 7,且c(Na+) + c(H+) = c(OH-) + c(CH3COO-)
C.pH < 7,且c(CH3COO-) >c(H+) > c(Na+) > c(OH-)
D.pH = 7,且c(CH3COO-) > c(Na+) > c(H+) = c(OH-)
5.pH=3的二元弱酸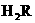 溶液与V L pH=11的NaOH溶液混合后,混合液的pH=7.下列判断正确的是( )
溶液与V L pH=11的NaOH溶液混合后,混合液的pH=7.下列判断正确的是( )
A.溶液的总体积为2 VL
B.溶液中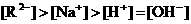
C.溶液中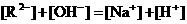 D.溶液中
D.溶液中
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com