
题目列表(包括答案和解析)
12、100℃时向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH=2,下列叙述不正确的是
A、此时水的离子积KW=1.0×10-14; B、水电离出的[H+]=1.0×10-10mol/L
C、水的电离度随温度升高而降低; D、[H3O+]>[SO42-]
11、在pH值都等于9的NaOH和CH3COONa两种溶液中,设由水电离产生的OH- 离子浓度分别为A摩/升与B摩/升,则A和B关系为
A、A>B B、A=10-4 B C、B=10-4 A D、A=B
10、室温下,等体积0.5mol/L的①KCl ②FeCl3 ③HF ④Na2CO3四种物质的水溶液中,所含阳离子数目由少到多的顺序是
A.④①②③ B.③①②④ C.①④③② D.④②①③
9.经测定某溶液中只含NH4+、C1- 、H+、OH-四种离子,下列说法错误的是……( )
A.溶液中四种粒子之间不可能满足:c(C1-)>c(H+)>c(NH4+)>c(OH-)
B.若溶液中离子间满足:c(NH4+)>c(C1-)>c(OH-)>c(H+),则溶液中溶质一定为:
NH4Cl和NH3·H2O
C.若溶液中离子间满足:c(C1-)>c(NH4+)>c(H+)>c(OH-)溶液中溶质一定只有NH4Cl
D.若溶液中c(NH4+)=c(Cl-),则该溶液一定显中性
8.下列说法正确的是( )
A.某二元弱酸的酸式盐NaHA溶液中: c(H+)+c(A2-)=c(OH-)十c(H2A)
B.0.020 mol/L的HCN(aq)与0.020 mol/L NaCN(aq)等体积混合得到碱性混合溶液中:
c(Na+)> c(CN-)
C.在物质的量浓度均为0.01mol/L的CH3COOH和CH3COONa的混合溶液中:
c(CH3COOH)+c(CH3COO-)=0.01 mol/L
D.c(NH4+)相等的(NH4)2SO4溶液、NH4HCO3溶液、NH4Cl溶液:
c[(NH4)2SO4] > c(NH4HCO3) > c(NH4Cl)
7.下列事实能说明醋酸是弱电解质的是
①醋酸与水能以任意比互溶 ②醋酸溶液能导电
③醋酸溶液中存在醋酸分子 ④0.1 mol/L醋酸的pH比0.1 mol/L盐酸pH大
⑤醋酸能和碳酸钙反应放出CO2 ⑥0.1 mol/L醋酸钠溶液pH=8.9
⑦大小相同的锌粒与相同物质的量浓度的盐酸和醋酸反应,醋酸产生H2速率慢
A.②⑥⑦ B.③④⑥⑦ C.③④⑤⑥ D.①②
6.为了更好地表示溶液的酸碱性,科学家提出了酸度(AG)的概念,AG=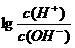 。已知某澄清溶液常温下的AG=12,则在此溶液中能大量共存的离子组( )
。已知某澄清溶液常温下的AG=12,则在此溶液中能大量共存的离子组( )
A.Na+、AlO2-、K+、ClO- B.MnO4-、K+、SO32-、Na+
C.Mg2+、SO42-、HCO3-、Na+ D.NH4+、NO3-、Al3+、Cl-
5.(2005广东)关于小苏打水溶液的表述正确的是 ( AD )
A. c(Na+)=c(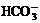 )+c(
)+c(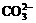 )+c(H2CO3)
)+c(H2CO3)
B. c(Na+)+c(H+)=c(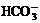 )+c(
)+c(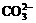 )+c(OH-)
)+c(OH-)
C. 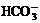 的电离程度大于
的电离程度大于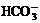 的水解程度
的水解程度
D. 存在的电离有:NaHCO3=Na++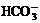 ,
,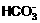
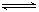
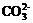 +H+。
+H+。
H2O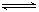 H++OH-
H++OH-
4、(2005上海)叠氮酸(HN3)与醋酸酸性相似,下列叙述中错误的是( )
A、HN3水溶液中微粒浓度大小顺序为:c(HN3)>c(H+)>c(N3¯)>c(OH¯)
B、HN3与NH3作用生成的叠氮酸铵是共价化合物
C、NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(N3¯) >c(OH¯)>c(H+)
D、N3¯与CO2含相等电子数
3.(2005江苏)在一定体积pH = 12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH = 11。若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是
A.1∶9 B.1∶1 C.1∶2 D.1∶4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com