
题目列表(包括答案和解析)
19.(6分)有一质量为Wg,相对分子质量为b的某种碱M(OH)2,在一定温度下完全溶解为VmL的饱和溶液。若溶液的密度为dg/cm3,则溶液的物质的量浓度是________,溶质的质量分数是__________,该温度下的溶解度是__________。
18.蓄电池在放电时起原电池的作用,在充电时起电解池的作用。下式是爱迪生蓄电池分别在充电和放电时发生的反应:
Fe+NiO2+2 H2O Fe(OH)2+Ni(OH)2
Fe(OH)2+Ni(OH)2
下列有关对爱迪生蓄电池的推断错误的是( )
A.放电时,Fe是负极,NiO2是正极
B.充电时,阴极上的电极反应式为Fe(OH)2+2e-====Fe+2OH-
C.放电时电解质溶液中的阴离子是向正极方向移动
D.蓄电池的电极必须浸入碱性电解质溶液中
17.1998年两位希腊化学家在《科学》杂志上发表论文,称他们在常压下把氢气和用氦气稀释的氮气分别通入一个加热到570℃的电解池(如下图)中,氢气和氮气在电极上合成了氨气,且转化率达到了78%。用来合成的电解质在电解池中起传导H+的作用,它是一种固体复合氧化物(缩写为SCY),电解池的两个电极则是吸附在SCY内外表面上的金属钯多晶薄膜。下列说法中不正确的是( )
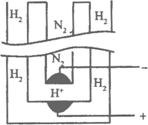
A.阳极的反应式为H2-2e-====2H+
B.阴极的反应式为 N2+6e-+6H+====2NH3
C.电解的总反应式
N2+3H2 2NH3
2NH3
D.电解的总反应式
3H++N3- NH3
NH3
16.在恒温恒容的密闭容器中放入一定量的NO2,发生反应2NO2(g)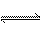 N2O4(g);ΔH<0,达到平衡后,若分别单独改变下列条件,重新达到平衡后,能使该反应的平衡混合气体平均相对分子质量减小的是( )
N2O4(g);ΔH<0,达到平衡后,若分别单独改变下列条件,重新达到平衡后,能使该反应的平衡混合气体平均相对分子质量减小的是( )
A.降低温度 B.通入NO2 C通入N2O4 D.升高温度
15.某可逆反应:mA(气)+nB(气) pC(气)(焓变为ΔH),其温度T、时间t与生成物C的体积百分数C%、平衡混合气体的平均相对分子质量M的关系如下图所示,下列结论正确的是( )
pC(气)(焓变为ΔH),其温度T、时间t与生成物C的体积百分数C%、平衡混合气体的平均相对分子质量M的关系如下图所示,下列结论正确的是( )
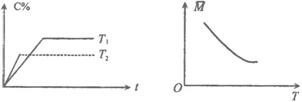
A.m+n>p ΔH>0 B.m+n>p ΔH<0
C.m+n<p ΔH>0 D.m+n<p Δ<0
14.某体积可变的密闭容器,盛有适量的A和B的混合气体,在一定条件下发生反应:A+3B 2C,若维持温度和压强不变,当到达平衡时,容器的体积为VL,其中C气体的体积占10%,下列推断正确的是( )
2C,若维持温度和压强不变,当到达平衡时,容器的体积为VL,其中C气体的体积占10%,下列推断正确的是( )
①原混合气体体积为1.2VL;②原混合气体的体积为1.1VL;③反应达平衡时气体A消耗0.05VL;④反应达平衡时气体B消耗掉0.05VL。
A.②③ B.②④ C.①③ D.①②
13.下列物质中能够与酸反应生成盐和水,但不属于碱性氧化物的是( )
A.Na2O B. Na2O2 C.Na D.CuO
12.我国发射“神五”所用的“长征2号”火箭的主要燃料是偏二甲肼(C2H8N2),氧化剂是N2O4,燃烧的产物若只有N2、CO2和H2O。有的国家用肼(N2H4)作为火箭发动机的燃料,NO2为氧化剂,反应生成N2和水蒸气。已知:N2(g)+2O2(g)====2NO2(g);ΔH=+67.7kJ·mo L-1,N2H4(g)+O2(g)====N2(g)+2H2O(g);ΔH=-534 kJ·mol-1
下列关于肼和NO2反应的热化学方程式中,正确的是( )
A.2N2H4(g)+2NO2(g)====3N2(g)+4H2O(1); ΔH=-1 135.7 kJ·mol-1
B.2 N2H4(g)+2NO2(g)====3N2(g)+4H2O(g);ΔH=+1135.7kJ·mol-1
C.N2H4(g)+NO2(g)====3/2N2(g)+2H2O(g);ΔH=-1135.7kJ·mol-1
D.2 N2H4(g)+2NO2(g)====3N2(g)+4H2O(g);ΔH=-1135.7 kJ·mol-1
11.把Ba(OH)2溶液逐滴滴入明矾溶液中,使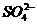 全部转化成BaSO4沉淀,此时铝元素的主要存在形式是( )
全部转化成BaSO4沉淀,此时铝元素的主要存在形式是( )
A.Al3+ B.Al(OH)3
C.AlO2或[Al(OH)4]- D.Al3+和AlC(OH)3
10.在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中大量共存的有( )
A.滴加石蕊试液显红色的溶液:Fe3+、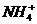 、Cl-、SCN-
、Cl-、SCN-
B.pH值为1的溶液:Cu2+、Na+、Al3+、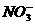
C.水电离出来的c(H+)=10-13mol/L的溶液:K+、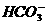 、Br-、Ba2+
、Br-、Ba2+
D.所含溶质为Na2SO4的溶液:K+、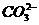 、
、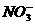 、Mg2+
、Mg2+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com