
题目列表(包括答案和解析)
19. (10分)下列表示分子结构的图示中,●表示短周期的几种元素的“原子实”[指原子除去最外电子层电子后剩余的部分,周围小黑点表示没有用于形成共价键的最外层电子,短线代表共价键。例如X2(X代表卤素原子):
]
(10分)下列表示分子结构的图示中,●表示短周期的几种元素的“原子实”[指原子除去最外电子层电子后剩余的部分,周围小黑点表示没有用于形成共价键的最外层电子,短线代表共价键。例如X2(X代表卤素原子):
]
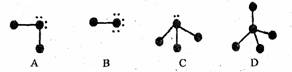
试回答下列问题:
(1)A、B、C、D四种“图示”中,所表示的物质可分为四组共____种。这些物质的分子中的电子总数可能为___或____。
(2)分子的空间构型为正四面体的物质的分子式是 。该组中,物质的稳定性顺序是____;它们沸点的变化与其余各组相比____(填“相同”或“不相同”),其原因是
(3)写出上述物质中的两种间相互反应生成离子化合物的化学方程式
(任写一个)。
18.(14分)某工业铁红中混有一种黑色的铁的氧化物杂质,为了解杂质的成分及测定铁红的纯度,化学兴趣小组的同学进行了实验探究。请你参与过程分析与交流。
[查阅资料]
①铁的常见氧化物
氧化亚铁(FeO)黑色固体,ω(Fe)=77.8%; 氧化铁(Fe2O3)红色固体,俗称铁红,
ω(Fe)=70.0%;四氧化三铁(Fe3O4)黑色固体,俗称磁性氧化铁,ω(Fe)=72.4%。
②草酸(乙二酸H2CO4)在浓H2SO4存在下受热分解的化学方程式为:
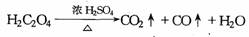
[实验准备]
①实验的装置图如下
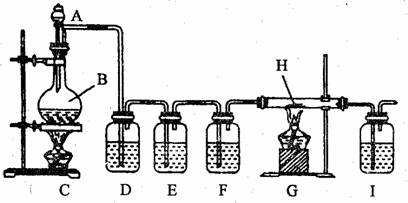
②药品及试剂
A、草酸 b、工业铁红 c、NaOH溶液 d、澄清石灰水
E、浓H2SO4 f、盐酸
[实验及数据]
取不同质量的样品进行实验,所得实验数据如下:
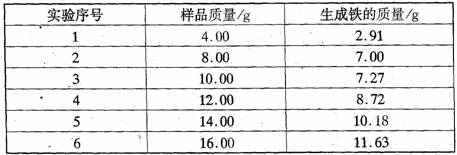
讨论与分析]
(1)兴趣小组的同学拟以纯净的CO还原铁的氧化物,所设计的实验装置中D、E、F应分别盛放的试剂为 、 、 、(填写序号,下同),其作用依次是
。
上述装置还有不完善之处,你建议改进措施是
(2)由实验数据不难得出,有-组实验数据不可靠,该组数据是 (填序号),该工业粗铁红所含杂质的化学式为 。
(3)该工业铁红中ω(Fe2O3)= 。
17.(8分)检查装置气密性是化学实验中的重要操作之一。试按要求回答下列问题:
(1)下列仪器或装置在使用前一定要检查气密性的是____(填序号,下同)。
A、容量瓶 B、洗气瓶 C、分液漏斗 D、酸(碱)式滴定管
(2)下列关于不进行气密性检查可能导致后果的叙述中,正确的是____。
A、收集不到气体 B、造成环境污染
 C、观察到的实验现象有误 D、引发爆炸事故 ·
C、观察到的实验现象有误 D、引发爆炸事故 ·
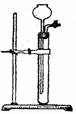
(3)为检查右图所示简易气体发生装置的气密性,甲、乙两位同学进行了以
下操作和方案设计。
①甲同学认为,只要往漏斗中加水,便可检验其气密性是否良好。经检验他
的方案可行。则甲同学的操作方法、现象和结论是 。
②乙同学设计的方案是:往漏斗中注人一定量的水至浸没长颈漏头下端。
关闭活塞,用手捂住试管中上部,待漏斗中液面上升一定高度,打开活塞让液面回落后,迅速关闭活塞,松开手,见漏斗中液面低于试管中液面且不再升降,说明气密性良好。乙同学设计方案的原理是 。
16.向某NaOH溶液中通人CO2气体后得溶液M,因CO2通人量的不同,溶液M的组成也不同。若向M中逐滴加人盐酸,产生的气体体积V(CO2)与加人盐酸的体积V(HCl)的关系有下列图示四种情况,且(2)、(3)、(4)图中分别有OA<AB,OA=AB,OA>AB,则下列分析与判断不正确的是(不计CO2的溶解)
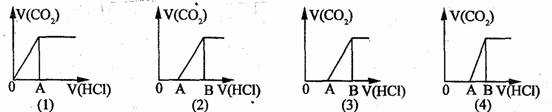
A、M中只有一种溶质的有(1)和(3)
B、M中有两种溶质的有(2)和(4)
C、(2)图显示M中c(NaHCO3)>c(Na2CO3)
D、(4)图显示M中c(NaHCO3)>c(Na2CO3)
15.25℃时,在25 mL o.1 mol·L-1的NaOH溶液中,逐滴加入
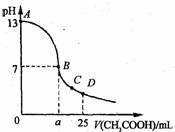 0.2 mol·Lˉ1的CH3COOH溶液。溶液pH的变化曲线如图
0.2 mol·Lˉ1的CH3COOH溶液。溶液pH的变化曲线如图
所示。下列分析的结论中,正确的是 ·
A、B点的横坐标a=12,5
B、C点时c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
C、D点时c(CH3COO-)+c(CH3COOH)=2c(Na+)
D、曲线上A、B间任一点,溶液中都有:
c(Na+)>c(CH3COOˉ)>c(OH-)>c(H+)
14.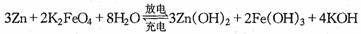 高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压,高铁电池的总反应为:
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压,高铁电池的总反应为:
下列叙述不正确的是
A、放电时负极反应式为:Zn-2eˉ+2OHˉ=Zn(OH)2
B、放电时每转移3mol电子,正极有1 mol K2FeO4被氧化
C、充电时阳极反应式为:Fe(OH)3 - 3e-+5OHˉ=FeO42ˉ+4H2O
D、放电时正极附近溶液的碱性增强
13.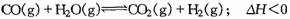 在容积可变的密闭容器中存在如下反应:
在容积可变的密闭容器中存在如下反应:
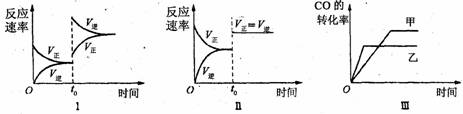
12.为实现2008北京“科技奥运”战略,我国兴奋剂检测生物芯片装置
已定型和批量生产,可快捷检测常见的16种兴奋剂。已知某兴奋
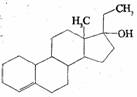 剂乙基雌烯醇(etylestrenol)的结构如右图所示。下列叙述中正确
剂乙基雌烯醇(etylestrenol)的结构如右图所示。下列叙述中正确
的是
A、该物质可以视为酚类
B、在浓硫酸作用下,分子内消去一个水分子,产物有二种同分异
构体
C、能使溴的四氯化碳溶液褪色
D、该物质分子中的所有碳原子均共面
11.工业生产中物质的循环利用有多种模式。例如:
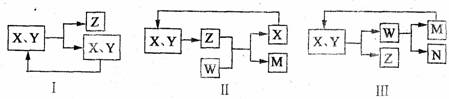
下列表述正确的是
A、图I可用于合成氨中的N2、H2的循环
B、图I可用于氨碱法制纯碱中CO2的循环
C、图Ⅱ可用于电解饱和食盐水中NaCl的循环
D、图Ⅲ可用于氨氧化法制硝酸中NO的循环
9,下列叙述中,结论(事实)和对应的解释(事实)均不正确蚺是
A、金刚石的熔沸点高于晶体硅,因为C一C键能大于Si一Si键能
B、稀有气体的晶体属于原子晶体,因为其组成微粒是原子,不存在分子间作用力
C、二氧化硅晶体中不存在简单的SiO2分子,因为其晶体是含有硅氧四面体的空间网状结构
D、分子空间构型为正四面体结构的分子中化学键的键角不一定是109028’,因为键角还有可能为60°
10.一定能在下列溶液中大量共存的离子组是
A、使紫色石蕊试液变蓝的溶液:Na+ AlO2- S2ˉ SO42ˉ
B、pH=0的溶液:Zn2+ NO3- Cl- I-
C、由水电离的c(H+)=10ˉ14 mol/ L-l的溶液中:Ba2+ K+ Na+ HCO3-
D、含有大量Al3+的溶液:H+ Cu2+ Mg2+ SO42-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com