
题目列表(包括答案和解析)
版权归四川省黄金屋文化传播有限责任公司所有
21.某校化学小组学生利用下图所示装置进行“铁与水反应”的实验,并利用产物进一步制取FeCl3•6H2O晶体。(图中夹持及尾气处理装置均已略去)
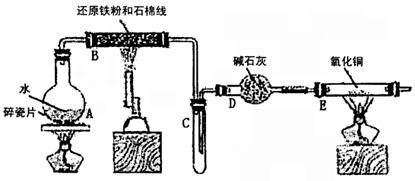
(1)装置B中发生反应的化学方程式是 。
(2)装置E中的现象是 。
(3)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。简述检验滤液中Fe3+的操作方法:
(4)该小组学生利用上述滤液制取FeCl3•6H2O晶体,设计流程如下:
|
 晶体
晶体
①步骤I中通入Cl2的作用是 。
②步骤II从FeCl3稀溶液中得到FeCl3•6H2O晶体的主要操作包括:
。
20.如图所示,各物质间存在如下相互转化关系,其中F为金属,能和氧化铁反应,生成单质。E和K为无色的气体单质,其它物质均为化合物,A为无色气体,C为无色液体,B是淡黄色固体。
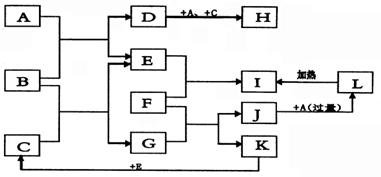
试回答下列问题:
(1)写出B的电子式 ,J的化学式 。
(2)F在元素周期表中 周期 族。
F能与下列物质反应放出H2的是 (只填序号)。
A. NH3•H2O B. 浓H2SO4 C. 稀HCl
D. KHSO4溶液 E. NaOH溶液 F. 稀HNO3
(3)写出F与G反应的离子方程式 ,J生成L的离子方程式 。
(4)分别写出下列反应的化学方程式:
①H固体转化为D:
②F与氧化铁反应:
19.短周期的三种元素X、Y、Z,原子序数依次减小,原子核外电子层数之和是5,X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和;X元素原子可以与Z元素原子形成1:1的无机化合物,Y和Z可以形成YZ3的化合物。请回答:
(1)X元素是 ,Y元素是 ,Z元素是 。
(2)YZ3化合物的电子式是 ,它的空间构型是 (不画图,文字描述),是 (极性或非极性)分子。
(3)Y的最高价氧化物的水化物能与YZ3反应,写出反应的离子方程式:
(4)写出工业合成YZ3的化学方程式;
(注明条件)
18.已知三角锥形分子E和直线形分子G反应,生成两种直线形分子L和M,(组成E、G、L、M分子的元素原子序数均小于10)如下图,则下列判断错误的是
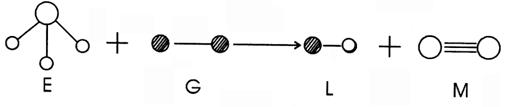
A. G是最活泼的金属单质 B. L是极性分子
C. E能使紫色的石蕊试液变成蓝色 D. M化学性质活泼
广安市高2006级“一诊”试题
化 学
总 分 栏
第Ⅰ卷答题栏
第Ⅱ卷(非选择题,共46分)
17.25℃时,pH=2某酸(HA)与pH=12某碱(BOH)等体积混合后,混合液的pH=10,下列描述中正确的是
A. 若两者中有一种为强电解质,则一定是BOH
B. 若HA是强酸,混合液中离子浓度关系一定是
C. 若混合液中存在离子水解,则一定是A-水解
D. 两者混合后,BOH有可能过量
16.在水中加入等物质的量的Ag+、Ba2+、 、
、 、
、 ,将该溶液放入惰性材料作电极的电解槽中通电片刻,则氧化产物与还原产物的质量比为
,将该溶液放入惰性材料作电极的电解槽中通电片刻,则氧化产物与还原产物的质量比为
A. 35.5:10.8 B. 16:207 C. 8:1 D.108:35.5
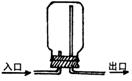
15.下列各气体能用如右图所示装置收集的是
A. NO B. CO C. H2 D. Cl2
14.Cl2和SO2均能使品红褪色,下列说法正确的是
A. 等物质的量的Cl2和SO2同时通入品红溶液中,变色最快
B. 两者漂白原理相同
C. 将褪色的品红溶液加热,可区别是Cl2漂白还是SO2漂白
 D. 分别通入H2S溶液中,可区别Cl2和SO2
D. 分别通入H2S溶液中,可区别Cl2和SO2
13.下列除杂质的方法不可行的是
A. 用过量的氨水除去Al3+溶液中的少量Mg2+
B. 将混合气体通过灼热的铜网除去N2中少量的O2
C. 用MgCO3固体可除去酸性MgCl2溶液中少量的FeCl3
D. 除去FeCl3酸性溶液中少量的FeCl2,加入稍过量双氧水后放置
12.某无色透明溶液能与铝反应放出H2,则该溶液中可大量共存的离子是
A. OH- Mg2+ 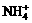 Cl- B.
Cl- K+ Na+ Ba2+
Cl- B.
Cl- K+ Na+ Ba2+
C. Ba2+ Cl- Cu2+  D.
H+ Na+
D.
H+ Na+  Cl-
Cl-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com