
题目列表(包括答案和解析)
9.下列反应的离子方程式正确的是 ( )
A.向溴化亚铁溶液通入过量氯气:
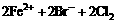 ===
===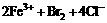
B.向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全:
2Al3++ 3SO42-+ 3Ba2++ 6OH-2Al(OH)3↓+ 3BaSO4↓
C.乙醛与银氨溶液在热水浴中的反应:
CH3CHO+2[Ag(NH3)2]++2OH-  CH3COO-+NH4++2Ag↓+3NH3+H2O
CH3COO-+NH4++2Ag↓+3NH3+H2O
D.苯酚钠溶液中通入少量的CO2:
2C6H5O-+CO2 +H2O→2C6H5OH+CO32-
8、设NA为阿伏加德罗常数,下列叙述正确的是( )
A、1molNa2O2固体中含有2NA个阴离子
B、1molCH4与1molSiO2中所含的共价键数目均为4NA
C、1molFe3+完全水解生成氢氧化铁胶体粒子的数目为NA
D、1mol/L盐酸和1mol/LCH3COOH溶液中的H+数目比较:前者有NA个,后者少于NA个
7、 已知在101kPa时:CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-820kJ/mol。下列说法中正确的是( )
已知在101kPa时:CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-820kJ/mol。下列说法中正确的是( )
A、反应过程中能量关系可用右图表示
B、CH4的燃烧热是820kJ
C、11.2LCH4完全燃烧放出热量410kJ
D、若将此反应设计成原电池,甲烷在正极被氧化
6. 2006年诺贝尔化学奖授予美国科学家Roger.D.Kormberg,他揭示了真核生物体内的细胞如何利用基因内存储的信息生产蛋白质。下列关于蛋白质的说法中正确的是(
)
2006年诺贝尔化学奖授予美国科学家Roger.D.Kormberg,他揭示了真核生物体内的细胞如何利用基因内存储的信息生产蛋白质。下列关于蛋白质的说法中正确的是(
)
A.蛋白质均为天然有机高分子化合物,没有蛋白质就没有生命
B.蛋白质均易溶于水,均能跟浓硝酸作用变黄
C.HCHO溶液或(NH4)2SO4溶液均能使蛋白质变性
D.可以采用多次盐析或多次渗析的方法分离提纯蛋白质
29. (15分)有机物A的化学式为C9H16O4,且分子内无支链。有机物B和A结构相似,A→K相互间转化关系如下图所示(转化过程中产生的无机物均已略去):
请回答下列问题:
(1)A→K 十一种有机物中属于酯类的是 (填对应的字母)。
(2)A→K 十一种有机物中有 对物质可互称为同系物。
(3)A→K 十一种有机物中可发生银镜反应的物质有 (填对应字母)。
(4)B的结构简式为 。
(5)C→J该反应的类型是 反应。
(6)C在适当的条件下(无其它反应物),也可形成有机高分子化合物,该有机高分子化合物的结构简式为 。
28.(16分)为了研究氯水能否和碳酸钙发生化学反应,某学生设计如下实验:
实验一:向盛有饱和氯水的锥形瓶中加入大理石,并充分振荡,观察到氯水的黄绿色褪去并同时产生少量气体。
实验二:取上述实验一后锥形瓶中清液,进行如下实验:
(1)该清液滴在有色布条上有极强的漂白作用。
(2)该清液中滴加碳酸钠溶液产生白色沉淀。
(3)该清液中滴加盐酸可产生大量气体。
(4)该清液加热后变浑浊并产生大量气体。
实验三:该学生设想用下列装置收集实验二中产生的气体作进一步检验。
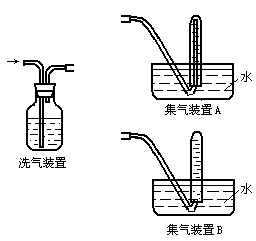
回答下列问题:
(1)在实验二中,清液滴在有色布条上有极强的漂白作用说明该清液中含有 (写化学式)。
(2)在实验二中,清液中滴加碳酸钠溶液产生白色沉淀说明该清液中含有 离子。
(3)在实验二中,清液中滴加盐酸产生的气体是 。
(4)在实验二中,清液加热后产生浑浊的原因是因为生成了 物质。
(5)实验三中,洗气装置内的洗涤液一般用 溶液。
(6)在反应物的量相同情况下,该学生尝试用集气装置A和集气装置B分别和洗气装置相连来收集气体。选用集气装置 (选填“A”或“B”)可收集到更多的气体。
(7)经试验,该学生最终选用集气装置B进行下一步实验。其选择装置B的原因是 。
(8)该学生通过上述实验,写出氯水和碳酸钙反应的化学方程式为 。
27.(14分)已知某无色溶液中只含有包括Na+、CH3COO-在内的四种离子,请回答下列问题:
(1)若该溶液中只含有一种溶质,则该溶液显 性,相关的离子方程式为 。
(2)若该溶液呈酸性,则溶液中的溶质为 。
(3)若溶液中含有两种溶质,且溶液呈碱性,则该溶液中不可能出现的离子浓度大小关系是 。(选填编号字母)
(A)c(Na+)>c(CH3COO-) (B)c(CH3COO-)> c(Na+) (C)c(OH-)> c(Na+)
(D)c(Na+) > c(OH-) (E)c(OH-)> c(CH3COO-) (F)c(CH3COO-)> c(OH-)
(4)若溶液中含有物质的量相等的两种溶质,且该溶液中加入少量的强酸或少量的强碱时,溶液的pH几乎不变,试解释原因 。
26.(15分) A、B、C是三种常见的短周期元素,它们的原子序数逐渐增大,B元素原子最外层电子数是C元素原子最外层电子数的一半,A元素原子最外层电子数比B多一个。甲、乙、丙是三种最高价含氧酸的钠盐,甲中含B元素,乙中含C元素,丙中含A元素,甲、丙的水溶液均有较强的碱性,乙的水溶液pH小于7。丁为一种气体,戊为淡黄色固体。甲、乙、丙、丁、戊、已六种物质之间的相互反应关系如下图:(图中略去了物质转化时的部分生成物)
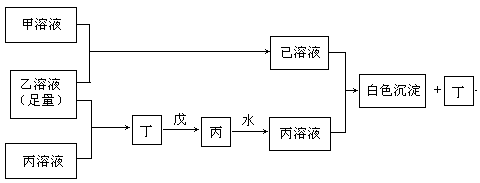
回答下列问题:
(1)写出A、B、C三种元素的元素符号 、 、 。
(2)写出戊的电子式 。
(3)若乙溶液不足量,乙溶液分别和甲、丙溶液也能发生化学反应,但生成物不是已和丁,写出不足量的乙溶液分别和甲溶液、丙溶液反应时的离子反应方程式:
乙+甲 ;乙+丙 。
(4)写出已溶液和丙溶液反应的离子方程式: 。
13.如右图所示,A、B为石墨电极,烧杯中加入的是只含一种溶质的电解质溶液500 mL,接通直流电源后,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;则下列判断正确的是
A.A电极的名称为阳极
B.B电极上的电极反应为2H++2e-==H2↑
C.总反应的离子方程式为:2Cu2++2H2O 2Cu+O2↑+4H+
2Cu+O2↑+4H+
D.电解一段时间后溶液的pH会升高
12.设NA为阿伏加德罗常数,钠的摩尔质量为M g·mol -1,钠的密度为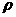 g·cm-3,则以下说法中,正确的是
g·cm-3,则以下说法中,正确的是
①1 g Na所含原子数为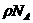 个 ②1 cm3 Na所含原子数为
个 ②1 cm3 Na所含原子数为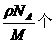 ③1个钠原子的质量为
③1个钠原子的质量为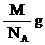 ④1 个钠原子占的体积为
④1 个钠原子占的体积为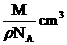 ⑤1 g钠在足量O2中燃烧失去的电子数为
⑤1 g钠在足量O2中燃烧失去的电子数为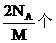
A.①② B.②③④ C.①②④ D.③④⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com