
题目列表(包括答案和解析)
8.2008北京奥运吉祥物福娃外材为纯羊毛线,内充物为无毒的聚酯纤维
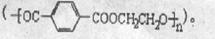 下列说法正确的是
下列说法正确的是
A.羊毛与聚酯纤维的化学成分相同 B.聚酯纤维和羊毛一定条件下均能水解
C.该聚酯纤维单体为对苯二甲酸和乙醇 D.由单体合成聚酯纤维的反应属加聚反应
7.下列表达式正确的是
A.甲基的电子式可写为: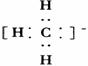
B.HClO的结构式为:H-Cl-O
C.乙醛的结构简式可写为:CH3COH
D.F¯ 的电子排布式 1s22s22p6
6.今年广东北江发生严重的水体镉污染事件,专家确定用1200吨的聚合铁{简称PFS,化学式为:[Fe2(OH)n(SO4)3-n/2]m,n<5,m<10}分批加入,利用PFS在水体中形成絮状物,以吸附镉离子。结合题中信息,下列说法不正确的是
A.10848Cd核素中中子数为60
B.含镉废电池应进行回收处理
C.PFS中铁显十2价
D.实验室由FeSO4溶液制PFS需经过氧化、水解和聚合的过程
5.对下列各种溶液中所含离子的判断合理的是
A.使紫色石蕊试液变红色的溶液中可能含:K+、Na+、Ca2+、HCO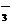
B.某溶液,加铝粉有氢气放出,则溶液中可能含:K+、Na+、H+、NO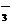
C.在c(H+)=10-14mol/L的溶液中可能含:Na+、A1O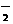 、CO
、CO 、SO
、SO
D.向无色溶液中加氯水变橙色,溶液中可能含: SO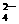 、Br-、OH-、Ba2+
、Br-、OH-、Ba2+
4.根据所学知识,下列有关胶体的说法中正确的是
A.将饱和的FeCl3溶液加热至沸,制得Fe(OH)3胶体
B.将磁性物质制成胶体离子作为药物的载体,可在磁场作用下送到病灶
C.化工生产上可利用丁达尔效应将油漆粒子均匀地沉积在镀件上
D.在Al(OH)3胶体中逐滴加入Ba(OH)2溶液至过量,先有沉淀,后沉淀溶解
3.下列分子结构图中的大黑点表示原子序数小于10的元素的“原子实”(指原子除去最外层电子的剩余部分),小黑点表示没形成共价键的最外层电子,短线表示共价键。其中分子结构图与化学式关系错误的是
A.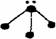 (NH3)
B.
(NH3)
B. (HCN)
(HCN)
C.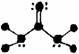 (C3H4O)
D.
(C3H4O)
D.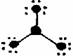 (BF3)
(BF3)
2.亚硝酸盐中毒,又名乌嘴病、紫绀病等。亚硝酸盐可将正常的血红蛋白氧化成高铁血红蛋白,血红蛋白中的铁元素由二价变为三价,失去携氧能力,使组织出现缺氧现象。美蓝是亚硝酸盐中毒的有效解毒剂。下列说法不正确的是
A.在中毒过程中血红蛋白被氧化 B.中毒时亚硝酸盐发生氧化反应
C.药品美蓝应具有还原性 D.解毒时血红蛋白被还原
1.汽车排放的尾气中因含有氮的氧化物而污染大气,造成产生氮的氧化物的主要原因是
A.燃烧含氮化合物燃料 B.燃烧含铅汽油
C.由于燃烧不充分 D.在气缸中N2被氧化
29.(15分)(1)在100 mL浓度为1mol•Lˉ1的明矾[KAl(SO4)2•12H2O]溶液中,加入
▲ mL 1mol•Lˉ1的氢氧化钡溶液,能使产生的沉淀中Al(OH)3质量最多。当加入过量的1mol•Lˉ1的氢氧化钡溶液后,产生的沉淀的质量是 ▲ g。(6分)
(2)在2L恒容的密闭容器中,加入1molN2和3molH2,在一定温度和催化剂条件下使其反应,当反应到8min时达到平衡,此时NH3的浓度c (NH3) = a mol•Lˉ1;分离出NH3,剩余气体回收于原容器,再向该容器通入1molN2和3molH2,平衡时N2的转化率比第一次增大5%,c (NH3) = b mol•Lˉ1。
①下列属于工业上增加氮气转化率的措施是 ▲ ;
A、提高反应温度至500℃ B、使用催化剂
C、增大压强至20-50MPa D、充入过量的氮气
②第一次达到平衡时c(N2)=c(NH3),则a= ▲ ;第二次达到平衡时b= ▲ ;
26.(12分)下列图中A-J分别代表相关反应中的一种物质,已知A是常用作肥料的无机盐,A分解得到相等物质的量的B、C、D,已知F是一种单质,图中有一些生成物未写出。
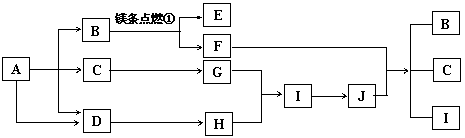

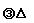
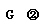
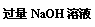
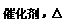
请填写以下空白:
(1)A的化学式___▲___,D的电子式__▲__ ,B物质的晶体类型为__▲ 。
(2)写出反应②的化学方程式:_______▲_____;
(3)写出反应④的化学方程式,并标出电子的转移方向和数目:____▲______。
27(16分)某研究性学习小组的同学为在实验室再现二氧化硫催化氧化的过程,并制取少量三氧化硫晶体,设计了如图所示的装置。
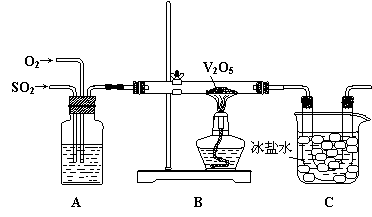
已知: ①三氧化硫遇水生成硫酸并放出大量热,容易形成酸雾。
②V2O5在450℃左右,活性最好,温度过高或过低都会使催化剂活性下降。
试回答:
(1)已知3.2g二氧化硫被氧气完全氧化成气态三氧化硫时,可以放出4.915kJ热量。反应的热化学方程式为 ▲ ;
(2)A装置可用来观察二氧化硫和氧气的进气量。实验时使A中氧气导管冒出的气泡与二氧化硫导管冒出的气泡速率相近,其目的是 ▲ ;A中的药品是 ▲ ;
(3)检查完装置的气密性且加入药品后,开始进行实验。此时首先应该进行的操作是
▲ ;
(4)在实验过程中不能持续加热的理由是 ▲ ;
(5)C装置用来收集三氧化硫,其中冰盐水的作用是 ▲ ;
(6)为了减轻实验对环境的污染,请你设计尾气处理装置,用简要文字回答: ▲ 。
 28.(17分)已知如下信息:
28.(17分)已知如下信息:
① RNH2+R∕CH2Cl RNHCH2R∕+HCl (R和R∕代表烃基)
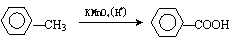
② 苯的同系物能被高锰酸钾氧化,如:

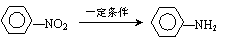 ③
③
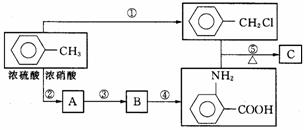
化合物C是制取消炎灵(盐酸祛炎痛)的中间产物,其合成路线为:
请回答下列问题:
(1)写出反应④的主要产物中含有的官能团的结构简式(除苯环外)____▲____;
(2)写出B、C物质的结构简式是_____▲_____, ▲ ;
(3)写出反应①②的化学方程式 ①______▲____,②___▲____;
(4)反应①-⑤中,属于取代反应的有(填反应序号)______▲____;
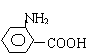 (5)写出符合下列要求的
的含有苯环的同分异构体
(5)写出符合下列要求的
的含有苯环的同分异构体
①含硝基的(任选一种) ▲ ;②属于酯类(任选一种) ▲ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com