
题目列表(包括答案和解析)
7.Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,若反应中Na2Sx
与NaClO的物质的量之比为1∶16,则x值是
A.2 B.3 C.4 D.5
6.X、Y、Z均为短周期元素。已知X元素的原子核内无中子,Y元素的原子核外最外层电
子数是其次外层电子数的2倍,Z元素是地壳中含量最丰富的元素。有下列含该三种元素
的化学式:①X2Y2Z2 ②X2YZ3 ③X2YZ2 ④X2Y2Z4 ⑤X3YZ4 ⑥XYZ3,其中可能存在对应物质的是
A.①②④⑤ B.①②③④ C.②③④ D.②⑤⑥
5.下列表述正确的是
①人造刚玉熔点很高,可用作高级耐火材料,主要成分是二氧化硅
②提前建成的三峡大坝使用了大量水泥,水泥是硅酸盐材料
③化学家采用玛瑙研钵摩擦固体反应物进行无溶剂合成,玛瑙的主要成分是硅酸盐
④太阳能电池可采用硅材料制作,其应用有利于环保、节能
⑤游客佩戴由添加氧化亚铜的二氧化硅玻璃制作的变色眼镜来保护眼睛
A.①②③ B.③④⑤ C.②④ D.③⑤
4.分类方法在化学学科的发展中起到了非常重要的作用。下列分类标准合理的是
①根据酸分子中含有的H原子个数将酸分为一元酸、二元酸等
②根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应
③根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液
④根据反应中的热效应将化学化学反应分为放热反应和吸热反应
A.①③ B.②④ C.①②④ D.②③④
3.用NA表示阿伏加德罗常数的值,下列说法正确的是
A.60.0g二氧化硅晶体中,含有“Si-O”键的数目为NA
B.34g过氧化氢分子中极性共价键的数目为NA
C.标准状况下,22.4L甲烷和氨气的混合气体所含有的电子总数约为10NA
D.1molT2气体分子(超重氢分子)中所含的中子总数为2NA
2.根据下表中列出的数据,判断下列热化学方程式书写不正确的是
|
化 学 键 |
H-H |
Cl-Cl |
H-Cl |
|
生成1mol化学键时放出的能量 |
436kJ·mol-1 |
243kJ·mol-1 |
431kJ·mol-1 |
A.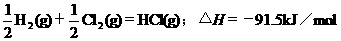
B.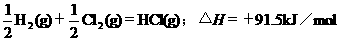
C.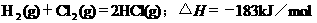
D.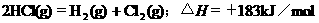
1.下列各原子或离子的电子排布式错误的是
A.Si 1s22s22p2 B.O2- 1s22s22p6
C.Na+ 1s22s22p6 D.Al 1s22s22p63s23p1
32.(11分)
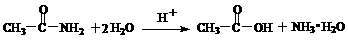 已知:
已知:
有机物A是一种镇痛解热药品,其结构简式为:
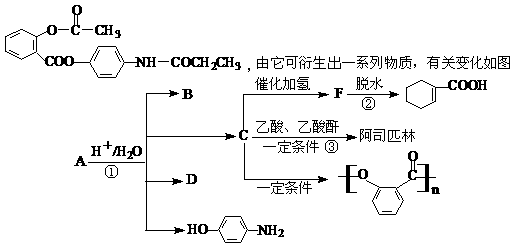
(1)B、D的关系是 (填序号)。
a.互为同位素 b.互为同系物 c.互为同分异构体 d.同类物质
(2)写出②③反应的化学方程式,注明反应类型
反应② ; 。
反应③ ; 。
(3)1molA在氢氧化钠溶液中水解,最多消耗氢氧化钠 mol。
(4)能与FeCl3溶液发生显色反应的属于酯类的C的同分异构体有 种。
31.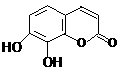 (9分)瑞香素是一种具有抗菌、抗炎、抗凝血等生物活性的香豆素化合物,其分子结构如图所示。
(9分)瑞香素是一种具有抗菌、抗炎、抗凝血等生物活性的香豆素化合物,其分子结构如图所示。
回答下列问题:
(1)瑞香素的化学式为 。
(2)瑞香素含有的官能团有 (写名称)
(3)瑞香素与溴的四氯化碳溶液反应的化学方程式(有机物用结构简式表示)是 ;
(4)瑞香素与氢氧化钠溶液反应的化学方程式(有机物用结构简式表示)是 ;
(5)一定条件下,瑞香素与足量氢气反应所得产物的结构简式(可用键线式表示) 。
30.(12分)占地球上储量99%的溴分布在海洋中,从海水中提取溴的一般过程如下:

(1)在过程②中,海水中的Br-离子转化为溴的离子方程式是_____ 。
(2)过程③之所以能将溴以蒸气状态吹出,从物质结构知识角度来看是因为 。
(3)溴和其它卤素原子可形成卤素互化物,如果将3.73g 溶于水,再通入SO2,使其发生如下反应:
溶于水,再通入SO2,使其发生如下反应:
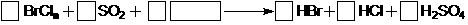

然后将所得溶液调至中性,再加入过量的Ba(NO3)2溶液,充分反应后除去生成的沉淀,再将所得滤液用过量AgNO3溶液处理,可得沉淀12.37g。
①配平上述化学反应方程式。
②确定该卤素互化物 中的n(写出计算过程)
中的n(写出计算过程)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com