
题目列表(包括答案和解析)
9.氕化锂、氘化锂、氚化锂可以作为长征2号火箭发射的重要燃料,下列说法正确的是
A.H、D、T之间互称同素异形体 B.氕化锂、氘化锂、氚化锂起催化剂作用
C.LiH、LiD、LiT的摩尔质量之比为1﹕2﹕3 D.它们都是强还原剂
8.美国科学家用有机分子和球形笼状分子C60,首次制成了“纳米车”(如图),每辆“纳米车”是用一个有机分子和4个球形笼状分子“组装”而成。 “纳米车”可以用来运输单个的有机分子,生产复杂的材料和药物,成为“纳米生产”中的有用工具。下列说法正确的是
“纳米车”可以用来运输单个的有机分子,生产复杂的材料和药物,成为“纳米生产”中的有用工具。下列说法正确的是
A.我们可以直接用肉眼清晰地看到这种“纳米车”的运动
B.“纳米车”的诞生,说明人类操纵分子的技术进入一个新阶段
C.C60是一种新型化合物 D.C60熔点比金刚石熔点高
7.信息、材料、能源被称为新科技革命的“三大支柱”。下列有关资讯错误的是
A.在即将到来的新能源时代,核能、太阳能、氢能将成为主要能源
B.目前,中、美、日等国掌握的陶瓷发动机技术,能较大程度地降低能耗,节约能源
C.光缆在信息产业中有广泛应用,制造光缆的主要材料是单质硅
D.结构陶瓷碳化硼(B4C3)常用于制造切削工具,它是一种新型无机非金属材料,属于原子晶体
4.下列除去括号内杂质的有关操作方法不正确的是:①苯(苯酚):加入NaOH溶液,分液;②乙醇(乙酸):加KOH溶液,分液;③苯(甲苯):加KMnO4/NaOH溶液,蒸馏;④乙烷(乙烯):酸性KMnO4
溶液,洗气;⑤乙酸乙酯(乙酸):加入乙醇和浓硫酸,使乙酸全部转化为乙酸乙酯;⑥淀粉溶液(葡
萄糖):渗析;⑦提取溶解在水中的少量碘:加入CCl4,分液,取出有机层再分离
A.①②④⑤ B.②③④⑤ C.②④⑤ D.④⑤⑥⑦
[ ]5教材是学习的重要材料,但不能迷信教材。下列是从中学化学教材中摘录的部分表述内容,根据你学的化学知识判断,其中不够科学严密的是
A.结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物。
B.离子方程式不仅可以表示一个具体的化学反应,而且还可以表示同一类型的离子反应。
C.元素性质的周期性变化是元素原子的核外电子排布的周期性变化的必然结果。
D.不同的化学反应,具有不同的反应速率,这说明,参加反应的物质的性质是决定化学反应速率的重要因素。
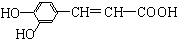 [ ]6. 咖啡酸具有止血、镇咳、祛痰等疗效,其结构简式为
。下列有关咖啡酸的说法中,不正确的是
[ ]6. 咖啡酸具有止血、镇咳、祛痰等疗效,其结构简式为
。下列有关咖啡酸的说法中,不正确的是
A.咖啡酸可以发生还原、取代、加聚等反应 B.咖啡酸与FeCl3溶液可以发生显色反应
C.1 mol咖啡酸可与4 mol H2发生加成反应 D.1 mol咖啡酸最多能消耗3 mol的NaHCO3
3. 下列排列顺序正确的一组是
A.半径:Fe(OH)3胶粒>I->K+>Na+ B.熔沸点:HF<HCl<HBr<HI
C.还原性:Fe3+>Cu2+>Fe2+>Zn2+ D.热稳定性:H3PO4<H2SO3<H2SiO3<H2SO4
2.固体电解质又称离子导体,在一定温度范围内具有很强的导电性。固体电解质虽然是固体,但却像电解质溶液一样以离子为导电载体。下列物质能作为固体电解质的是
A.银 B.碳素钢 C.硝酸钾晶体 D.水晶
1.下列关于铜电极的叙述,正确的是
A.铜锌原电池中铜为负极,发生氧化反应 B.用电解法精炼粗铜时,粗铜作阴极
C.在镀件上电镀同时,可用精铜做阳极 D.电解稀硫酸制H2、O2时,可用铜作阳极
25.(11分)未来的交通工具将采用新一代无机非金属材料制成的无水冷发动机,这类材料中研究得较多的是化合物G。
(1)G可以由化合物E(含两种元素)与NH3反应而生成,同时产生HCl气体,G的相对分子质量为140,分子中硅元素的质量分数为60%,另有元素J。请推断:
①化合物G的化学式为
②若1mol NH3和0.75mol E恰好完全反应,则化合物E的化学式为
(2)为了使化合物G能成为新一代汽车发动机材料,现采用常压下在其中添加氧化铝,经高温烧结制成一种高强度、超硬度、耐磨损、抗腐蚀的陶瓷材料,它的商品叫“赛伦”(Sialon),化学通式可表达为Si6-xAlxOxJ8-x。在接近于1700oC时x的极限值约为4.0,在1400oC时x为2.0,以保持整个化合物呈电中性。试通过计算说明随温度的升高,赛伦中铝元素的质量分数的变化趋势。

24.(7分)某制药公司生产一种钙片,其主要成分是碳酸钙。为测定钙片中碳酸钙的质量分数,取一钙片碾碎后放入足量的盐酸中(假设钙片除碳酸钙之外的成分不与盐酸反应)过滤,取滤液加入足量的(NH4)2C2O4,使Ca2+全部生成CaC2O4沉淀,再过滤出沉淀并洗涤后将其溶解于强酸中,使其全部转化为草酸(H2C2O4),再稀释成1.00L溶液,取出该溶液20.0mL,然后用0.0100mol·L-1酸性KMnO4溶液滴定,恰好完全反应时用去6.00mL酸性KMnO4溶液。滴定时反应的离子方程式为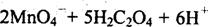
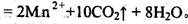
(1)滴定时是否需要指示剂?答: ,理由是
,理由是
(2)试计算每片钙剂中钙元索有多少毫克?

23.(8分)化合物A经李比希法测得其中含c 72.0%、H 6.67%,其余含有氧,质谱法分析得知A的相对分予质量为150。现代仪器分析有机化合物的分子结构有以下两种方法。
方法一:核磁共振仪可以测定有机分子里不同化学环境的氢原子及其相对数量。如乙醇(CH3CH2OH)的核磁共振氢谱有3个峰,其面积之比3:2:1,见下图所示。
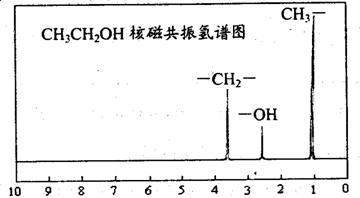
现测出A的核磁共振氢谱有5个峰,其面积之比为1:2:2:2:3。
方法二:利用红外光谱仪可初步检测有机化合物中的某些基团,现测得A分子的红外光谱如下图:

己知。A分子中只含一个苯环,且苯环上只有一个取代基,试填空。
(1)A的分子式为
(2)A的结构简式为
(3)A的芳香类同分异构体有多种,请按要求写出其中两种结构简式:
①分子中不含甲基的芳香酸:
②遇FeCl3显紫色且苯环上只有两个取代基的芳香醛:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com