
题目列表(包括答案和解析)
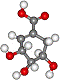
26.医学研究成果显示,从八角茴香中提取到的莽草酸具有抗炎、镇痛作用,是合成某些抗癌药物的中间体。莽草酸的分子结构模型如图所示(分子中只有C、H、O三种原子)。请回答下列问题:
⑴观察右图分子结构模型,写出莽草酸分子中能发生取代反应的官能团的名称________ 。
 ⑵莽草酸跟有机物A在一定条件发生酯化反应,可生成一种相对分子质量为188的酯类物质。A的结构简式为
。
⑵莽草酸跟有机物A在一定条件发生酯化反应,可生成一种相对分子质量为188的酯类物质。A的结构简式为
。
⑶莽草酸在一定条件下可以发生消去反应,能生成一种芳香族化合物,写出该物质的结构简式
。
⑷环状有机物B是莽草酸的同分异构体,1mol该有机物与足量的银氨溶液反应生成4mol金属银;1mol该有机物与足量的金属钠反应生成1.5molH2。试写出符合上述条件的有机物B的结构简式(写一种)
_ 。
25.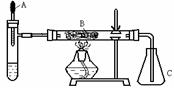 已知多种重金属化合物能催化H2O2的分解。下图是氨的催化氧化的实验装置。试管中加入过量浓氨水并滴入2ml 5%AgNO3溶液;A为胶头滴管,预先吸有25%的H2O2溶液; B中装有铂石棉催化剂。点燃酒精灯一段时间后,将A中的H2O2溶液慢慢地滴入试管,试管内产生大量气体。不久,锥形瓶C内出现红棕色气体。回答下列问题:
已知多种重金属化合物能催化H2O2的分解。下图是氨的催化氧化的实验装置。试管中加入过量浓氨水并滴入2ml 5%AgNO3溶液;A为胶头滴管,预先吸有25%的H2O2溶液; B中装有铂石棉催化剂。点燃酒精灯一段时间后,将A中的H2O2溶液慢慢地滴入试管,试管内产生大量气体。不久,锥形瓶C内出现红棕色气体。回答下列问题:
(1)你认为反应中能催化分解H2O2的物质是(写化学式)
(2)试管中产生的气体是 。
(3)B中发生反应的化学方程式 。
(4)本实验还可以改用其他药品,例如在试管中加固体 ,胶头滴管预先吸入液体 。
(5)除干燥装置外,此实验装置的缺点是还缺少 装置。
24.为比较Fe3+和Cu2+对H2O2分解的催化效果甲乙两组同学分别设计了如图一、图二所示的实验。
⑴图一可通过观察 定性比较得出结论。有同学提出将CuSO4改为CuCl2更为合理,其理由是 ,
你认为还可以作何改进? 。
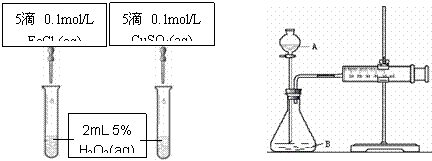
图一 图二
⑵检查图二装置气密性的方法是
图二所示实验中需测量的数据是 。
23.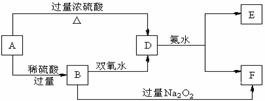 中学化学中几种常见物质的转化关系如下:已知A→D的反应必须加热,否则会发生钝化现象。请回答下列问题:
中学化学中几种常见物质的转化关系如下:已知A→D的反应必须加热,否则会发生钝化现象。请回答下列问题:
(1)B、D、E的化学式依次为 、 、 。
(2)写出B的酸性溶液与双氧水反应的离子方程式:
(3)写出B和过量过氧化钠反应生成F的化学方程式
22.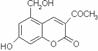 针对齐齐哈尔第二制药有限公司(以下简称齐二药)生产的假药“亮菌甲素注射液”导致多名患者肾功能衰竭一事,药品安全问题引起人们的关注。“亮菌甲素”结构简式如图,是黄色或橙黄色结晶粉末,几乎不溶于水,辅料丙二醇(C3H8O2)溶成针剂用于临床。该药为利胆解痉药,适用于急性胆囊炎、慢性胆囊炎急性发作及慢性浅表性胃炎等。
针对齐齐哈尔第二制药有限公司(以下简称齐二药)生产的假药“亮菌甲素注射液”导致多名患者肾功能衰竭一事,药品安全问题引起人们的关注。“亮菌甲素”结构简式如图,是黄色或橙黄色结晶粉末,几乎不溶于水,辅料丙二醇(C3H8O2)溶成针剂用于临床。该药为利胆解痉药,适用于急性胆囊炎、慢性胆囊炎急性发作及慢性浅表性胃炎等。
(1) 写出“亮菌甲素”的分子式
(2) 1 mol亮菌甲素最多能和 mol H2发生反应,该反应类型是 反应。
(3) 写出“亮菌甲素”和足量NaOH溶液完全反应的化学反应方程式:
21.物质的分离是化学研究中常用的方法,填写下列物质分离时需使用的方法(不必叙述操作细节)。
(1)两种互不相溶的液体的分离 (2)固体和液体的分离
(3)含固体溶质的溶液中除去部分溶剂 (4)胶体中分离出可溶电解质
(5)几种沸点相差较大的互溶液体的分离 。
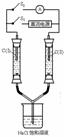
18.( )如右图所示装置,两玻璃管中盛满滴有酚酞溶液的NaCl饱和溶液,C(Ⅰ)、(Ⅱ)为多孔石墨电极。接通S1后,C(Ⅰ)附近溶液变红,两玻璃管中有气体生成。一段时间后(两玻璃管中液面未脱离电极),断开S1,接通S2,电流表的指针发生偏转,说明此时该装置形成了原电池,关于该原电池的叙述正确的是
A. C(I)的电极名称是阴极 B.C(II)的电极名称是负极
C.C(I)的电极反应式是2H++2e-=H2↑ D.C(II)的电极反应式是Cl2+2e-=2Cl-.
 ( )19.在室温下,某溶液中由H2O H++OH-这一途径产生出H+和OH-浓度的乘积为1×10-26,则此溶液中可能大量共存的离子组为
( )19.在室温下,某溶液中由H2O H++OH-这一途径产生出H+和OH-浓度的乘积为1×10-26,则此溶液中可能大量共存的离子组为
A.HCO3-、Al3+、H+、SO42- B.SiO32-、ClO-、Na+、K+
C.Cu2+、Cl-、NO3-、K+
D.I-、Fe3+、SCN-、NH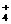
 (
)20.随着信息技术的迅猛发展,计算机在化学化工领域得到了广泛应用。下面四幅图是用计算机制作的在密闭容器里,在不同条件下进行反应:X(g) Y(g)达到平衡的图解。图中的“●”是X,“○”是Y。
(
)20.随着信息技术的迅猛发展,计算机在化学化工领域得到了广泛应用。下面四幅图是用计算机制作的在密闭容器里,在不同条件下进行反应:X(g) Y(g)达到平衡的图解。图中的“●”是X,“○”是Y。


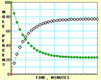

图Ⅰ 图Ⅱ图Ⅲ图Ⅳ
下列有关说法正确的是
A.图中的纵坐标表示物质的物质的量分数
B.四幅图中,图Ⅲ所示反应达到平衡时,X的转化率为60%
C.图Ⅰ和图Ⅱ所采用的不同条件是反应体系压强不同D.图Ⅳ说明反应开始时是向正反应方向进行的
17.( )某研究小组研究了其他条件不变时,改变条件对以下可逆反应的影响:
2SO2(g)+O2(g) 2SO3(g);△H<0下列说法正确的是
2SO3(g);△H<0下列说法正确的是
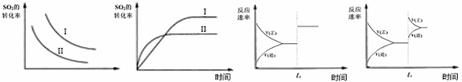
图一 图二 图三 图四
A.图一研究的是温度、压强对平衡的影响,横坐标表示压强
B.图二研究的是温度对平衡的影响,Ⅱ采用的温度更高
 C.图三中t0时使用了催化剂,使平衡向正反应方向进行
C.图三中t0时使用了催化剂,使平衡向正反应方向进行
D.图四中t0时增大压强,使平衡向逆反应方向进行
16.( )下列溶液中有关微粒的物质的量浓度关系正确的是
A.NaHSO3和NaHCO3的中性混合溶液中(S和C均用R表示):c(Na+)=c(HRO3-)+c(RO32-)
B.常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后溶液中:c(Na+)>c(Cl-)>c(CH3COOH)
C.常温下物质的量浓度相等的①(NH4)2CO3、②(NH4)2SO4、③NH4HSO4三种溶液中c(NH4+):①<②<③
D.相同条件下,pH=5的 ①NH4Cl溶液、②CH3COOH溶液、③稀盐酸溶液中由水电离出的c(H+):①>②>③
14.( )对室温下pH相同、体积相同的氨水和氢氧化钠溶液分别采取下列措施,有关叙述正确的是
A.加入适量的氯化铵晶体后,两溶液的pH均减小 B.温度下降10℃,两溶液的pH均不变
C.分别加水稀释10倍,两溶液的pH仍相等 D.用同浓度的盐酸中和,消耗的盐酸体积相同
 ( )15.一定条件下,电解较稀浓度的硫酸,其还原产物为双氧水,该原理可用于制取双氧水,其电解的化学方程式为:3H2O+3O2 O3+3H2O2。下列有关说法正确的是
( )15.一定条件下,电解较稀浓度的硫酸,其还原产物为双氧水,该原理可用于制取双氧水,其电解的化学方程式为:3H2O+3O2 O3+3H2O2。下列有关说法正确的是
A.电解池的阳极生成双氧水,阴极生成臭氧 B.电解池中硫酸溶液的pH保持不变
C.产生臭氧的电极反应式为3H2O-6e-=O3+6H+
D.产生双氧水的电极反应式为2H2O-2e-= H2O2+2H+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com