
题目列表(包括答案和解析)
20.( )下列各叙述中正确的是 ①元素的相对原子质量是该元素的原子质量与碳原子质量的比值;②质子数相同的微粒均属于同一种元素;③分子是保持物质性质的一种微粒;④原子是物质变化中的最小微粒;⑤同一种元素组成的物质是纯净物;⑥原电池是把化学能转变为电能的装置;⑦有新单质生成的化学反应通常是氧化还原反应
A.都不正确 B.只有①②⑤⑥⑦正确 C.只有①②③④⑤正确 D.只有⑥⑦正确
18.( ) 目前,人类已经发现的非金属元素除稀有气体元素外共16种,下列对16种非金属元素的表述正确的有:①都是主族元素,最外层电子数都大于3 ②单质形成的晶体都为分子晶体 ③氢化物常温下都是气态,所以又叫气态氢化物 ④氧化物常温下都可以与水反应生成酸
A.只有①②正确 B.只有①③正确 C.只有③④正确 D.①-④都不正确
 ( )19.用下图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U型管的质量差,实验测得m(H):m(O)>1:8。下列对导致这一结果的原因的分析中,一定错误的是
( )19.用下图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U型管的质量差,实验测得m(H):m(O)>1:8。下列对导致这一结果的原因的分析中,一定错误的是
A.I、Ⅱ装置之间缺少干燥装置 B.CuO没有全部被还原
C.Ⅱ装置中玻璃管内有水冷凝 D.Ⅲ装置后缺少干燥装置
17.( )24mL H2S在30mL O2中燃烧,在同温同压下得到SO2的体积为
A.24mL B.30mL C.20mL D.18mL
16.( )若pH = 3的酸溶液和pH = 11的碱溶液等体积混合后,溶液呈酸性,其原因可能是
A.生成了一种强碱弱酸盐 B.弱酸溶液和强碱溶液反应
|
14.( )Cl2、SO2均能使品红溶液褪色。后者因为品红分子结构中的发色团遇到亚硫酸后结构发生改变,生成不稳定的无色化合物。其漂白原理可用下面的反应方程式表示:
 下列说法正确的是
下列说法正确的是
A. 品红溶液中同时通入Cl2、SO2,漂白效果会更好 B.加热不能判断品红褪色是通入SO2还是通入Cl2引起的
C.上述可逆反应中,正反应的△H>0 D.品红分子结构中,19个碳原子都可能在同一平面上
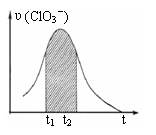 ( )15.KClO3和KHSO3能发生反应:ClO3-+HSO3-→SO42-+ Cl-+ H+(未配平)。已知该反应的速率随c(H+)的增大而加快。右图为用ClO3-在单位时间内物质的量浓度变化表示的该反应υ-t图。下列说法正确的
( )15.KClO3和KHSO3能发生反应:ClO3-+HSO3-→SO42-+ Cl-+ H+(未配平)。已知该反应的速率随c(H+)的增大而加快。右图为用ClO3-在单位时间内物质的量浓度变化表示的该反应υ-t图。下列说法正确的
A.反应开始时速率增大不可能是c(H+)所致
B.纵坐标为υ(Cl-)的υ-t曲线与图中曲线不能完全重合
C.后期速率υ下降的主要原因是反应向逆反应方向进行
D.图中阴影“面积”可以表示t1-t2时间内c(Cl-)增大
13.( )下列离子方程式正确的是:
A.向NH4HSO4的稀溶液中逐滴加入Ba(OH)2溶液至刚好沉淀完全:NH4+ + H+ + SO42- + Ba2+ + 2OH- = NH3·H2O + BaSO4↓+ 2H2O
B.少量硝酸银溶液滴入稀氨水中:Ag+ + 2NH3·H2O ==Ag(NH3)2+ + 2H2O
C.向碳酸氢钙溶液中滴入少量澄清石灰水:Ca2+ + 2HCO3- + 2OH- = CaCO3 + 2H2O + CO32-
D. 向次氯酸钠溶液中通入少量的二氧化硫气体:3ClO-+H2O+SO2=2HClO+SO42-+Cl-
12.( )已知:2Fe2++Br2===2Fe3++2Br-。在100mL FeBr2溶液中通入标准状况下3.36LCl2,Cl2全部被还原,测得溶液中c(Br-)= c(Cl-),则原FeBr2溶液的物质的量浓度是
A.0.75 mol/L B.1.5 mol/L 或2 mol/L C.4 mol/L D.3 mol/L
11.( )醋酸钡[(CH3COO)2Ba·H2O]是一种媒染剂,有关0.1mol/L醋酸钡溶液中粒子浓度比较不正确的是
A.c(Ba2+) >c(CH3COO-)>c(OH-)>c(H+)
B.c(H+)+2c(Ba2+)= c(CH3COO-)+c(OH-)
C.c(H+) = c(OH-)-c(CH3COOH) D.2c(Ba2+)= c(CH3COO-)+ c(CH3COOH)
10.( )在氯水中存在多种分子和离子,它们在不同的反应中表现各自的性质。下列实验现象和结论一致且正确的是
A.加入有色布条,一会儿有色布条褪色,说明溶液中有Cl2存在
B.溶液呈黄绿色,且有刺激性气味,说明有Cl2分子存在
C.先加入盐酸酸化,再加入AgNO3溶液产生白色沉淀,说明有Cl-存在
D.加入NaOH溶液,氯水黄绿色消失,说明有HClO分子存在
9.( )下列离子在溶液中能大量共存,加入(NH4)2Fe(SO4)2·6H2O晶体后,仍能大量共存的是
A.Na+ H+ Cl- NO3- B.K+ Ba+ OH- I- C.Na+ Mg2+ Cl- SO42- D.Cu2+ S2- Br- ClO-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com