
题目列表(包括答案和解析)
24.用实验确定某酸HB的弱电解质。两同学的方案是:
甲:①称取一定质量的HB配制0.1mol/L的溶液100mL;
②用pH试纸测出该溶液的pH值,即可证明HB是弱电解质。
乙:①用已知物质的量浓度的HB溶液、盐酸,分别配制pH = 1的两种酸溶液各100mL;
②分别取这两种溶液各10mL,加水稀释为100mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HB是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是
(2)甲方案中,说明HB是弱电解质的理由是测得溶液的pH 1(选填>、<、=)
乙方案中,说明HB是弱电解质的现象是
A.HCl溶液的试管中放出H2的速率快; B.装HB溶液的试管中放出H2的速率快;
C.两个试管中产生气体速率一样快。
(3)请你评价:乙方案中两个难以实现之处
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表达
23.用于分离或提纯物质的方法有:A.蒸馏(分馏) B.盐析C.过滤 D.重结晶 E.升华 F.渗析 G.加热分解 。下列各组混合物的分离或提纯应选用上述哪一种方法最合适?(把选用的方法的标号填入括号内) (1)除去Ca(OH)2溶液中悬浮的CaCO3微粒( ) (2)除去Fe(OH)3胶体中混有的Cl-离子( ) (3)除去乙醇中的少量水( ) (4)除去氧化钙中的碳酸钙( )(5)除去固体碘中混有的砂子 ( )
22.将pH值为8的NaOH溶液与pH值为10的 NaOH溶液等体积混和后,溶液中的氢离子浓度(mol·L-1)最接近于
A.1/2(10-8+10-10) B.(10-8+10-10) C.(1×10-14-5×10-5) D.2×10-10
21.一元酸HA溶液中,加入一定量强碱MOH溶液后,恰好完全反应,反应后的溶液中,下列判断正确的是
A.c(A-)≥c(M+) B.c(A-)≤c(M+)
C.若MA不水解,则c(OH-)<c(H+) D.若MA水解,则c(OH-)≥c(H+)
20.将相同物质的量浓度的某弱酸HX溶液与NaX溶液等体积混合,测得混合溶液中c(Na+)>c(X-),则下列关系错误的是
A.c(OH-)>c(H+) B.c(HX)<c(X-)
C.c(X-)+c(HX)==2c(Na+) D.c(HX)+c(H+)==c(Na+)+c(OH-)
19.将pH=3的盐酸溶液和pH=11的氨水等体积混合后,溶液中离子浓度关系正确的是
A.c(NH4+)>c(Cl-)>c(H+)>c(OH-) B.c(NH4+)>c(Cl-)> c(OH-)>c(H+)
C.c(Cl-)>c(NH4+)>c(H+)>c(OH-) D.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
18.下面二维平面晶体所表示的化学式为AX3的是
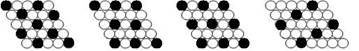
A. B. C. D.
17.磁流体是电子材料的新秀,它既具有同体的磁性,又具有液体的流动性。制备时将含等物质的量的FeSO4和Fe2(SO4)3的溶液混合,再滴入稍过量的氢氧化钠溶液,随后加入油酸钠溶液,即可生成黑色的、分散质粒子的直径在5.5nm-36nm的磁流体。下列说法中正确的是
A.所得的分散系属于悬浊液 B.所得的分散系中的分散质为Fe2O3
C.给分散系通电时阳极周围黑色加深 D.该分散系能产生丁达尔效应
16.某研究性学习小组为了探索镁粉与FeCl3溶液的反应机理,做了如下两组实验:①将镁粉投入冷水中,未见明显现象;②将镁粉投入FeCl3y溶液中,观察到有气泡产生,溶液颜色逐渐变浅,同时逐渐产生红褐色沉淀。则下列有关镁与FeCl3溶液反应的叙述中,正确的是
A.镁只与FeCl3溶液中的Fe3+直接反应 B.气泡是镁与FeCl3溶液中的水直接反应产生的
C.红褐色沉淀是镁与水反应生成的Mg(OH)2与Fe3+反应所得
D.气泡是镁与FeCl3水解生成的盐酸反应产生的
15.硫代硫酸钠可作为脱氯剂,已知25.0mL0.100mol·L-1Na2S2O3溶液恰好把224mL(标准状况下)Cl2完全转化为Cl-离子,则S2O32-将转化成
A.S2- B.S C.SO32- D.SO42-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com