
题目列表(包括答案和解析)
26. (16分) A-M有如下图转化关系。已知D、L是相对分子质量相等的两种气体,且含有同一种元素,D是石油化工的重要基础原料,也是一种植物生长调节剂;A、E都是无色溶液,B是无色气体单质,反应②、③、④都是工业生产中的重要反应,H与J反应生成的溶液遇苯酚显紫色。(有些反应条件已省略)
(16分) A-M有如下图转化关系。已知D、L是相对分子质量相等的两种气体,且含有同一种元素,D是石油化工的重要基础原料,也是一种植物生长调节剂;A、E都是无色溶液,B是无色气体单质,反应②、③、④都是工业生产中的重要反应,H与J反应生成的溶液遇苯酚显紫色。(有些反应条件已省略)
(1) C的化学式_____________,D的电子式_____________。
(2)上述框图中的物质能使溴水褪色的气体是_________________(写化学式)
(3)反应①的化学方程式___________________________________________________
(4) H与J的稀溶液反应的离子方程式_________________________________________
(5) 已知生成1 mol I放出98.3 kJ的热量。写出反应③的热化学方程式 ,工业上进行这一反应的设备是 反应的适宜条件为 。
13.在密闭容器中,对于可逆反应A +3B  2C(气),平衡时C的体积分数
2C(气),平衡时C的体积分数
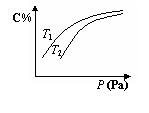
与温度和压强的关系如图所示,下列判断不正确的是 ( )
A.若正反应方向△H >0,则T1 > T 2
B.压强增大时,混合气体的平均相对分子质量增大
C.A可能为气体
D.B不一定为气体
选择题答题栏
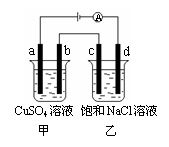
12.如图所示,a、b、c、d均为石墨电极,通电进行电解。下列说法错误的是( )
A.乙烧杯中c极的电极反应为 2Cl––2e– ══ Cl2↑
B.a、c两极产生气体的物质的量不相等
C.甲、乙两烧杯中溶液的pH均保持不变
D.甲烧杯中发生的反应为
 2CuSO4 + 2H2O
电 解 2Cu + O2 ↑ + 2 H2SO4
2CuSO4 + 2H2O
电 解 2Cu + O2 ↑ + 2 H2SO4
11.化学用语是学习化学的重要工具。下列用来表示物质变化的化学用语中,正确的是 ( )
A.钢铁腐蚀时可能发生的正极反应 4OH– – 4e– ══ 2H2O + O2↑
B.表示中和热的离子方程式 H+ + OH–══ H2O; △H=–57.3 kJ/ mol
C.明矾水解反应的离子方程式 Al3+ + 3H2O══Al(OH)3 + 3H+
 D.硫酸铵浓溶液与氢氧化钠浓溶液混合的离子方程式 NH4+
+ OH– ══ NH3↑+ H2O
D.硫酸铵浓溶液与氢氧化钠浓溶液混合的离子方程式 NH4+
+ OH– ══ NH3↑+ H2O
10.下列叙述正确的是 ( )
A.同周期元素的原子半径越小,气态氢化物还原性越弱
B.晶体中分子间作用力越强,分子越稳定
C.稀有气体原子序数越大,熔点越低
D.同主族金属的原子半径越大,熔点越高
9.以下有关溶液(均在常温下)的结论不正确的是 ( )
A. pH>7的溶液中可能存在CH3COOH分子
B.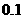 mol / L醋酸溶液100
mL与50
mL
mol / L醋酸溶液100
mL与50
mL  mol / L氨水混合后能恰好完全中和
mol / L氨水混合后能恰好完全中和
C.pH =1的盐酸与pH =5的盐酸等体积混合后pH等于3
D.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量后者多
8.用NA表示阿伏加德罗常数,下列说法正确的是 ( )
A.0.2 mol过氧化氢完全分解转移的电子数目为0.4NA
B.300 mL 2 mol / L蔗糖溶液中所含分子数为0.6 NA
C.在常温常压下,17 g硫化氢所含质子数目为8 NA
D.在标准状况下,2.24 L二氧化硫与氧气混合气体中所含氧原子数为0.2 NA
7.下列各组物质中,能发生不同化学反应的是 ( )
①C与O2 ② P与Cl2 ③Fe与Cl2 ④ NaAlO2 溶液与H2SO4 溶液
⑤CO2与NaOH溶液 ⑥Cu与硝酸 ⑦ AgNO3溶液与氨水 ⑧AlCl3溶液与氨水
A.除③外 B.除③⑧外 C.除③⑦外 D.除⑥⑦⑧外
6.保护环境是公民的责任和义务。下列说法正确的是 ( )
A.大量使用含磷洗涤剂会带来白色污染
B.减少使用氟氯代烷的目的是为了减少酸雨
C.硫酸厂的尾气用氨水吸收,生产中的污水含有硫酸等杂质可用烧碱中和处理
D.北京城区限制冬季燃煤供暖,是因为燃烧化石燃料会产生二氧化硫
28.(18分)2005年的诺贝尔化学奖颁给了3位在烯烃复分解反应研究方面做出突出贡献的化学家。烯烃复分解反应实际上是在金属烯烃络合物的催化下实现C=C双键两边基团换位的反应。如下图表示了两个丙烯分子进行烯烃换位,生成两个新的烯烃分子--丁烯和乙烯。

现以石油裂解得到的丙烯为原料,经过下列反应可以分别合成重要的化工原料I和G。I和G在不同条件下反应可生成多种化工产品,如环酯J。
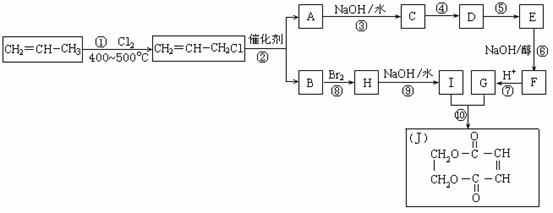 请按要求填空:
请按要求填空:
⑴写出下列反应的反应类型:
①:______________,⑥:______________,⑧:______________。
⑵反应②的化学方程式是___________________________________________。
⑶反应④、⑤中有一反应是与HCl加成,该反应是________(填反应编号),设计这一步反应的目的是_________________________________________,物质E的结构简式是_______________ ________。
⑷反应⑩的化学方程式是___________________________________________。
⑸C的同分异构体很多,写出满足下列条件的同分异构体的结构简式:①含有酯基 ②能发生银镜反应:
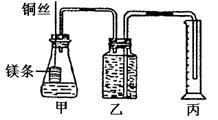 29.(18分)某课外学习小组设计如下的简易实验装置,证明在相同条件下,体积相同、物质的量浓度相同的两种强弱不同的一元酸与足量镁带反应时,生成氢气的体积相同而反应速率不同,同时测定实验条件下的气体摩尔体积。请回答下列问题:
29.(18分)某课外学习小组设计如下的简易实验装置,证明在相同条件下,体积相同、物质的量浓度相同的两种强弱不同的一元酸与足量镁带反应时,生成氢气的体积相同而反应速率不同,同时测定实验条件下的气体摩尔体积。请回答下列问题:
(1)请将该实验的主要操作步骤补充完全:
①配制浓度均为1mol·L-1的盐酸和醋酸溶液;
②用 量取10.00mL 1mol·L-1盐酸和醋酸分别加入两个锥形瓶中;
③分别称取除去表面氧化膜的镁带ag,并系于铜丝末端,a的数值要大于 。
④在广口瓶中装足量的水,按图连接好装置并检查装置的气密性。
⑤将铜丝向下移动,使足量镁带浸入酸中(铜丝不与酸接触),至反应完全,记录
和反应后量筒中水的体积。
⑥反应结束后待温度恢复到室温,读出量筒中水的体积为VmL。(包括导管里的水)
(2)本实验中应选用 (填序号)的量筒。
A.100mL B.200mL C.500mL
(3)若水蒸气的影响忽略不计,在实验室条件下,气体摩尔体积的计算式为:
Vm= L·mol-1
(4)简述速率不等的原因
(5)写出醋酸和镁带反应的离子方程式:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com