
题目列表(包括答案和解析)
4、用NA表示阿伏加德罗常数,下列说法错误的是:( )
A.1mol C20H42分子中共含61NA个共价键
B.25℃时,1mL纯水中含有10-10NA个OH-离子
C.含4mol Si-O键的石英晶体中,氧原子为2NA个
D.当NO2溶于水产生1molNO时,反应转移的电子数为NA。
3、下列制绿矾的方法最适宜的是:
A.铁屑与稀硫酸 B.FeO与稀硫酸
C.Fe(OH)3与稀硫酸 D.Fe2(SO4)3与铜粉。
2、周期表中有些元素有隔类相似现象(即对角线相似),如Mg、Li; Si、B ;Al、Be等性质相似。现电解熔融LiCl可得Li和Cl2。若用已潮解的LiCl加热蒸干并强热至熔融,再用惰性电极电解,结果得到金属锂,还有一种无色无气味的气体,其主要理由是:
A.电解出的锂与水反应放出H2
B.电解前LiCl加热时已发生水解,电解时产生H2
C.电解时产生的无色气体是O2
D.在高温时阳极放出的Cl2与水作用会放出O2。
1、生活离不开化学,下列有关说法正确的是( )
A.乙醇和汽油都是可再生能源.应大力推广使用“乙醇汽油”
B.太阳能电池可采用硅材料制作,其应用有利于环保、节能
C.棉花、蚕丝和人造丝的主要成分都是纤维素
D.凡含有食品添加剂的食物对人体健康均有害,不宜食用
29.
(14分)( 德州市) 已知:有机物D( )是组成人体蛋白质的氨基酸之一,它可由A通过以上反应合成制取。有机物A(
)是组成人体蛋白质的氨基酸之一,它可由A通过以上反应合成制取。有机物A( )为食品包装中的常用防腐剂,常温下难溶于水, 可以使溴水褪色。有机物B(
)为食品包装中的常用防腐剂,常温下难溶于水, 可以使溴水褪色。有机物B( ),其分子中没有支链,通常状况下为无色晶体,能与氢氧化钠溶液发生反应。
),其分子中没有支链,通常状况下为无色晶体,能与氢氧化钠溶液发生反应。
请回答下列问题: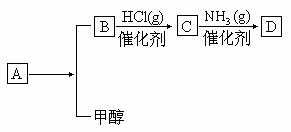
(1)B、D的结构简式分别是__________、__________。
(2)A可以发生的反应有__________(选填序号)
①加成反应 ②氧化反应 ③酯化反应 ④加聚反应
(3)B分子中所含的官能团名称是______________________________。
(4)B的具有相同官能团的同分异构体的结构简式是____________________。
(5)写出由B与甲醇反应制A的化学方程式是____________________。
28. ( 德州市)(22分)为了从含有 的废液中回收Cu,某研究性学习小组的同学们设计了两种方案:回答下列问题:
的废液中回收Cu,某研究性学习小组的同学们设计了两种方案:回答下列问题:
(1)根据实验方案的内容和步骤补全下述实验方案中的①②③。
方案1:向废液中加入过量的铁粉,充分反应后,①__________。在所得滤渣中加入足量的②__________,
充分反应后,再过滤即得到铜。
方案2:在废液中加入适量的盐酸调节溶液的pH=1,用铜和石墨作电极进行电解。当观察到③_______________时,即停止电解,这时要回收的Cu已全部析出。
(2)方案1中涉及的四种阳离子的氧化性由强到弱的顺序为:____________________过滤操作时,需要用到的玻璃仪器是:____________________。
(3)方案2中铜作__________极,所发生的电极反应为(若有多个电极反应,请按照反应发生的先后顺序全部写出)_________________________________,另一电极所发生的电极反应为_________________________________。
(4)方案2在电极上直接回收铜,操作上比方案1简便,但方案2也有不足之处,主要表现为:__________________________________________________。
27. ( 德州市)(10分)已知A为常见金属,X、Y为常见非金属,X、E、F、G常温下为气体,C为液体,B是一种盐,受热易分解,在工农业生产中用途较广(如被用作某些电池的电解质)。现用A与石墨作电极,B的浓溶液作电解质,构成原电池。有关物质之间的转化关系如下图:(注意:其中有些反应的条件及部分生成物已略去)

请填写下列空白:
(1)反应④为A在某种气体中燃烧,生成单质Y和A的氧化物,其反应方程式为________________________________________。
(2)反应②的化学方程式为________________________________
(3)反应⑤的化学方程式为________________________________
(4)原电池反应①中正极的电极反应式为________________________
(5)B溶液在工业上常被用作焊接时的除锈剂,其应用原理是___________________________________________。
26. ( 德州市)(14分)(1)20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成,而是在反应物到生成物的过程中经过一个高能量的过渡态。图甲是白磷( )和
)和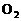 反应生成
反应生成 过程中能量变化示意图,请写出白磷(
过程中能量变化示意图,请写出白磷( )和
)和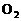 反应生成
反应生成 的热化学方程式:
的热化学方程式:
_(△H用含 和
和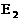 的代数式表示,其中E1、E2均大于0)。
的代数式表示,其中E1、E2均大于0)。

(2)常温下取0.2mol/L HCl溶液与0.2mol/L MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答以下问题:
①混合溶液中由水电离出的 ________0.2mol/L HCl溶液中由水电离出
________0.2mol/L HCl溶液中由水电离出 ;(填“>”、“<”或“=”)
;(填“>”、“<”或“=”)
②求出混合物中下列算式的精确计算结果。
 =________mol/L,
=________mol/L, =________mol/L。
=________mol/L。
③如果常温下取0.2mol/L MOH溶液与0.1mol/L HCl溶液等体积混合,测得混合溶液的pH<7,则说明MOH的电离程度________MCl的水解程度。(填“>”、“<”或“=”)
12.(滨州市)X、Y、Z为短周期元素,X原子最外层只有一个电子,Y原子的最外层电子数比内层电子数少4,Z的最外层电子数是内层电子总数的3倍。下列有关叙述正确的是 ( )
A.X肯定为碱金属元素 B.稳定性:Y的氢化物>Z的氢化物
|
|
 13.(崇文区一模)利用下列各组中的物质制备并收集少量相应的气体,能采用右图装置的是 ( )
13.(崇文区一模)利用下列各组中的物质制备并收集少量相应的气体,能采用右图装置的是 ( )
①浓氨水和固体NaOH制NH3 ②大理石和稀盐酸制CO2
③过氧化氢溶液和二氧化锰制O2 ④稀硝酸和铜片制NO
⑤浓盐酸和二氧化锰制Cl2 ⑥电石和水制C2H2
⑦锌粒和稀硫酸制H2 ⑧乙醇和浓硫酸制C2H4
A.②③ B.①⑥⑦
C.②⑤⑧ D.①④⑥
选择题答题栏
11.(滨州市)据悉,奥运会上使用的发令枪所用的“火药”成分是氯酸钾和红磷,经撞击发出响声,同时产生白色烟雾。撞击时发生的化学反应方程式为:5KclO3+6P=3P2O5+5KCl,则下列有关叙述错误的是 ( )
A.上述反应中氧化剂和还原剂的物质的量之比为5:6
B.产生白色烟雾的原因是生成的P2O5白色固体小颗粒(烟)吸水性很强,吸收空气中 的水分,
生成磷酸小液滴(雾)
C.上述反应中消耗3molP时,转移电子的物质的量为15mol
D.因红磷和白磷互为同分异构体,所以上述火药中的红磷可以用白磷代替
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com