
题目列表(包括答案和解析)
16. 某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量):

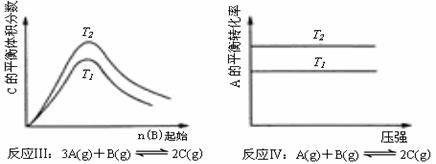
根据以上规律判断,下列结论正确的是
A.反应Ⅰ:△H>0,P2>P1
B.反应Ⅱ:△H<0,T1>T2
C.反应Ⅲ:△H>0,T2>T1;或△H<0,T2<T1
D.反应Ⅳ:△H<0,T2>T1
第Ⅱ卷(非选择题共86分)
15. 电动车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为:
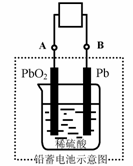 Pb+PbO2+4H++2SO42-
Pb+PbO2+4H++2SO42- 2PbSO4+2H2O,
2PbSO4+2H2O,
则下列说法正确的是:
A.放电时:电子流动方向由B到A
B.放电时:正极反应是Pb-2e-+SO42- PbSO4
PbSO4
C.充电时:铅蓄电池的负极应与充电器电源的正极相连
D.充电时:阳极反应是
PbSO4-2e-+2H2O PbO2+SO42-+4H+
PbO2+SO42-+4H+
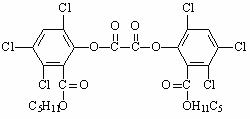
14. 近年来无锡建设了多个市民广场,为市民提供了夏夜纳凉的好去处,夜色中常看到小朋友手持被称为“魔棒”的荧光棒玩耍,“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式如右图所示:
下列有关说法正确的是
A.草酸二酯属于芳香族化合物 B.草酸二酯属于高分子化合物
C.1mol草酸二酯与氢氧化钠稀溶液反应(苯环上卤素不水解),最多消耗4mol NaOH
D.1mol草酸二酯与氢气完全反应,需要氢气10mol
13. 下列叙述正确的是
A.0.01mol/LCH3COOH与pH=12的NaOH溶液混合,若有c(CH3COO-)>c(Na+),则混合液
一定呈碱性
B.常温下,将等体积0.01mol/LHCl与pH=12的氨水混合,则混合液的pH=7,
C.0.1mol/L的某二元弱酸盐Na2A溶液中,c(Na+)=2c(H2A)+2c(HA-)+2c(A2-)
D.将5 mL 0.02mol/L的H2SO4与5 mL 0.02mol/LNaOH溶液充分混合,若混合后溶液的体
积为10mL,则混合液的pH=2
12. 下列反应的离子方程式书写正确的是
A.等体积等物质的量浓度的氢氧化钡溶液与明矾溶液混合:
Ba2++3OH-+Al3++ SO42- BaSO4↓+Al(OH)3↓
BaSO4↓+Al(OH)3↓
B.向苯酚钠溶液中通人少量CO2:C6H5O-+CO2+H2O→C6H5OH+HCO3-
C.Fe3O4与稀硝酸反应:Fe3O4+8H+ Fe2++2Fe3++4H2O
Fe2++2Fe3++4H2O
D.向沸水中滴人适量的饱和氧化铁溶液;Fe 3++3H2O Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
11. X、Y、Z、W为四种短周期主族元素。其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6。下列说法正确的是
A.Y元素最高价氧化物对应水化物的化学式为H2YO4
B.X与W可以形成W2X、W2X2两种化合物
C.W2X的沸点比W2Z的沸点高
D.Y、Z两元素的气态氢化物中,Z的气态氢化物较稳定
10. 某结晶水合物的化学式为A·H2O,其相对分子质量为B,在60℃时m g 该晶体溶于ng
水中,得到V mL 密度为d g· mL-1 的饱和溶液,下述表达式或判断正确的是
A.该溶液物质的量浓度为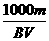 mol·L-1
mol·L-1
B.60℃时A的溶解度为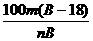 g
g
C. 该溶液溶质的质量分数为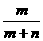 ×100%
×100%
D.60℃时,将10g A 投入到该饱和溶液中,析出晶体大于l0g
9. 下列各组离子能大量共存,当溶液中c(H+)=10-1mol/L时,有气体产生;而当溶液中c(H+)=10-13mol/L时,又能生成沉淀。试组离子可能是
A.Na+、Cu2+、NO3-、CO32- B.Ba2+、K+、Cl-、HCO3-
C.Fe2+、Na+、SO42-、NO3- D.Mg2+、NH4+、SO42-、Cl-
8. 下列关于晶体的说法一定正确的是
A.含有共价键的晶体不一定是分子晶体,而分子晶体中一定含有共价键
B.金属晶体的熔点都比分子晶体的熔点高
C.SiO2晶体中每个硅原子与两个氧原子以共价键相结合
D.离子晶体中可能含有共价键,而分子晶体中不可能含有离子键
7. 设NA为阿伏加德罗常数的值,下列叙述中正确的是
A.35.5g超氧化钾(KO2)所含的阴离子中电子数为8NA
B.标准状况下,11.2L氯仿中含有的C-Cl键的数目为1.5NA
C.常温常压下,92gNO2和N2O4混合气体中含有的原子数为6NA
D.工业上铜的电解精炼时电解池中每转移1mol电子时阳极上溶解的铜原子数为0.5 NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com