
题目列表(包括答案和解析)
2.区分清楚萃取和分液的原理、仪器、操作以及适用范围与其他物质分离方法不同。
萃取和分液是物质分离的众多方法之一。每一种方法适用于一定的前提。分液适用于分离互不相溶的两种液体,而萃取是根据一种溶质在两种互不相溶的溶剂中溶解性有很大差异从而达到提取的目的。一般萃取和分液结合使用。其中萃取剂的合理选择、分液漏斗的正确使用、与过滤或蒸馏等分离方法的明确区分等是此类命题的重点和解决问题的关键。
命题以选择何种合适的萃取剂、萃取后呈何现象、上下层如何分离等形式出现。解题关键是抓住适宜萃取剂的条件、液体是否分层及分层后上下层位置的决定因素。分液操作时注意“先下后上、下流上倒”的顺序。为确保液体顺利流出,一定要打开上部塞子或使瓶塞与瓶颈处的小孔或小槽对齐,与大气相通。
[典型例题评析]
例1 氯化碘(ICl)的化学性质跟氯气相似,预计它跟水反应的生成物是(1998年全国高考题)
A.HI和HClO B.HCl和HIO C.HClO3和HIO D.HClO和HIO
思路分析:题目以考生未学过的卤素互化物为素材,让考生对不同卤素的非金属性相对强弱作出判断。这种判断是以卤素跟氢、氧相互结合以及形成正负化合价的能力来实现的。
先联想Cl2+H2O=HCl+HClO,推断ICl与H2O反应有两种可能:ICl+H2O=HI+HClO,ICl+H2O=HCl+HIO。问题是I、Cl两元素何者形成氢卤酸,何者形成次卤酸。与I相比,氯的非金属性比碘强,更易形成负化合价;与Cl相比,I的金属性较强,较易形成正化合价,即产物不能是HI和HClO。
答案:B
方法要领:学习元素化合物知识时,抓住代表物的性质,并结合元素周期律知识,来指导同主族元素性质的学习。在ICl中I为+1价,Cl为-1价与水反应后其产物的化合价均不发生改变,防止受Cl2+H2O=HCl+HClO影响,认为ICl与H2O反应也是氧化还原反应,而误选A。
无机信息题在考卷中经常出现,在做这类题目时,必须对信息理解透彻,活学活用,这样才能保证答题的准确性。
水解产物的判断可根据电荷相互吸收的原则去思考,因化学作用也是电性作用。此类化学方程式可按下列“模式”书写:
A+B-+H+-OH-=A+OH-+H+B-
除ICl外,Mg3N2、CaC2、NaH、Al2S3、CH3COONa等水解均遵循该“规律”。
例2 下列物质在空气中久置变质,在变质过程中,既有氧化还原反应发生,又有非氧化还原反应发生的是(1997年高考化学试测题)
A.食盐 B.漂白粉 C.氯水 D.硫酸亚铁溶液
思路分析:食盐在空气中不变质;漂白粉在空气中发生如下反应:Ca(ClO)2+CO2+H2O=2HClO
+CaCO3↓、2HClO 2HCl+O2↑;氯水中只是2HClO
2HCl+O2↑;氯水中只是2HClO 2HCl+O2↑;硫酸亚铁溶液中只是Fe2+被氧化为Fe3+。
2HCl+O2↑;硫酸亚铁溶液中只是Fe2+被氧化为Fe3+。
答案:B
方法要领:掌握各种物质的化学性质及反应中元素的价态变化。
例3 将1体积选项中的一种气体与10体积O2混合后,依次通过盛有足量浓NaOH溶液的洗气瓶和盛有足量的热铜屑的管子(假设反应都进行完全),最后得到的尾气可以是(1996年全国高考题)
A.Cl2 B.CO C.CO2 D.N2
思路分析:假如“1体积为A中Cl2,则当通过足量浓碱液时,因Cl2+2NaOH=NaCl+NaClO+H2O而被完全吸收,而10体积O2在通过铜屑时被完全吸收,故无尾气产生;若为B中CO,则在通过碱液时无变化;而通过铜屑时,因O2过量而生成CO2故选C;若分别为C中CO2或D中N2,当依次通过时C中无气体剩余,D中仍然保留了原来的N2。
答案:C、D
方法要领:该题要答正确,必须审明题意:即反应物需从四个选项中选,产物也要从四个选项中选。防止漏选C。
例4 为实现中国2000年消除碘缺乏病的目标,卫生部规定食盐必须加碘,,其中的碘以碘酸钾(KIO3)形式存在。已知在溶液中IO3-可和I-发生反应:IO3-+5I-+6H+=3I2+2H2O。根据此反应,可用试纸和一些生活中常见的物质进行实验,证明在食盐中存在IO3-。可供选用的物质有:①自来水;②蓝色石蕊试纸;③碘化钾淀粉试纸;④淀粉;⑤食糖;⑥食醋;⑦白酒。进行上述实验时必须使用的物质是(1997年全国高考题)
A.①③ B.③⑥ C.②④⑥ D.①②④⑤⑦
思路分析:依题给信息要检验NaCl中含有IO3-,宜使其变成有特殊颜色的物质才好识别。因此,应加含有I-和H+的物质使其变成I2,而且存在着能I2与结合成蓝色物质的淀粉。因而,③中含有I-和淀粉,⑥中含有H+(由CH3COOH溶液电离而得)。
答案:B
方法要领:题中向考生传达了我国在2000年消灭碘缺乏症的目标和达到此目标的办法。解题关键是:抓住IO3-+5I-+6H+=3I2+2H2O,可知所给物质要提供I-和H+。
本题属于原理型信息给予题,它给出两条反应原理的新信息:一是食盐中的碘是以碘酸钾(KIO3)的形式存在;二是给出了IO3-、I-、H+3种离子共同存在时发生的生成I2的氧化还原反应的信息,此反应原理成为实现问题解决的根本依据。为此,应能提取出I2和淀粉互检的已有知识,并把IO3-被I-在H+存在下还原为I2的反应和I2的常规检验联系起来,从而完成对问题的解答。
如果能深入把握KI淀粉试纸检验出氧化性物质(如Cl2、O3等)的反应原理,将已有知识迁移运用到IO3-氧化I-(H+存在)的新情境中,则不难找出用碘化钾淀粉试纸(H+存在)检出IO3-的方法。可见,将知识系统化、结构化,对形成知识的类比与迁移能力,是十分重要的。
例5 甲、乙、丙三种溶液各含有一种X--(X--为Cl-、Br-、I-)离子。向甲中加淀粉溶液和氯水,则溶液变橙色,再加丙溶液,颜色无明显变化。则甲、乙、丙依次含有(1991年全国高考题)
A.Br-、Cl-、I- B.Br-、I-、Cl- C.I-、Br-、Cl- D.Cl-、I-、Br-
思路分析:在甲溶液中加入淀粉溶液和氯水,淀粉不显蓝色,证明甲中不含I-离子,溶液显橙色,证明甲中含Br-离子(溴水显橙色);再加丙溶液,无明显变化,表明丙中不含I-离子。综上所述,甲中含Br-离子,乙中含I-离子,丙中含Cl-离子。
答案:B
方法要领:利用非金属置换反应规律进行逻辑分析。非金属性较强的单质能从盐溶液(或酸溶液)中把非金属性弱的非金属置换出来。
本题考查了对卤素离子还原性强弱的理解及卤素置换实验现象的分析,它运用的知识有:Cl2+2Br-=2Cl-+Br2,Cl2+2I-=2Br-+I2和Br2+2I-=2Br-+I2,I2遇淀粉变蓝色。
例6 冰箱致冷剂氟氯甲烷在高空中受紫外线辐射产生Cl原子,并进行下列反应:Cl+O3→ClO+O2,ClO+O→Cl+O2。下列说法不正确的是(1998年上海高考题)
A.反应后将O3转化为O2 B.Cl原子是总反应的催化剂
C.氟氯甲烷是总反应催化剂 D.Cl原子反复起分解O3的作用
思路分析:可将两个分反应合并得总反应2O3→3O2,催化剂应是Cl而不是氟氯甲烷,由于催化剂在反应前后物质的量保持不变,故Cl反复起分解O3的作用。
答案:C
方法要领:这是一道与环境化学相关的题目,也属信息给予题。中间产物和催化剂有相同点:①均参与了反应过程;②当分反应合并成总反应时两者均可消去,即生成量等于消耗的量。两者的不同之处在于催化剂先消耗后生成,而中间产物则先生成后消耗。据此可判断出Cl在上述过程中是催化剂。平时要善于比较一些相关的概念,找出它们的本质区别。
例7 某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO-和ClO3-的浓度之比为1:3,则Cl2与NaOH反应时,被还原的氯元素与被氧化的氯元素物质的量之比为(1999年全国高考题)
A.21:5 B.11:3 C.3:1 D.4:1
思路分析:Cl2与NaOH溶液反应,Cl2既是氧化剂又是还原剂,从电子得失角度分析,被氧化的Cl分别从0→+1、0→+5,根据题目所给条件分析得ClO-和ClO3-的个数之比为1:3,则被氧化的一方4个0价Cl共失电子1+3×5=16;被还原Cl从0→-1,欲使得失电子总数相等,则需16个0价Cl。所以,被还原的氯元素与被氧化的氯元素的物质的量之比为16:4=4:1。 答案:D
方法要领:本题考查利用氧化还原反应的本质分析问题的能力,考查学生应变的灵活性。Cl2与NaOH溶液反应,本身既是氧化剂又是还原剂,氧化产物为NaClO、NaClO3,还原产物为NaCl,通过电子守恒原理快解。
例8 KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯.其变化可表述为: KClO3+ HCl(浓)== KCl+ ClO2↑+ Cl2↑+
 (1)请完成该化学方程式并配平(未知物化学式和化学计量数填入框内)
(1)请完成该化学方程式并配平(未知物化学式和化学计量数填入框内)
(2)浓盐酸在反应中显示出来的性质是 (填写编号,多选倒扣分)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)ClO2具有很强的氧化性。因此,常被用作消毒剂,其消毒效率(以单位质量得到的电子数表示)是Cl2的 倍。(2000年上海市高考题)
思路分析:(1)此题的难点是方程式的配平,用化合价升降法配平时,首先要分清氧化产物是Cl2还原产物是ClO2,KCl中的Cl-来源于盐酸,化合价没有变化,再配平氧化剂,还原剂,氧化产物和还原产物的计量数,最后依据原子种类和个数守恒,配平其它物质的计量数和补加未知物。(2)由配平的方程式可知,参加反应的浓盐酸有一半被氧化,另一半起了酸作用。(3)消毒后,Cl元素的价态为为-1价,对ClO2单位质量得电子(1/67.5)×5;对Cl2单位质量得电子:(1/71)×2;二者的比值为2.63。
答案:(1)2 4 2 2 1 2 H2O (2) ② (3)2.63
方法要领:此题考查了氯及其化合物的相互转化和性质,氧化还原反应方程式的配平,氧化性还原性分析,电子转移数目的计算等知识;此题是一信息题,情境新颖,思考量大,有效地考查了学生的分析问题的能力,代表了今后高考命题的方向。
 例9 已知氯水中有如下平衡:Cl2+H2O
HCl+HClO。常温下,在一个体积为50mL的针筒里吸入40mL氯气后,再吸进10mL水。写出针筒中可能观察到的现象
。
例9 已知氯水中有如下平衡:Cl2+H2O
HCl+HClO。常温下,在一个体积为50mL的针筒里吸入40mL氯气后,再吸进10mL水。写出针筒中可能观察到的现象
。
若将此针筒长时间放置,又可能看到何种变化 ;试用平衡观点加以解释
。(1994年上海市高考题)
 思路分析:因Cl2与H2O反应而溶解,气体体积缩小,溶液呈浅黄绿色。若此针筒长时间放置,气体体积进一步缩小,气体和溶液均变成无色;原因是氯水中的平衡Cl2+H2O HCl+HClO,由于HClO逐渐分解(2HClO=2HCl+O2)而不断地向右移动,最终Cl2耗尽全部转化为O2,导致气体体积缩小和黄绿色消退。
思路分析:因Cl2与H2O反应而溶解,气体体积缩小,溶液呈浅黄绿色。若此针筒长时间放置,气体体积进一步缩小,气体和溶液均变成无色;原因是氯水中的平衡Cl2+H2O HCl+HClO,由于HClO逐渐分解(2HClO=2HCl+O2)而不断地向右移动,最终Cl2耗尽全部转化为O2,导致气体体积缩小和黄绿色消退。
 答案:气体体积缩小,溶液呈浅黄绿色。气体体积继续减小,气体和溶液均变成无色;氯水中的平衡Cl2+H2O HCl+HClO,又由于2HClO=2HCl+O2,HClO不断分解,平衡右移,最终Cl2耗尽全部转化成O2。由总反应式2Cl2+2H2O===4HCl+O2,可知,气体体积减少。
答案:气体体积缩小,溶液呈浅黄绿色。气体体积继续减小,气体和溶液均变成无色;氯水中的平衡Cl2+H2O HCl+HClO,又由于2HClO=2HCl+O2,HClO不断分解,平衡右移,最终Cl2耗尽全部转化成O2。由总反应式2Cl2+2H2O===4HCl+O2,可知,气体体积减少。
方法要领:回答实验现象要完整并且表达确切。
例10 某化学课外小组用海带为原料制取少量碘水。现用CCl4从碘水中萃取碘并用分液漏斗分离两种溶液,其实验操作可分为如下几步:(1991年全国高考题)
A. 把盛有溶液的分液漏斗放在铁架台的铁圈中
B. 把50mL碘水和15mLCCl4加入分液漏斗中,并盖好玻璃塞
C. 检验分液漏斗活塞和上口的玻璃塞是否漏液
D. 倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正
E. 打开活塞,用烧杯接收溶液
F. 从分液漏斗上口倒出上层水溶液
G. 将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔
H. 静置,分层
就此实验,完成下列填空:
(1)正确操作步骤的顺序是 → → A→G→ →E→F。
(2)上述E步骤的操作中应注意
上述G步骤操作的目的是
(3)能选用CCl4从碘水中萃取碘的原因是
(4)下列物质,不能作为从溴水中萃取溴的溶剂是
A.热裂汽油 B.苯 C.酒精 D.正庚烷
思路分析:(1)检验分液漏斗活塞和上口的玻璃塞是否漏液,这当然是第一步。B、D的操作属于萃取,E、F属于分液操作,A、G、H是分液前的准备操作。(4)中的热裂汽油中,含碳碳双键,与溴水发生加成反应,而酒精与溴水互溶,所以两者均不适宜作萃取剂。
答案:(1)CBDH;(2)使漏斗下端管口紧靠烧杯内壁,及时关闭活塞,不要让上层液体流出;使漏斗内外空气相通,以保证E操作时漏斗里液体能够流出;(3)四氯化碳与水不溶,I2且在四氯化碳溶解度比在水中大很多;(4)A、C
方法要领:萃取和分液操作是中学化学实验中分离物质的常用方法之一,本题所涉及到的知识的技能有:分液漏斗的作用,萃取操作步骤及每一步聚的目的,萃取操作中的注意事项,萃取剂的性质及选择原则;碘在水和CCl4等有机溶剂中的溶解性,热裂汽油的不饱和性,乙醇和水的互溶性等。只有掌握这些基本知识,并在学生实验中注意这些问题,才能在解决实际问题时综合运用这些知识进行正确的推理和判断。
例11 实验室可用氯气与金属铁反应制备无水三氯化铁,该化合物呈棕红色,易潮解,100℃左右时升华,下图是两个学生设计的实验装置,左边的反应装置相同,而右边的产物收集装置则不同,分别如(Ⅰ) (Ⅱ)所示:(2000年全国高考题)

(1)B中反应的化学方程式为: 。
(2)D中的反应开始前,需排除装置中的空气,应采取的方法是: 。
(3)D中反应的化学方程式为: 。
(4)装置(Ⅰ)的主要缺点是: 。
(5)装置(Ⅱ)的主要缺点是: ,如果选用此装置来完成实验,则必须采取的改进措施是: 。
思路方法:此题综合了氯气的性质、制法,三氯化铁的性质和制取,化学实验操作及实验装置等问题。此题中涉及的制取氯气和三氯化铁的原理比较简单,排除装置中空气的方法属常识性操作,(1)、(2)、(3)问容易作答。只要根据题给信息,对装置(Ⅰ)、(Ⅱ)的不同部分进行对比分析,答案就在(Ⅰ)、(Ⅱ)两图中,(4)、(5)问即可得解。
1.分清氯水、溴水的成分,反应时的作用和褪色的原理。
 氯水中正因为存在可逆反应Cl2+H2O HCl+HClO,使其成分复杂且随着条件的改变,平衡发生移动,使成分发生动态的变化。当外加不同的反应物时,要正确判断是何种成分参与了反应。氯水中的HClO能使有色物质被氧化而褪色。反之,也有许多物质能使氯水、溴水褪色,发生的变化可属物理变化(如萃取),也可属化学变化,如歧化法(加碱液)、还原法(如Mg、SO2等)、加成法(加不饱和的有机物)等。值得一提的是有时虽然发生化学变化,但仍生成有色物,如Br2与Fe或KI反应。
氯水中正因为存在可逆反应Cl2+H2O HCl+HClO,使其成分复杂且随着条件的改变,平衡发生移动,使成分发生动态的变化。当外加不同的反应物时,要正确判断是何种成分参与了反应。氯水中的HClO能使有色物质被氧化而褪色。反之,也有许多物质能使氯水、溴水褪色,发生的变化可属物理变化(如萃取),也可属化学变化,如歧化法(加碱液)、还原法(如Mg、SO2等)、加成法(加不饱和的有机物)等。值得一提的是有时虽然发生化学变化,但仍生成有色物,如Br2与Fe或KI反应。
29、某金属锡样品的纯度可通过下述方法分析:将试样溶于酸,反应方程式为:
 Sn+2HCl
SnCl2+H2↑ 再加入过量 FeCl3 溶液,发生如下反应:
Sn+2HCl
SnCl2+H2↑ 再加入过量 FeCl3 溶液,发生如下反应:
 SnCl2+2 FeCl3 2 FeCl2+SnCl4 ,最后用已知浓度的 K2Cr2O7 溶液滴定生成的Fe2+,反应式为:
SnCl2+2 FeCl3 2 FeCl2+SnCl4 ,最后用已知浓度的 K2Cr2O7 溶液滴定生成的Fe2+,反应式为:
 6FeCl2+K2Cr2O7 +14HCl 6FeCl3 +2KCl+2CrCl3+7H2O
6FeCl2+K2Cr2O7 +14HCl 6FeCl3 +2KCl+2CrCl3+7H2O
现有该金属试样0.613克,经上述各步反应后,共用去0.100mol/L K2Cr2O7溶液16.0ml。
请列式求解试样中锡的质量分数(假定杂质不参加反应)。(相对原子质量 Sn-119)
28、 在一定条件下可发生反应:2SO2(g)+O2 (g) 2SO3(g)。现取8L SO2和6L O2混合,当反应达到平衡后,测得混合气体的体积减小10% 。求:
在一定条件下可发生反应:2SO2(g)+O2 (g) 2SO3(g)。现取8L SO2和6L O2混合,当反应达到平衡后,测得混合气体的体积减小10% 。求:
(1)SO2的转化率。
(2)平衡混合气体中SO3的体积分数。
27、化合物A(C8H8O3)为无色液体,难溶于水,从A开始,可发生图示的一系列反应,图中H的化学式为C6H6O,G能发生银镜反应,A硝化时可生成两种一硝基取代物。
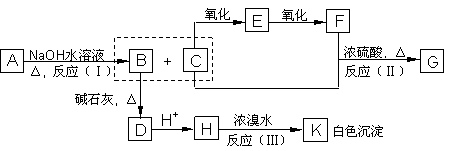

(1) 写出下列化合物可能的结构简式:
A___________________,E___________________。
(2) 写出反应类型:(Ⅰ)__________(Ⅱ)__________(Ⅲ)__________
(3)
 写出化学方程式:H K ___________________________________________;
写出化学方程式:H K ___________________________________________;
 C E _____________________________________________;
C E _____________________________________________;
 C+F G___________________________________________。
C+F G___________________________________________。
26、具有强烈催化作用的有机物质二乙烯酮,是由单体乙烯酮(CH2=C=O)聚合而成的。已知乙烯酮可与含活泼氢原子的化合物在不同的条件下发生加成反应(见图示),生成各种化合物(加成的取向完全一样),如与氯化氢加成生成乙酰氯。


回答下列问题:
(1) 写出A、B的结构简式:A___________________,B__________________。
(2) 反应①的化学方程式______________________________________;
反应②的化学方程式______________________________________;
反应③是乙酰氯与过量氨水混合而发生的,其化学方程式为
______________________________________。
25、 在10.0℃和2×105Pa的条件下,反应aA(g) dD(g)+eE(g)建立平衡后,再逐步增大体系的压强(维持温度不变),下表列出了不同压强下反应建立平衡时物质D的浓度(压强增大到一定程度时,E可能会发生状态的改变):
在10.0℃和2×105Pa的条件下,反应aA(g) dD(g)+eE(g)建立平衡后,再逐步增大体系的压强(维持温度不变),下表列出了不同压强下反应建立平衡时物质D的浓度(压强增大到一定程度时,E可能会发生状态的改变):
|
压强(Pa) |
2×105 |
5×105 |
1×106 |
|
D的浓度(mol/L) |
0.085 |
0.20 |
0.44 |
根据表中压强和浓度变化的数据关系,回答下列问题:
(1) 压强从2×105增加到5×105Pa时,平衡向______(正或逆)反应方向移动,理由是_________________________________________________。
(2) 压强从5×105增加到1×106Pa时,平衡向________(正或逆)反应方向移动,理由是________________________________________,这可能是由于__________________。
24、 298K时,合成氨反应的热化学方程式为N2(g)+3H2(g) 2NH3(g)+92.4KJ/mol
298K时,合成氨反应的热化学方程式为N2(g)+3H2(g) 2NH3(g)+92.4KJ/mol
在该温度下,取1mol N2和3mol H2放在一密闭容器中,在催化剂催化下进行反应,测得反应放出的热量总是小于92.4KJ,其原因是__________________________________________。
23、 在一定条件下,可逆反应A2(g)+B2(g) 2C(g)达到平衡时,各物质的浓度为:A2 0.5mol/L,B2 0.1mol/L,C 1.6mol/L,若用a、b、c分别表示A2、B2、C的初始浓度(mol/L),则:(1)a、b应满足的关系式是____________________________;
在一定条件下,可逆反应A2(g)+B2(g) 2C(g)达到平衡时,各物质的浓度为:A2 0.5mol/L,B2 0.1mol/L,C 1.6mol/L,若用a、b、c分别表示A2、B2、C的初始浓度(mol/L),则:(1)a、b应满足的关系式是____________________________;
(2)a的取值范围是___________________________________。
22、元素周期表中位于对角线的两种元素其性质相似称之为对角线规律,根据周期表对角线规律,金属Be与Al的单质及其化合物的性质相似。又知AlCl3熔沸点较低,易升华。根据题目所给信息,试回答下列问题:
(1)写出Be与NaOH溶液反应的离子方程式(生成物之一是Na2BeO2):
_______________________________________________________
(2 ) Be(OH)2和Mg(OH)2可用试剂____________鉴别,其化学方程式为:
________________________________________________________________________
(3 )BeCl2是____________(填“离子”或“共价”)化合物,其电子式为___________________。
BeCl2水溶液呈酸性,其水解的离子方程式为___________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com