
题目列表(包括答案和解析)
3.下列离子方程式正确的是
A.向苯酚钠溶液中通人少量的CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32-
B.Ca(HCO3)2溶液中加入过量澄清石灰水:Ca2++HCO3-+OH-=CaCO3↓+H2O
C.KI溶液和KIO3溶液混合并加入稀硫酸:IO3-+I-+6H+ = I2+3H2O
D.向KHSO4溶液中滴人Ba(OH)2溶液使pH=7 SO42-+H++Ba2++OH-=BaSO4↓+H2O
2.下列离子方程式书写正确的是
A.等体积、等物质的量浓度的Ba(OH)2溶液与NaHCO3溶液混合
Ba2++2OH-+2HCO3-====BaCO3↓+CO32-+H2O
B.次氯酸钙溶液中通入少量SO2气体:
Ca2++2ClO-+SO2+H2O====CaSO3↓+2HClO
C.NH4HCO3溶液与足量NaOH溶液混合
NH4++HCO3-+2OH-====NH3·H2O+ CO32-+ H2O
D.明矾溶液中加入过量的Ba(OH)2溶液:
2Al3++3SO2-4+3Ba2++6OH-===3BaSO4↓+2Al(OH)3↓
1.能正确表示下列化学反应的离子方程式是
A.氯气通入水中:Cl2+H2O==2H++ClO-+Cl-
B.硫化钠溶于水中:S2-+2H2O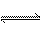 H2S+2OH-
H2S+2OH-
C.铜与稀硝酸反应:Cu+4H++NO3- ==Cu2++NO↑+2H2O
D.水玻璃与盐酸反应:SiO32-+2H+=H2SiO3↓
9.在25℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,下列热化学方程式正确的是
A. CH3OH(l)+ O2(g)=CO2(g)+2H2O(l) DH=+725.8 kJ / mol
O2(g)=CO2(g)+2H2O(l) DH=+725.8 kJ / mol
B. 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) DH=-1452 kJ / mol
C. 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) DH=-725.8 kJ / mol
D. 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) DH=+1452 kJ / mol
8. C(石墨)+O2(g)=CO2(g) △H=-393.51 kJ ·mol-1
C(金刚石)+O2(g)=CO2(g) △H=-395.41 kJ ·mol-1
据此判断,下列说法中正确的是
A.由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的低
B.由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的高
C.由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的低
D.由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的高
7.已知25℃、101kPa下,石墨、金刚石燃烧的热化学方程式分别为:
C(石墨)+O2(g)=CO2(g);ΔH= -393.51 kJ/mol
C(金刚石)+O2(g)=CO2(g);ΔH= -395.41 kJ/mol
据此推理所得到的下列结论正确的是
A.金刚石的燃烧热比石墨的燃烧热小
B.石墨晶体中碳碳键的强度小于金刚石中的碳碳键
C.石墨的能量比金刚石的能量高 D.由石墨制备金刚石一定是吸热反应
6. 以NA代表阿伏加德罗常数,有关反应
C2H2(g)+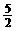 O2(g)→2CO2(g)+H2O(l);ΔH= -1300kJ/mol
O2(g)→2CO2(g)+H2O(l);ΔH= -1300kJ/mol
下列关于热化学方程式的说法正确的是
A.有10NA个电子转移时,该反应放出1300kJ的能量
B.有NA个水分子生成且为液体时,吸收1300kJ的能量
C.有4NA个碳氧共用电子对生成时,放出1300kJ的能量
D.有8NA个碳氧共用电子对生成时,放出1300kJ的能量
5. 已知胆矾溶于水时溶液温度降低。胆矾分解的热化学方程式为:
CuSO4·5H2O(s) CuSO4(s)+5H2O(l);ΔH= +Q1
kJ/mol
CuSO4(s)+5H2O(l);ΔH= +Q1
kJ/mol
室温下,若将1mol无水硫酸铜溶解为溶液时放热Q2 kJ,则Q1与Q2的关系为
A.Q1>Q2 B.Q1=Q2 C.Q1<Q2 D.无法比较
4.氢气(H2)、一氧化碳(CO)、辛烷(C8H18)、甲烷(CH4)的热化学方程式分别为:
H2 (g)+1/2O2(g)=H2O(l); ΔH= -285.8 kJ/mol
CO(g)+1/2O2(g)=CO2(g); ΔH= -283 kJ/mol
C8H18(l)+25/2O2(g)=8CO2(g)+9H2O(l); ΔH= -5518 kJ/mol
CH4(g)+ 2O2(g)= CO2(g)+ 2H2O(l); ΔH= -890.3 kJ/mol
相同质量的H2、CO、C8H18、CH4完全燃烧时,放出热量最少的是
A.H2(g) B.CO(g) C.C8H18(l) D.CH4(g)
3.已知充分燃烧a g乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是
A.2C2H2(g)+5O2(g)= 4CO2(g)+2H2O(l);ΔH= -4b kJ/mol
B.C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l);ΔH= 2b kJ/mol
C.2C2H2(g)+5O2(g)= 4CO2(g)+2H2O(l);ΔH= -2b kJ/mol
D.2C2H2(g)+5O2(g)= 4CO2(g)+2H2O(l);ΔH= b kJ/mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com