
题目列表(包括答案和解析)
7.(1)冷凝、回流 防止倒吸
|
(3)由于SO2产生的快而多且溶解度较大。Ca(OH)2溶解度很小,生成了Ca(HSO3)2溶液的缘故。 取样后,向其中加入氢氧化钠溶液,观察是否有沉淀生成。(或者加热、加盐酸检验SO2气体等方法。)
(4)CuO、CuS、Cu2S
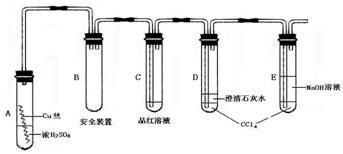
7.某研究性学习小组为研究Cu与浓H2SO4的反应,设计如下实验探究方案(装置中的固定仪器和酒精灯均未画出)。
实验选用细铜丝、98.3%H2SO4、品红溶液、澄清石灰水、CCl4、NaOH溶液等药品,铜丝被卷成螺旋状,一端浸入浓H2SO4中,另一端露置在液面上方。以下是该学习小组部分交流记录及后续探究实验的记录:
 材料一:小组交流摘录
材料一:小组交流摘录
学生1:加热前,无现象发生;加热后,液面下的铜丝变黑,表面产生气泡,有细小黑色颗粒状物质从铜丝表面进入浓硫酸中,黑色物质是什么?值得探究!
学生2:,我也观察到黑色颗粒状物质,后来逐渐转变为灰白色固体,我想该灰白色固体极有可能是未溶于浓硫酸的无水CuSO4。
学生3:你们是否注意到液面以上的铜丝也发黑,而且试管上部内壁有少量淡黄色固体凝聚,会不会液面以上的铜丝与硫发生了反应,我查资料发现:2Cu+S→Cu2S(黑色)。
材料二:探究实验剪辑
实验1:将光亮的铜丝在酒精灯火焰上灼烧变黑,然后插入稀硫酸中,铜丝重新变得光亮,溶液呈蓝绿色;将光亮的铜丝置入加热的硫蒸气中变黑,然后插入稀硫酸中无变化。
实验2:截取浓硫酸液面上方变黑的铜丝,插入稀硫酸中无变化;将浓硫酸液面下方变黑的铜丝,插入稀硫酸,黑色变浅了些,溶液呈蓝色。
实验3:将溶液过滤得黑色颗粒状物质,经稀硫酸洗、蒸馏水洗、干燥后放入氧气流中加热,然后冷却,用电子天平称重发现质量减少。
根据上述材料回答下列问题
(1)A试管上方的长导管的作用是 ;D、E两支试管中CCl4的作用是 。
(2)加热过程中,观察到A试管中出现大量白色烟雾,起初部分烟雾在试管上部内壁析出淡黄色固体物质,在持续加热浓硫酸(沸腾)时,淡黄色固体物质又慢慢地消失。写出淡黄色固体消失的化学反应方程式: 。
(3)对A试管中的浓H2SO4和铜丝进行加热,很快发现C试管中品红溶液褪色,并有大量气泡冒出,已知SO2难溶于CCl4中,但始终未见D试管中澄清石灰水出现浑浊或沉淀。你的猜想是: 。设计实验验证你的猜想 。
(4)根据上述研究,结合所学知识,你认为液面下方铜丝表面的黑色物质成分是 。(写化学式)
4.陈放水样中氧的含量:5.20mg·L-1
计算过程:102.2mL中氧的含量:
n(O2)=0.25×c(S2O32-)×V(S2O32-)
=0.25×9.841×10-3mmol·mL-1×6.75mL=1.66×10-2mmol
氧含量:r(O2)=1.66×10-2mmol×32.00mg·mmol-1/102.2×10-3L=5.20mg·L-1
注:陈放引起氧的消耗量=8.98mg·L-1-5.20mg·L-1=3.78mg·L-1
3.新鲜水样中氧的含量:8.98mg·L-1
计算过程:103.5mL水样中氧的含量:
n(O2)=0.25×c(S2O32-)×V(S2O32-)
=0.25×9.841×10-3mol·L -1×11.80×10-3L=2.903´10-5mol
氧含量:r(O2)=2.903×10-5mol×32.00×103mg·mol-1/103.5×10-3L
=8.98mg·L-1(3分)
注:新鲜水样的氧饱和度=(8.98/9.08)×100%=98.9%
2.标准溶液的浓度:9.841×10-3 mol·L-1
计算过程:
c(IO3-)=174.8×10-3g·L-1/214.0g·mol-1=8.168×10-4mol·L-1(1分)
c(S2O32–)=6×c(IO3–)×V(IO3-)/V(S2O32-)
=6×8.168×10-4mol·L-1×25.00mL/12.45mL=9.841×10-3mol·L-1(3分)
5.以上测定结果说明水样具有什么性质?
答案:1.步骤1:2Mn2++O2+4OH-=2MnO(OH)2(1分)
步骤2:2I-+MnO(OH)2+4H+=Mn2++I2+3H2O(1分)
或3I-+MnO(OH)2+4H+=Mn2++I3-+3H2O
步骤3:I2+2S2O32-=2I-+S4O62-(1分)
或I3-+2S2O32-=3I-+S4O62-
4.计算陈放水样中氧的含量(单位mg·L-1)。
3.计算新鲜水样中氧的含量(单位mg·L-1)。
2.计算标准溶液的浓度(单位mol·L-1)。
1.写出上面3步所涉及的化学反应方程式。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com