
题目列表(包括答案和解析)
23.在化工试剂生产中,要除去某种杂质离子,往往采用一定条件下使之生成MXAy(DE4)Z(OH)12浅黄色复盐晶体析出。化学式中OH为氢氧根,而M、A、D、E代表四种未知元素。已知⑴X+Y+Z=12(x、Y、Z为正整数)。⑵取9.7g该化合物溶于含有稀硝酸的水中,滴加硝酸钡溶液,使D、E元素完全转变为白色沉淀,过滤干燥后称量为9.32g。⑶滤液中A、M以阳离子形式存在,用胶头滴管滴滤液2-3滴在白色点滴板(或玻璃片)上,再滴加1-2滴硫氰化钾溶液,溶液呈血红色。⑷往滤液中通入足量的硫化氢气体,使A离子全部被还原后,产生黄色沉淀物,过滤干燥后,称量为0.96g。⑸化合物中A元素的百分含量为34.64%。
试通过计算推理判断:
⑴ 确定D和E:
D是 ,E是 (写元素符号)。
⑵ 确定x、y、z和A:
x== y== z== A是 。
⑶ M代表的元素是 ;化合物的化学式为 。
[专题一 基本概念](答案)
22.著名的“侯氏制碱法”:第一步反应是先向氨化的饱和食盐水中通入CO2而使小苏打析出,该反应可以表示为:NaCl + NH3 +CO2 + H2O == NaHCO3↓ + NH4Cl。在40℃时,向434g饱和食盐水中通入44.8L(标准状况)氨气,在向其中通入稍过量CO2。通过计算求:
(1) 可析出小苏打多少g?
(2) 是否有NH4Cl析出?
(3) 若降温至10℃,可析出NH4Cl多少g?
(溶解度:40℃时,NaCl 37g;NaHCO3 13g;NH4Cl 46g;10℃时,NH4Cl 33g)
21.已知A+B→C+水。t℃,A、B、C三种物质的溶解度分别为S1、S2、S3g。现取t℃时A的饱和溶液Mg,B的饱和溶液Ng,混合后恰好完全反应生成C物质Pg。
(1)求反应中生成水多少g?
(2)通过计算推断:在此反应中,C物质沉淀的条件是什么?
20.A、B、C是在中学化学中常见的三种化合物,它们各由两种元素组成。甲乙是两种单质。这些化合物、单质之间的关系如下图所示
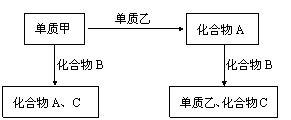
据此判断
⑴在A、B、C这三种化合物中,必含乙元素的是
⑵单质乙必为 (填“金属”或“非金属”),其理由为
⑶单质乙的化学式可能是 ,则化合物B的化学式是 。
19. 从下列括号中选择合适的用语,填写在的横线上,使它跟各种变化的情况相符(分解、潮解、溶解、蒸发、干馏、蒸馏、结晶、化合、挥发、升华、风化):
① 食盐放在水中逐渐消失__________;
② 萘在空气中逐渐消失________;
③ 不盖灯帽的酒精灯,灯内酒精会减少,以致消失________;
④ 无水氯化钙吸收空气中的水分______;
⑤ 生石灰吸收空气中的水分___________;
⑥ 胆矾受热后变成白色粉末___________;
⑦ 石碱晶体在空气中变成白色粉末___________;
⑧ 氢氧化铜加热后变成黑色固体____________;
⑨ 木块隔绝空气加热后变成黑色固体__________;
⑩ 饱和KNO3溶液降温,出现晶体______。
18.硼酸晶体呈片状,有滑腻感,可作润滑剂。硼酸分子结构可表示为 硼酸对人体的受伤组织有和缓的防腐作用,故可用于医药和食品防腐等方面。可见硼酸当属于 。
A.强酸 B.中强酸 C.弱酸
科研表明:在多数情况下,元素的原子在形成分子或离子时,其最外电子层具有达到8个电子稳定结构的趋向。在硼酸分子中,原子最外层电子达到8个电子稳定结构的原子有 个。
已知0.01mol硼酸可被20mL 0.5mol•L-1NaOH溶液恰好完全中和,据此推测:硼酸在水中显酸性的原因是(写方程式) ;
硼酸和甲醇在浓H2SO4存在的条件下,可生成挥发性硼酸酯,试写出硼酸与甲醇完全酯化的化学方程式: 。
17.固体物质A的化学式为NH5,它的所有原子的最外电子层都符合相应的稀有气体原子的电外电子层结构。适当加热该物质,它可分解成两种气体。A物质中的氢元素的化合价为 和 。A是 型化合物,它的电子式是 。将A溶入含紫色石蕊试液的水中,产生的现象是 。
16.锗酸铋(简称BGO)是我国研制成功的一种优良的闪烁晶体材料,其中锗元素处于它的最高价态,铋元素的价态与它跟氯形成某些共价化合物所呈的价态相同,且此氯化物中铋具有8电子稳定结构。BGO的化学式是
A.Bi3Ge3O13 B.Bi4Ge3O12 C.Bi4Ge3O16 D.Bi3Ge3O12
  HO? B?OH HO? B?OH│ OH |
15.我国拥有世界上最大的稀土矿,品味甚高,以RE表示稀土元素,可以向RE的硫酸盐溶液中加入粉末状的Na2SO4,使稀土元素转入沉淀,反应为RE2(SO4)3 + Na2SO4 + x H2O→RE2(SO4)3·Na2SO4·x H2O↓(x == 1.2)下列有关叙述正确的是
A.该反应为复分解反应 B.该反应一定在强碱溶液中进行
C.产生的沉淀物属于复盐 D.产生的沉淀物一定是难溶物质
14.下列关于物质的分类正确的组合是
 分 类 分 类组 合 |
碱 |
酸 |
盐 |
碱性氧化物 |
酸性氧化物 |
|
A |
纯碱 |
盐酸 |
烧碱 |
氧化铝 |
二氧化氮 |
|
B |
烧碱 |
硫酸 |
食盐 |
氧化镁 |
一氧化碳 |
|
C |
苛性钠 |
醋酸 |
硝酸 |
过氧化钠 |
二氧化硫 |
|
D |
苛性钾 |
油酸 |
苏打 |
氧化钠 |
硫酐 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com