
题目列表(包括答案和解析)
14.实验室用燃烧法测定某氨基酸(CxHyNzOp)的分子组成。取m g 该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2。按下图所示装置进行实验。
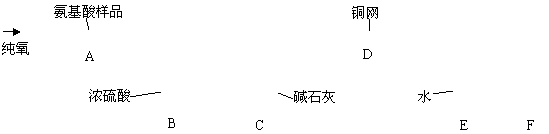

请回答下列问题:
(1)实验开始时,首先要通入一段时间的氧气,其理由是________________________。
(2)以上装置中需要加热的仪器有_________________(用字母填空,下同)。操作时应先点燃_______处的酒精灯。
(3)A装置中发生反应的化学方程式是________________________________ _____。
(4)装置D的作用是________________________________________________ _____。
(5)读取N2的体积时,应注意①__________ __;②________ ___。
(6)实验中测得N2的体积为V mL(标准状况)。为确定此氨基酸的化学式,还需要的有关数据是________________________。
13.化合物A是石油化工的一种重要的原料,用A和水煤气为原料烃下列途径合成化合物D(分子式为C3H6O3)
 已知:(1)
已知:(1)
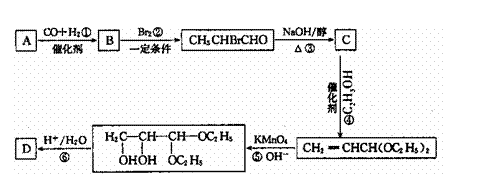
(2)
(1)写出下列物质的结构简式: A. D.
(2)指出反应②反应类型
(3)写出反应③的化学方程式 。
(4)反应④的目的是 。
(5)化合物G是D的一种同分异构体,它最早发现于酸牛奶中,是人体内糖类代谢的
中间产物。G在浓硫酸存在的条件下加热,既可生成能使溴水褪色的化合物E(C3H4O2),
又可生成六原环状化合物F(C5H3O4),请分别写出G生成E和F的化学方程式:
G→E:
G→F:
12.有甲、乙两份等体积的浓度均为 的氨水,pH=11。
的氨水,pH=11。
①将甲用蒸馏水稀释100倍,则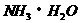 的电离平衡向__________(填“促进”或“抑制”)电离的方向移动,溶液的pH将变为____________(填序号)
的电离平衡向__________(填“促进”或“抑制”)电离的方向移动,溶液的pH将变为____________(填序号)
A. 9~10之间 B. 11
C. 12~13之间 D. 13
②将乙用 的
的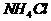 溶液稀释100倍,稀释后的乙溶液与稀释后的甲溶液比较,甲的pH__________(填“大于”、“小于”或“等于”)乙,其原因是
溶液稀释100倍,稀释后的乙溶液与稀释后的甲溶液比较,甲的pH__________(填“大于”、“小于”或“等于”)乙,其原因是
_____________________________________________________________________。
11.已知a、E、b为三种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下:
|
粒子代码 |
a |
E |
b |
|
原子核数 |
单核 |
三核 |
双核 |
|
粒子的电荷数 |
一个单位正电荷 |
0 |
一个单位负电荷 |
物质A由a、b构成,B、C都是单质,反应①、②都是用于工业生产的反应,各
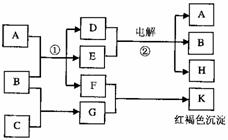 有关物质之间的相互反应转化关系如下图所示,部分生成物已略去。请填写下列空白:
有关物质之间的相互反应转化关系如下图所示,部分生成物已略去。请填写下列空白:
(1) 写出b粒子的电子式_______________
C在元素周期表中的位置_____________
(2)写出反应①的离子方程式____________
写出反应②的化学方程式______
(3) 实验室配制G溶液时需要加入一定量______,
理由是
(用相关文字和离子方程式表示)。
10.在恒温恒容的密闭容器中,发生反应3A(g)+B(g) 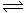 xC(g)。
xC(g)。
Ⅰ、将3molA和2molB在一定条件下反应,达平衡时C的体积分数为a;
Ⅱ、若起始时A、B、C投入的物质的量分别为n(A)、n(B)、n(C),平衡时C的体积分数也为a。
下列说法正确的是 ( )
A.若Ⅰ达平衡时,A、B、C各增加1mol,则B的转化率将一定增大
B.若向Ⅰ平衡体系中再加入3molA和2molB,C的体积分数若大于a,可断定x>4
C.若x=2,则Ⅱ体系起始物质的量应当满足3 n(B) =n(A)+3
D.若Ⅱ体系起始物质的量当满足3 n(C) +8n(A)==12 n(B)时,可断定x=4
8.在下列实验中,不能达到目的的是 ( )
A.用金属钠分别与水和乙醇反应,确定水和乙醇分子中羟基氢的活泼性强弱
B.用石墨作电极,电解Mg(NO3)2、Cu(NO3)2的混合溶液,确定铜和镁的金属活动性强弱
C.进行H2O和H2S的热分解实验,确定硫和氧两种元素的非金属性强弱
D.为确定溴乙烷中含有溴元素,向该溴乙烷中加入NaOH水溶液后,再加入AgNO3
溶液
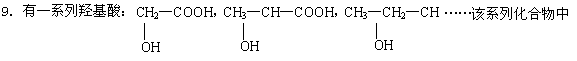 碳元素的质量分数的最大值是 ( )
碳元素的质量分数的最大值是 ( )
A.32% B.46.6% C.85.7% D.无法确定
7.
 杠杆AB两端分别挂有体积相同,质量相同的空心铜球和空心铁球,调节杠杆使其在水中保持平衡,然后小心向烧杯中央滴入浓CuSO4溶液,
杠杆AB两端分别挂有体积相同,质量相同的空心铜球和空心铁球,调节杠杆使其在水中保持平衡,然后小心向烧杯中央滴入浓CuSO4溶液,
一段时间后,下列有关杠杆的偏向判断正确的是(实验
过程中不考虑铁丝反应及两边浮力的变化) ( )
A.杠杆为导体和绝缘体时,均为A端高B端低
B.杠杆为导体和绝缘体时,均为A端低B端高
C.当杠杆为绝缘体时,A端低B端高;为导体时,A端低B端高
D.当杠杆为绝缘体时,A端高B端低;为导体时,A端低B端高
6.两份等体积、等浓度的NaOH溶液,分别与体积相等的MgCl2、AlCl3溶液混合,充分反应后,Mg2+、Al3+均恰好形成沉淀,则原MgCl2、AlCl3溶液中Cl-浓度之比为 ( )
A.1∶1 B.1∶2 C.2∶3 D.3∶2
5. 已知在101kPa时:CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-820kJ/mol。下列说法中正确的是( )
已知在101kPa时:CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-820kJ/mol。下列说法中正确的是( )
A、反应过程中能量关系可用右图表示
B、CH4的燃烧热是820kJ
C、11.2LCH4完全燃烧放出热量410kJ
D、若将此反应设计成原电池,甲烷在正极被氧化
4.已知Co2O3在酸性溶液中易被还原成Co2+,Co2O3、Cl2、FeCl3、I2的氧化性依次减弱。下列反应在水溶液中不可能发生的是 ( )
A.3Cl2 + 6FeI2 == 2FeCl3 + 4FeI3 B.Cl2 + 2Fe2+ == 2Fe3++ 2Cl-
C.Co2O3 + 6HCl == 2CoCl3 + 3H2O D.2Fe3+ + 2I- == 2Fe2+ + I2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com