
题目列表(包括答案和解析)
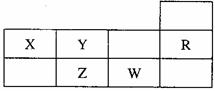
8.下表为元素周期表短周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是
A、常压下五种元素的单质中w单质的沸点最高
 B、z的氢化物的沸点比Y的氢化物的沸点高
B、z的氢化物的沸点比Y的氢化物的沸点高
C、w元素最高价氧化物的水化物酸性比z元素的强
D、w、Y的阴离子电子层结构与R原子的相同
7.pH=1的两种一元酸HX和HY溶液,分别取50mL加入足量的镁粉,充分反应后,收集到H2体积分别为v(HX)和V(HY)。若V(HX)>V(HY),则下列说法正确的是
A、HX可能是强酸
B、HX的酸性比HY的酸性弱
C、两酸的浓度大小c(HX)<c(HY)
D、pH=l的两种一元酸均稀释100倍,稀释后两溶液的pH均为3
6.镁铁混合物4.9g,溶解在过量某浓度的稀硝酸中,完全反应得到标况下气体2.24L(假设气体全为NO),则向反应后的溶液中加入足量的烧碱,则可生成沉淀的量是
A、6g B、8g C、10g D、12g
5. 一定条件下,可逆反应N2(g)+3H2(g) 2NH3(g),若N2,H2、NH3起始浓度分别为c(N2)、c(H2)、c(NH3)
(均不为0),平衡时N2、H2、NH3的浓度分别为0.1mol/L、0.3mol/L、0.08mol/L,则下列判断不合理的是
( )
一定条件下,可逆反应N2(g)+3H2(g) 2NH3(g),若N2,H2、NH3起始浓度分别为c(N2)、c(H2)、c(NH3)
(均不为0),平衡时N2、H2、NH3的浓度分别为0.1mol/L、0.3mol/L、0.08mol/L,则下列判断不合理的是
( )
A、起始时N2利H2的浓度之比为c(N2):c(H2)=l∶3
B、平衡时H2和NH3的生成速率之比为3∶2
C、N2和H2的转化率之比为1∶3
D、达到平衡后,若保持温度不变,将容器的体积增大一倍,平衡向逆反应方向移动
4.下列离子方程式表示正确的是 ( )
A.铜片加入稀硝酸中: Cu + NO3-+ 4 H+ Cu2+ + NO↑+ 2 H2O
Cu2+ + NO↑+ 2 H2O
B.过量SO2通入次氯酸钙溶液中:Ca2+ + 2ClO- + SO2 + H2O CaSO3↓+ 2HClO
CaSO3↓+ 2HClO
C.等体积、等物质的量浓度的NaHCO3和Ba(OH)2两溶液混合:
HCO3-
+ Ba2+ + OH- BaCO3↓+ H2O
BaCO3↓+ H2O
D.铁作电极电解饱和食盐水:2Cl-+ 2H2O 2OH-+ H2 ↑+ Cl2↑
2OH-+ H2 ↑+ Cl2↑
3.阿伏加德罗常数约为6.02×1023mol-1。下列叙述中正确的是 ( )
A.将含有NO2和N2O4分子共约6.02×1023个的混合气,温度降至标准状况,其体积约为22.4L
B.7.8gNa2O2与足量水充分反应转移电子数约为6.02×1022个
C.0.05molC5H12分子中所含共价键数约为6.02×1023
D.标准状况下,1molSiO2晶体中含有共价键数约为2×6.02×1023
2.下列说法不正确的是 ( )
A.在化学反应进行的过程中放出或吸收的热量称为反应热
B. 在稀溶液中,1mol酸跟1mol碱发生中和反应所放出的热量叫做中和热
C.对于吸热反应,反应物所具有的总能量总是低于生成物所具有的总能量
D.在101KPa时 , 1mol物质完全燃烧生成稳定氧化物时,所放出的热量叫做该物质的燃烧热
1.冰的晶体中,分子间存在的最强作用力是 ( )
A.离子键 B.共价键 C.氢键 D.范德瓦耳斯力
26.(18分)
(1)BDE
(2)过滤 蒸馏
(3)2I-+MnO2+4H+=Mn2++I2+2H2O
(4)苯与水互不相溶;碘在苯中的溶解度比在水中大
(5)取少量提取碘后的水溶液于试管中,加入几滴淀粉试液;观察是否出现蓝色(如果变蓝,说明还有单质碘)
21.第(1)和第(2)小题每空3分,第(3)小题两个方程式前一个1分,后一个2分
(1)A:FeS2 C.H2S D.FeCl3
(2)FeS2+2H+=Fe2++H2S↑+S
(3)FeCl2+2NaOH=Fe(OH)2↓+2NaCl; 4Fe(OH)2+O2+2H2O=4Fe(OH)3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com