
题目列表(包括答案和解析)

G H I
⑷能说明G装置中反应完全的现象是 ,其反应的化学方程式是
相关的实验步骤为:
第一步:将过量的甲醇和苯甲酸混合加热发生酯化反应
第二步:水洗提纯
第三步:蒸馏提纯
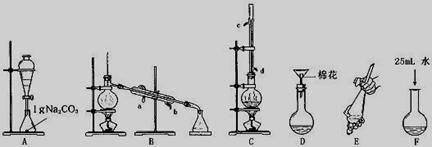
⑴上述是合成和提纯的有关装置图,请写出合成和提纯苯甲酸甲酯的操作顺序(填字母) 。
⑵C装置中除了装有15g苯甲酸和20mL过量的甲醇外还需要 , ,
作用分别是 , 。
⑶C装置中冷凝管的作用是 ,A装置中固体Na2CO3作用是 。
18.(14分)苯甲酸甲酯是一种重要的工业原料,有机化学中通过酯化反应和水解反应的原理,可以进行苯甲酸甲酯的合成和皂化反应。有关物质的物理性质见下表所示:
|
|
苯甲酸 |
甲醇 |
苯甲酸甲酯 |
|
熔点/℃ |
122.4 |
-97 |
-12.3 |
|
沸点/℃ |
249 |
64.3 |
199.6 |
|
密度/g.cm-3 |
1.2659 |
0.792 |
1.0888 |
|
水溶性 |
微溶 |
互溶 |
不溶 |
17.(6分)下列实验操作或对实验事实的描述不正确的是__ACDE__________________(填序号,错选一个倒扣1.5分,不出现负分)
A.用酸式滴定管量得KMnO4溶液20.0mL
B. 实验室快速制备少量H2、O2、NH3、HCl可以用同一种气体发生装置;
C.除去乙酸中混有的乙醇:加入生石灰后蒸馏
D.用热的NaOH溶液洗涤做过制酚醛树脂实验的试管
E.蒸馏石油时,加热一段时间后发现未加碎瓷片,立刻拔开橡皮塞并投入碎瓷片
F.配制浓硫酸与酒精混合液时,将3体积的浓硫酸倒入1体积的酒精中
16.在25mL0.1mol/LNaOH溶液中逐滴加入0.2mol/L醋酸溶液,曲线如下图所示,有关粒子浓度关系比较不正确的
A.在A、B间任一点,溶液中一定都有
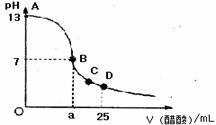 c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.在B点,a>12.5,且有
c(Na+)==c(CH3COO-)=c(OH-)==c(H+)
C.在C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
D.在D点:c(CH3COO-)十c(CH3COOH)==2c(Na+)
班级高三( ) 考号 姓名
选择题答案请一律填写在以下指定空格中:
第II卷(非选择题,共86分)
15.含有C=C的有机物与O3作用形成不稳定的臭氧化物,臭氧化物在还原剂存在下,与水作用分解为羰基化合物,总反应为:
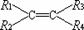
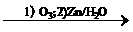
 +
+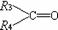 (R1、R2、R3、R4为H或烷基)。
(R1、R2、R3、R4为H或烷基)。
以下四种物质发生上述反应,所得产物为纯净物且能发生银镜反应的是
A.(CH3)2C=C(CH3)2 B.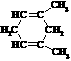 C.
C.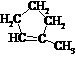 D.
D.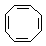
14.锂钒氧化物电池的能量密度远远超过其他材料电池,其成本低,便于大量推广,且对环境无污染。电池总反应式为;V2O5+ xLi→LixV2O5 , 下列说法不正确的是
A.向外供电时,锂离子在凝胶中向正极移动
B.正极材料是锂,负极材料为V2O5
C.正极的电极反应为:V2O5+xe-+ xLi+ →Lix V2O5
D. 负极的电极反应为:xLi-xe一→ xLi+
13.恒温下,容积均为2L的密闭容器M、N中,分别有以下列两种起始投料建立的可逆反应:3A(g) + 2B(g)  2C(g) + xD(s) 的化学平衡状态,相关数据如下:
2C(g) + xD(s) 的化学平衡状态,相关数据如下:
M:3molA 2molB; 2min达到平衡,生成D1.2mol,测得从反应开始到平衡C的速率0.3mol·L-1·min-1
N:2molC ymolD; 达到平衡时c(A)=0.6mol·L-1。
下列推断的结论中不正确的是
A.x=2 B.平衡时M中c(A)﹤0.6mol·L-1
C.y﹥0.8 D.y﹤0.8
12.冰晶石(化学式为Na3AlF6)的结构单元如右图所示,已知冰晶石熔融时电离方程式为:Na3AlF6 =3Na+ + AlF6- 。
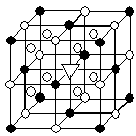 ●位于大立方体顶点和面心
●位于大立方体顶点和面心
○位于大立方体的12条棱的中点和8个小立方体的体心
那么大立方体的体心处▽所代表的微粒是
A.Na+ B.Al3+
C.F- D.AlF6-
11.Cl2、SO2均能使品红溶液褪色。后者因为品红分子结构中的发色团遇到亚硫酸后结构发生改变,生成不稳定的无色化合物。其漂白原理可用下面的反应方程式表示:
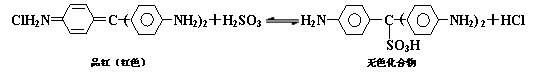 下列说法正确的是
下列说法正确的是
A.品红溶液中同时通入Cl2、SO2,漂白效果会更好
B. 加热可判断品红褪色是通入SO2还是通入Cl2引起的
C.上述可逆反应中,正反应的△H>0
D.品红分子结构中,19个碳原子都可能在同一平面上
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com