
题目列表(包括答案和解析)
15、今有两种正盐的稀溶液,分别是a mol/LNaX溶液和b mol/LNaY溶液,下列说法不正确的是
A.若a=b,pH(NaX) >pH(NaY),则相同浓度时,酸性HX>HY
B.若a=b,并测得c(X-)=c(Y-)+c(HY) ,则相同浓度时,酸性HX>HY
C.若a>b,测得c(X-)=c(Y-),则可推出溶液中c(HX)>c(HY),且相同浓度时,酸性HX<HY
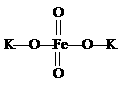 D.若两溶液等体积混合,测得c(X-)+c(Y-)+c(HX)+c(HY)=0.1mol/L,则可推出a=b=0.1 mol/L
D.若两溶液等体积混合,测得c(X-)+c(Y-)+c(HX)+c(HY)=0.1mol/L,则可推出a=b=0.1 mol/L
14、当向蓝色的CuSO4溶液中逐滴加入氨水时,观察到首先生成蓝色沉淀,而后沉淀又逐渐溶解成为深蓝色的溶液,向深蓝色溶液中通入SO2气体,又生成了白色沉淀:将白色沉淀加入稀硫酸中,又生成了红色粉末状固体和SO2气体,同时溶液呈蓝色,根据上述实验现象分析推测,下列描述正确的有
A.Cu2+和Ag+相似,能与NH3结合生成铜氨络离子
B.白色沉淀为+2价铜的某种亚硫酸盐,溶于H2SO4发生复分解反应
C.白色沉淀为+1价铜的某种亚硫酸盐,在酸性条件下发生了自身氧化还原反应
D.反应过程中消耗的SO2与生成的SO2的物质的量相等
13.锂钒氧化物电池的能量密度远远超过其他材料电池,其成本低,便于大量推广,且对环境无污染。电池总反应式为;V2O5+ xLi→LixV2O5 , 下列说法不正确的是
A.向外供电时,锂离子在凝胶中向正极移动
B.正极材料是锂,负极材料为V2O5
C.正极的电极反应为:V2O5+xe-+ xLi+ →Lix V2O5
D.负极的电极反应为:xLi-xe一→ xLi+
12、某无色溶液与NH4HCO3作用能产生气体,此溶液中可能大量共存的离子组是
A.Cl-、Mg2+、H+、Zn2+、SO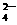 B.Na+、Ba2+、NO3-、OH
B.Na+、Ba2+、NO3-、OH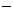 、SO
、SO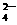
C.Ag+、K+、Cl-、H+、SO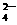 D.MnO
D.MnO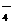 、NO
、NO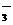 、SO
、SO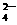 、OH-、Na+
、OH-、Na+
11.用NA表示阿伏加德罗常数的值,下列说法中正确的是
A.6.2克白磷分子中含P-P键为0.05NA
B.将含有NO2和N2O4分子共约NA个的混合气,温度降至标准状况,其体积约为22.4L
C.6.4 gS6与S8的混合物中所含S原子数一定为0.2 NA
D.2mol SO2和1 mol O2混合在V2O5存在的条件下于密闭容器中加热反应后,容器内物质分子数大于2 NA
10.对于某些离子的检验及结论一定正确的是
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32¯
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42¯ C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,不一定有Ba2+
9.2004年4月30号出版的《Science》杂志报道了中国科学家郑兰荪院士首次成功合成新型稳定小富勒烯C50Cl10,外侧有10个氯原子,其形状酷似太空船(见下图)。有关C50Cl10的说法不正确的是
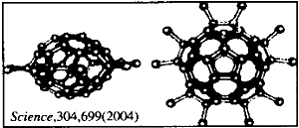
A.C50Cl10摩尔质量为955g·mol-1 B.C50Cl10晶体是原子晶体
C.C50Cl10分子中含有25个碳碳双键 D.C50Cl10分子中共用电子对数目为105
8.氯胺是长效缓释有机氯消毒剂,其杀菌能是一般含氯消毒剂的4-5倍,有关氯胺(NH2Cl)
的说法不正确的是
A.氯胺在水中水解产物最初产物为NH2OH(羟氨)和HCl
B.加入足量FeI2和少许淀粉溶液,很可能会显蓝色
C.氯胺的消毒原理与漂白粉相似
D.氯胺与浓盐酸混合可产生氯气
7.下列反应的离子方程式正确的是
A.Fe3O4与稀硝酸反应:Fe3O4+8H+ Fe2++2Fe3++4H2O
Fe2++2Fe3++4H2O
B.电解饱和食盐水:2Cl-+2H2O Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
C.Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++2HCO3-+2OH- CaCO3↓+CO32-+2H2O
CaCO3↓+CO32-+2H2O
D.Na2S溶液呈碱性:S2-+2H2O H2S+2OH-
H2S+2OH-
6.中学化学教材中提供了不少数据(图表)。下列为某同学利用相关数据作出推理和判断的依据,其中不正确的是
A.依据中和热的数据,推算一定量的H2S04和NaOH的稀溶液反应的反应热
B.依据沸点的数据判断将两种互溶的液态混合物用蒸馏的方法分离开来的可能性
C.依据相对分子质量的大小,判断组成和结构相似的物质的熔、沸点的高低
D.用键能大小的数据,判断分子的稳定性
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com