
题目列表(包括答案和解析)
5.科学家致力于二氧化碳的“组合转化”技术研究,把过多的二氧化碳转化为有益于人类的物质。如将CO2与H2混合,在一定条件下以1:3的比例发生反应,生成某种重要的化工原料和水。该化工原料可能是
A.烷烃 B.烯烃 C.炔烃 D.芳香烃
4.下列物质提纯的方法正确的是
A.除去乙烷中的乙烯:将混合气体依次通过盛有足量酸性KMnO4溶液和浓硫酸的洗气瓶
B.除去乙酸中的乙醇:向混合液中加入生石灰后蒸馏即可
C.除去KCl溶液中的K2CO3:加入过量HCl溶液后再加入NaOH溶液调节溶液至中性
D.除去甲苯中的苯酚:在混合物中加入足量的NaOH溶液,振荡、静置、分液
3.生活中遇到的某些问题,常常涉及到化学,下列叙述正确的是
A.用聚氯乙烯薄膜包装蔬菜、水果及熟食等,不会影响人体健康
B.铅笔芯和铅球的主要成分都是铅
C.被蜂蚁蜇咬会感觉痛痒难忍,若在患处涂抹稀氨水或碳酸氢钠溶液,能减轻症状
D.废旧电池必须进行集中处理的主要原因是回收其中的石墨电极
2.据报道,科学家使用普通氧分子和带正电的氧离子制造出了由4个氧原子组成的O4分子,并用质谱仪探测到它的存在。你认为这种氧分子是
A.氧元素的一种同位素
B.臭氧的同素异形体,其相对分子质量为64
C.一种比O2更稳定的新的氧化物
D.与O2互为同分异构体
1.2004年诺贝尔化学奖授予美国和以色列的三位科学家,以表彰他们在蛋白质降解的研究中取得的成果。下列关于蛋白质的说法中错误的是
A.蛋白质属于天然有机高分子化合物,没有蛋白质就没有生命
B.HCHO溶液或酒精可使蛋白质变性
C.蛋白质的变性是物理变化
D.可以采用多次盐析或多次渗析的方法分离、提纯可溶性蛋白质
24.(11分)铜是重要的工业原材料,现有Cu、Cu2O和CuO组成的混合物,某研究性学习小组为了探究其组成情况,向混合物中加入100mL0.6moL/LHNO3溶液刚好使其溶解,同时收集到224mLNO气体(标准状况)。请回答下列问题:
(1)写出Cu2O跟稀硝酸反应的化学方程式 ;
(2)产物中硝酸铜的物质的量 mol;
(3)如混合物中含0.01 molCu,则其中Cu2O、CuO的物质的量分别是 mol、 mol;
(4)如混合物中Cu的物质的量为X,则X的取值范围为 。
23.(7分)已知X是一种碱式盐,H是常见金属单质,F、I是常
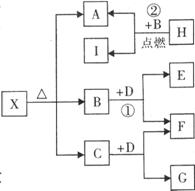 见非金属单质,E、G都是工业上重要的碱性物质,它们有右
见非金属单质,E、G都是工业上重要的碱性物质,它们有右
图所示的关系。
试回答下列问题:
(1)G的化学式为: 。
(2)写出下列反应的化学方程式
① ,
② 。
(3)X在医药上用作解酸剂,与盐酸作用时,生成B的物质
的量与消耗盐酸的物质的量之比为3:8,则X的化学
式为: 。
22.(7分)A、B、C、D均为短周期元素。A、B可形成两种液态化合物,其最简式分别为BA和B2A。A与D可形成气态化合物DA、DA2。A、B、D可组成离子化合物,该晶体化学式为B4A3D2,其水溶液呈弱酸性。B与D可形成一种极易溶于水的碱性气体X。B与C可形成极易溶于水的酸性气体Y。已知X分子与B2A分子中的电子数相等。Y分子与最简式为BA的分子中的电子数相等。请回答:
(1)写出元素的名称:A ,C 。
(2)Y分子是 分子(填极性和非极性)。
(3)写出实现下列转化的化学反应方程式并标明电子转移的方向和数目:
C2+(BA)n→A2
(4)B4A3D2水溶液呈酸性,写出其呈酸性的离子方程式:
21.(8分)在完全满足可逆反应:2H2O(g)  2H2+O2,2CO+O2
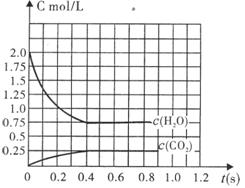
2H2+O2,2CO+O2 2CO2能顺利进行的条件下,将2molH2O(g)和2molCO充入l L密闭容器中,使其发生反应,一段时间后反应达到平衡。反应过程中部分气体浓度随时间t的变化情况如下图所示:
2CO2能顺利进行的条件下,将2molH2O(g)和2molCO充入l L密闭容器中,使其发生反应,一段时间后反应达到平衡。反应过程中部分气体浓度随时间t的变化情况如下图所示:
(1)请在图中画出c(H2)随时间t的变化曲线图;
 (2)平衡时c(O2)平为
mol/L。
(2)平衡时c(O2)平为
mol/L。
(3)欲计算出平衡时O2的浓度,除已知“H2O(g)
和CO”的物质的量外,至少需要知道平衡体
系中某两种气体的平衡浓度。这两种气体除
可以是H2O和CO2外还可以是 。
(4)在其它条件不变的情况下,若改为起始时在
容器中充入2molH2和2molCO2,则上述两反
应达到平衡时,c(O2)平= mol/L。
20.(6分)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。已知水是反应产物之一。
(1)该反应中还原剂是 ;
(2)该反应中还原产物是 ;
(3)若反应过程中转移了0.3mol电子,则生成水的质量是 g。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com