
题目列表(包括答案和解析)
29. 已知水解聚马来酸酐(HPMA)普遍用于锅炉中作阻垢剂。按下列步骤可以从不饱和烃A合成HPMA(其中D物质的结构简式为:
)
已知水解聚马来酸酐(HPMA)普遍用于锅炉中作阻垢剂。按下列步骤可以从不饱和烃A合成HPMA(其中D物质的结构简式为:
)
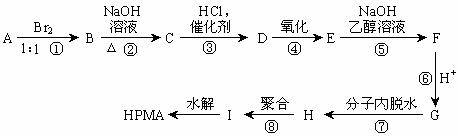
(1)写出下列物质的结构简式:A ,C ;G 。
(2)写出下列反应的化学方程式:②
⑧
(3)写出聚合物I的名称: ,合成产品HPMA的结构简式: 。
28.有机物X( )广泛存在于水果中,尤以苹果、葡萄、西瓜、山楂内为多。
(1)有机物中含有的官能团名称是 ;在一定条件下有机物X可发生化学反应的类型有 (填序号);
A.水解反应 B.取代反应 C.加成反应 D.消去反应 E.加聚反应 F.中和反应
(2)下列物质与X互为同分异构体的是 (填序号);
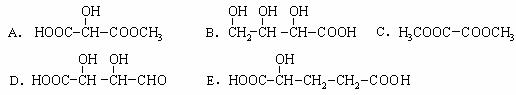
(3)写出X与金属钠发生反应的化学方程式: ;
(4)写出X与氧气在铜作催化剂加热的条件下发生反应所得的可能产物的结构简式 。
27. 某同学设计了下图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:
某同学设计了下图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:
(1)若A为浓氨水,B为烧碱,C中盛有AlCl3溶液,
旋开活塞E,足够长时间后,观察到C中的现象
为 ,C中发生反应的离子方程
式为 ;
(2)若A为30%的H2O2溶液,B为二氧化锰,C中盛
有氢硫酸饱和溶液,旋开活塞E后,观察到C中
的现象为 ,C中发生反应的
化学方程式为 ;
(3)利用上述装置还可以验证物质的性质,如设计证明氧化性:KMnO4 >Cl2 >Br2,则A中加浓盐酸,B中加 ,C中加 ,观察到C中的现象是 ;
(4)请利用上述装置自行设计有机实验,写出实验所用的试剂,简述C中的实验现象及实验的目的。A中加 ,B中加 ,C中加 ,观察到C中的现象是 ,实验目的是 。
26.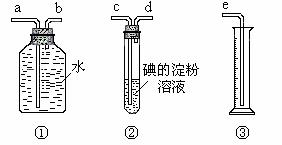 某化学兴趣小组模拟测定工业原料气SO2、N2、O2混合气体中SO2含量,选用了下列简易实验装置:
某化学兴趣小组模拟测定工业原料气SO2、N2、O2混合气体中SO2含量,选用了下列简易实验装置:
(1)若原料气从左向右流向时,上述装置组装连接的顺序是:
原料气→ (填a、b、c、d、e)。
(2)装置②中发生反应的离子方程式为 ;当装置②中出现 现象时,立即停止通气。若此时没有及时停止通气,则测定的SO2含量 (选填“偏高”、“偏低”或“不受影响”)。
(3)你认为下列试剂中,可以用来代替试管中的碘的淀粉溶液的是 (填编号)
A.酸性KMnO4溶液 B.NaOH溶液 C.溴水 D.氨水
(4)若碘溶液的浓度为0.05mol/L、体积为20mL,收集到的N2和O2的体积为297.6mL(已折算为标准状况的体积)。SO2的体积分数为 。
25.
(1)在短周期元素中,属于非金属元素但具有某种金属性,可做半导体材料的是 ;地壳中含量最高的是 ;形成化合物种类最多的是 (用化学符号表示)。
(2)在短周期元素中,某元素原子的核外p电子数比s电子数少1,则该元素的符号是 ,其单质的电子式为 。
(3)如果将十五种短周期主族元素按原子半径由小到大排成一横行,则该横行的第十三列 元素是 (填元素符号),这种元素的单质在空气中不易腐蚀,其原因是 。
(4)下图列出元素周期表中部分主族元素:
|
|
|
|
|||||
|
① |
② |
|
|
|
|
|
|
|
|
③ |
④ |
|
|
|
|
|
某些不同族元素的性质也有一定的相似性,如上表中元素④与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
。
24.在一容积为2L且容积不变的密闭容器中加入适量碳粉和0.2molH2O。在800 °C条件下,经20s后达到如下化学平衡:C(s) +H2O(g)  CO(g) + H2(g) + Q。已知达到平衡(I)时,CO为0.12mol。试回答:
CO(g) + H2(g) + Q。已知达到平衡(I)时,CO为0.12mol。试回答:
(1)写出上述反应平衡常数的表达式: ;
(2)若用υ(H2O)表示该反应前20s内的平均速率,则υ(H2O)= ;
(3)若在上述平衡混合物中加入少量Na2O固体,并在此温度下再次达到新的平衡(II),则平衡时H2的物质的量 (填“增大”、“减小”、“不变”)。理由是: ;
(4)若向上述平衡(I)的混合物中再充入a mol H2( a < 0.12 ),在相同条件下达到新的平衡(III),此时,CO的物质的量n的取值范围是 。
23.储氢纳米碳管研究成功体现了科技的进步。但用电弧法合成的碳纳米管常伴有大量的杂质--碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯。其反应式为:
C + K2Cr2O7 + H2SO4→ CO2 + K2SO4 + Cr2(SO4)3 + H2O
(1)完成并配平上述反应的化学方程式并标出电子转移方向与数目;
(2)此反应的氧化剂是 ,氧化产物是 ;
(3)H2SO4在上述反应中表现出来的性质是 (填选项编号)
A.酸性 B.氧化性 C.吸水性 D.脱水性
(4)上述反应中若产生0.1mol CO2气体,则转移电子的物质的量是 mol。
22.在一定温度下,向饱和的烧碱溶液中加入一定量的Na2O2,充分反应后恢复到原来温度,下列说法中正确的是…………………………………………………………………( )
A.溶液的pH不变,有H2放出 B.溶液中Na+ 数目减小,有O2放出
C.溶液的pH增大,有O2放出 D.溶液中c(Na+ )增大,有O2放出
第Ⅱ卷(共84分)
21.向100mL 0.1mol/L的NaOH溶液中通入224mL(标准状况下)CO2气体,恰好完全反应,则所得溶液中粒子浓度关系正确的是…………………………………………( )
A.c (Na+ )=c (HCO3- )+c (H2CO3)+c (CO32- )
B.c (Na+ )>c (HCO3- )>c (H + )>c (CO32- )>c (OH - )
C.c (Na+ )+c (H + )=c (HCO3- )+c (OH - )+c (CO32- )
D.c (H + )+c (H2CO3)=c (CO32- )+c (OH - )
20.NA代表阿佛加德罗常数,以下说法正确的是……………………………………( )
A.在标准状况下,2.24L苯中含有0.6mol碳原子
B.1L pH=1的硫酸溶液中含有0.2NA个氢离子
C.在1L 0.1 mol/L的HCOOH溶液中,所含HCOO-和HCOOH粒子数之和为0.1NA个
D.标准状况下,以任意比例混合的乙烷和乙烯混合物22.4L,所含分子数约为NA个
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com