
题目列表(包括答案和解析)
2、如图右图所示,在一U型管中装入含有紫色石蕊的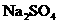 试液,通直流电,
试液,通直流电,
一段时间后U型管内会形成一个倒立的三色 “彩虹”,从左到右颜色的次序是
A、蓝、紫、红 B、红、蓝、紫
C、红、紫、蓝 D、紫、红、蓝
1、(2005上海)关于如图所示装置的叙述,正确的是( )
A、铜是阳极,铜片上有气泡产生
B、铜片质量逐渐减少
 C、电流从锌片经导线流向铜片
C、电流从锌片经导线流向铜片
D、氢离子在铜片表面被还原
2、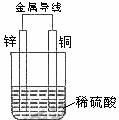 命题趋向:电化学的内容是历年高考的重要知识点之一,主要以选择题的形式出现,考查的内容有:原电池、电解池、电镀池的电极名称及根据总反应方程式书写原电池各电极反应式、根据电解时电极变化判电极材料或电解质种类、根据反应式进行计算、与电解池及电镀池精炼池进行综合考查、提供反应方程式设计原电池、提供电极材料电解质溶液进行原电池是否形成的判断、与图像进行结合考查各电极上质量或电解质溶液溶质质量分数的变化等。其中原电池的工作原理及其电极反应式的书写、电解产物的判断和计算是高考命题的热点。
命题趋向:电化学的内容是历年高考的重要知识点之一,主要以选择题的形式出现,考查的内容有:原电池、电解池、电镀池的电极名称及根据总反应方程式书写原电池各电极反应式、根据电解时电极变化判电极材料或电解质种类、根据反应式进行计算、与电解池及电镀池精炼池进行综合考查、提供反应方程式设计原电池、提供电极材料电解质溶液进行原电池是否形成的判断、与图像进行结合考查各电极上质量或电解质溶液溶质质量分数的变化等。其中原电池的工作原理及其电极反应式的书写、电解产物的判断和计算是高考命题的热点。
课堂训练
1、 方法与技巧
在复习电化学时,可通过对“三池”如下问题的思考,找出共性,明确差异,挖掘规律,突破难点。①这三种装置有何相似和相异的特点?②“三池”对电极有何要求?为什么?③“三池”对电解质溶液有何要求?为什么?④阴、阳离子放电顺序是怎样确定的?⑤怎样根据离子放电顺序和电极材料来分析“三池”反应的产物?⑥怎样根据离子放电顺序和电极反应判断电解质溶液PH的变化?⑦怎样用电极反应式和总反应方程式来表示“三池”的变化原理?这两种表示式如何进行书写变换?⑧“三池” 装置中,怎样判断正、负极或阴、阳极?书写电极反应式的技巧是将电池总反应式中失去电子的反应定为负极反应,得到电子的反应定为正极反应,具体的化学式形式根据总反应式和溶液的酸碱性进行判断。
22.化合物A含硫(每个分子只含一个硫原子)、氧以及一种或几种卤素;少量A与水反应可完全水解而不被氧化或还原,所有反应产物均可溶于水;将A配成水溶液稀释后分成几份,分别加入一系列0.1mol/L的试剂,现象如下:
①加入硝酸和硝酸银,产生白色沉淀 ;
②加入氯化钡溶液,无沉淀生成;
③溶液经酸化后加入高锰酸钾溶液,紫色褪去,再加入硝酸钡溶液,产生白色沉淀;
(1)由此判断组成该化合物的元素中,可能存在的卤素有 ,A与水反应后生成的溶液中含有的离子可能有 。
(2)要确定该化合物的分子式,称取11.90g A溶于水稀释至250.0mL,取25.00mL溶液加入足量的高锰酸钾溶液和硝酸钡溶液,使沉淀完全,沉淀经洗涤、干燥后称重,为2.33g,试确定A的化学式,写出计算过程。
高三 十校联考 第一次考试
21.(14分)我国第二代身份证采用的是具有绿色环保性能的PETG新材料,PETG新材料可以回收再利用,而且对周边环境不构成任何污染。这一材料是由江苏华信塑业发展有限公司最新研发成功的新材料,并成为公安部定点产地。PETG的结构简式为:
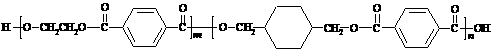
EG TPA CHDM TPA
已知:Ⅰ.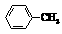
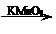

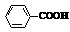
Ⅱ.RCOOR1+R2OH→RCOOR2+R1OH (R、R1、R2表示烃基)
这种材料可采用下列合成路线
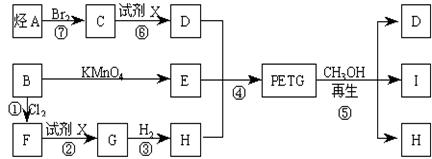 试回答下列问题:
试回答下列问题:
(1)反应②、⑥中加入的试剂X是_____________________;
(2)⑤的反应类型是________________;
(3)写出结构简式:B______________________,I________________________;
(4)合成时应控制的单体的物质的量n(D):n(E):n(H)=_____:_______:_______(用m、n表示)。
(5)写出化学方程式:
反应③:____________________________________________________;
反应⑥:_____________________________________________________。
20.(12分)硫酸钡是惟一无毒的钡盐,工业上以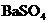 等为原料通入下列流程反应可以制备锌钡白和过氧化氢:
等为原料通入下列流程反应可以制备锌钡白和过氧化氢:
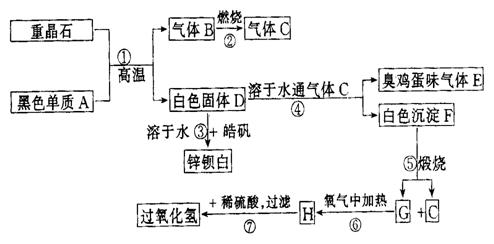
(1)上述流程中共有7个化学反应,其中_______(填编号)属于氧化还原反应.
(2)写出物质H的电子式_____________.
(3)写出下列化学反应方程式:
反应①:__________________________________________________________.
反应③:__________________________________________________________.
反应④:__________________________________________________________.
反应⑦:__________________________________________________________.
19.(6分)元素周期表是20世纪科学技术发展的重要理论依据之一,是我们学习化学的重要工具。假设NH4+是“元素”NH4的阳离子,则“元素” NH4在周期表中的位置应该是第 周期第 族;“元素” NH4的单质常温常压下应为 (填“固”、“液”或“气”)体;熔点 (填“高”或“低”) ; (填“能”或“不能”)导电;NH4的碳酸盐应 (填“易”或“不易”)溶于水。
18.(6分)氯、溴、碘同属于周期表中的VII A族,在上个世纪,人们很早就制得高碘酸及其盐,但得不到含+7价溴的化合物,1968年,化学家用发现不久的XeF2和KBrO3首先制得纯净的KBrO4晶体。
(1)高碘酸盐(IO65-)能在酸性条件下将Mn2+氧化为MnO4-(本身被还原成I03-),其反应平稳而迅速,写出离子反应方程式: 。
(2)在25℃,已知pH=2的高碘酸溶液与pH=12的NaOH溶液等体积混合,所得混合液显酸性;0.01mol·L-1的碘酸或高锰酸溶液与pH=12的NaOH溶液等体积混合,所得混合液显中性。则高碘酸是 ;高锰酸是 (填“强酸”或“弱酸”)。
(3)写出XeF2和含KOH、KBrO3的水溶液反应得到KBrO4的离子方程式 。
17.某研究性学习小组的一个课题是“NO2能否支持木条的燃烧?”由于实验室中没有现成的NO2气体,该小组的同学设计了两个方案(忽略N2O4的存在,图中铁架台等夹持仪器均已略去):
Ⅰ.实验装置如下图1所示

图1 图2
(1)浓硝酸受热分解的化学方程式是 。
(2)实验开始后木条上的火星逐渐熄灭,有的同学得出“NO2不能支持木条的燃烧”的结论。你认为这一结论是否正确? (填“正确”或“不正确),理由是 。
Ⅱ.实验装置如上图2所示
(1)硝酸铜固体加热分解的产物有氧化铜、二氧化氮和氧气,该反应的化学方程式是 。
(2)当集气瓶中充满红棕色气体时,木条复燃了,有的同学得出“NO2能支持木条的燃烧”的结论。你认为这一结论是否正确? (填“正确”或“不正确”),理由是 。
Ⅲ.为了更直接说明“NO2能否支持木条的燃烧”这一问题,请你重新设计一个简单的实验方案,简述实验原理和主要操作。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com