
题目列表(包括答案和解析)
15.在元素周期表短周期中的X和Y两种元素可组成化合物XY3,下列说法正确的是( )
A.XY3晶体一定是离子晶体 B.若Y的原子序数为n,X的原子序数一定是n土4
C.X和Y可属于同一周期,也可属于两个不同周期 D.X和Y可属于同一主族
14.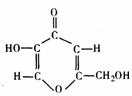 从米曲霉中分离出的曲酸是-种新型添加剂,其分子结构如下图。曲酸具有抗氧化性(保护其它物质不被空气氧化),在化妆、医药、食品、农业等方面具有广泛的应用前景。下列关于曲酸的说法正确的是
从米曲霉中分离出的曲酸是-种新型添加剂,其分子结构如下图。曲酸具有抗氧化性(保护其它物质不被空气氧化),在化妆、医药、食品、农业等方面具有广泛的应用前景。下列关于曲酸的说法正确的是
A. 曲酸是一种芳香族化合物 B.曲酸是一种羧酸,难溶于水
C. 曲酸分子中的所有原子不可能都在同一平面上
D. 曲酸被空气中的O2氧化时,反应发生在环上的羟基部位
13.表示0.1mol·L-1NaHCO3溶液有关微粒浓度的关系正确的是( )
A.c(Na+)+c(H+) c(HCO3-)+c(CO32-)+c(OH-) B.c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
C.c(Na+)>c(HCO3-)>c(CO32-)>c(H+)>c(OH-) D.c(OH-)=c(H+)+c(H2CO3)+c(HCO3-)
12.某恒温恒容的容器中,建立如下平衡:2A(g) B(g),若在相同条件下分别再向容器中通入一定量的A气体或B气体,重新达到平衡后,容器内A的体积分数比原平衡时
B(g),若在相同条件下分别再向容器中通入一定量的A气体或B气体,重新达到平衡后,容器内A的体积分数比原平衡时
A.都增大 B.都减小
C.前者增大后者减小 D.前者减少后者增大
11.体积相同,H+离子浓度均为0.1 mol/L的CH3COOH溶液、盐酸,分别加水稀释m倍、n倍,溶液的pH都变成5,则m与n的关系为( )
A.m>n B.m=n C.m<n D.无法确定
10.下列离子方程式书写正确的是( )
A.等体积、等物质的量浓度的Ba(OH)2溶液与NaHCO3溶液混合:
Ba2++2OH-+2HCO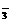 ====BaCO3↓+CO
====BaCO3↓+CO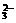 +H2O
+H2O
B.次氯酸钙溶液中通入少量SO2气体:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
C.NH4HCO3溶液与足量NaOH溶液混合:
NH +HCO
+HCO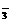 +2OH-= NH3·H2O+CO
+2OH-= NH3·H2O+CO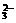 +H2O
+H2O
D.明矾溶液中加过量Ba(OH)2溶液
2A13++3SO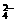 +3Ba2++6OH-=3BaSO4↓+2Al(OH)3↓
+3Ba2++6OH-=3BaSO4↓+2Al(OH)3↓
9..设NA表示阿伏加德罗常数,下列说法不正确的是( )
A.a g H2和b g He在同温同压时的体积比为a∶2b
B.2 L 0.1 mol/L的H2S溶液中,含有的H2S分子数小于0.2NA
C.78 g Na2O2与水充分反应,转移的电子数目为NA
D.1 mol FeCl3跟水反应完全转化成氢氧化铁胶体后,生成胶体粒子的数目为NA
8.A、B两元素的原子分别得到2个电子形成稳定结构时,A放出的能量大于B放出的能量;C、D两元素的原子分别失去一个电子形成稳定结构时,D吸收的能量大于C吸收的能量。A、B、C、D间形成最稳定化合物的化学式为( )
A.D2A B.C2B C.D2B D.C2A
7.1g氢气完全燃烧生成液态水放出142.9kJ的热量, 表示该反应的热化学方程式中, 正确的是 ( )
A、2 H2(g) + O2(g) = 2 H2O(l);△H =-142.9kJ/mol
B、2 H2(g) + O2(g) = 2 H2O(g);△H =-571.6kJ/mol
C、2 H2 + O2 = 2 H2O;△H =-571.6kJ/mol
D、H2(g) +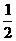 O2(g)
= H2O(l);△H =-285.8kJ/mol
O2(g)
= H2O(l);△H =-285.8kJ/mol
6.已知氢化锂(LiH)属于离子晶体,LiH跟水反应可以放出氢气,下列叙述正确的是( )
A LiH的水溶液呈中性 B LiH是一种强氧化剂
C. LiH中的氢离子可以被还原成氢气 D. LiH中氢离子与锂离子核外电子排布相同
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com