
题目列表(包括答案和解析)
7、在下列各组固体混合物中,等质量的分为两份,将其中一份隔绝空气加强热引发反应,然后分别将反应前与反应后的固体加入足量的稀硫酸中,在相同条件下所得气体的体积不相同的是 (不考虑生成气体在水中溶解)
A.Al和S B.Mg和S C. Al和Fe3O4 D. Al和FeO
6. 下列排列顺序正确的一组是
A.半径:Fe(OH)3胶粒>I->K+>Na+ B.熔沸点:HF<HCl<HBr<HI
C.还原性:Fe3+>Cu2+>Fe2+>Zn2+ D.热稳定性:H3PO4<H2SO3<H2SiO3<H2SO4
5.左表为烯类化合物与溴发生加成反应的相对速率
(以乙烯为标准),而下列化合物与氯化氢加成,取代基对速率的影响与表中规律相似。其中反应速率最慢的是:
A.(CH3)2C=C(CH3)2 B.CH2CH=CHCH3
C.CH2=CH2 D.CHCl=CHCl
4.下列实验操作中,先后顺序正确的是
A.稀释浓硫酸时,先在烧杯中加入一定体积的浓硫酸,后注入蒸馏水
B.为测定硫酸铜晶体的结晶水含量,称样时,先称取一定量的晶体,后放入坩锅中
C.为检验酸性溶液中的Cl-和SO42-,先加硝酸银溶液,滤去沉淀后加硝酸钡溶液
D.在制取干燥纯净的氯气时,先使氯气通过水(或饱和食盐水),后通过浓硫酸
|
烯类化合物 |
相对速率 |
|
(CH3)2C=CHCH3 |
10.4 |
|
CH2CH=CH2 |
2.03 |
|
CH2=CH2 |
1.00 |
|
CH2=CHBr |
0.04 |
3. 目前,人类已经发现的非金属元素除稀有气体元素外共16种。下列对这16种非金属元素的判断正确的有 ①都是主族元素,最外层电子数都大于3 ②单质形成的晶体都为分子晶体③氢化物常温下都是气态,所以又叫做气态氢化物 ④氧化物常温下都可以与水反应生成酸
A.只有①②正确 B.只有①③正确 C.只有③④正确 D.①-④都不正确
2.固体电解质又称离子导体,在一定温度范围内具有很强的导电性。固体电解质虽然是固体,但却像电解质溶液一样以离子为导电载体。下列物质能作为固体电解质的是
A.银 B.碳素钢 C.硝酸钾晶体 D.水晶
1.神舟六号成功的发射,第二次实现了毛泽东当年立下的“敢上九天揽月”的雄心壮志。长征2号火箭承担运载“神六”的使命。氢化锂、氘化锂、氚化锂可以作为起动长征2号火箭(CZ2F)发射的优良炸药,下列说法正确的是
A.等物质的量LiH , LiD, LiT中所含质子数不相同
B.它们都是氧化剂
C.H、D、T之间互称同素异形体
D.它们都是强还原剂
现代仪器分析有机化合物的分子结构有以下两种方法。
方法一:用核磁共振仪可以测定有机分子里不同化学环境的氢原子及其相对数量。
现测出A的核磁共振氢谱有5个峰,其面积之比为1:2:2:2:3。
方法二:利用红外光谱仪可初步检测有机化合物中的某些基团,现从A的红外光谱测得其结构中C-H、C=O、C-0-C、C-C和 -C等键与基团,已知A分子中只含一个苯环,且苯环上只有一个取代基,A与NaOH溶液共热的两种生成物均可用于食品工业,试回答下列问题:
-C等键与基团,已知A分子中只含一个苯环,且苯环上只有一个取代基,A与NaOH溶液共热的两种生成物均可用于食品工业,试回答下列问题:
(1)A的分子式为
(2)A的结构简式为
(3)试写出A与NaOH溶液共热的反应化学方程式:
(4)A的芳香类同分异构体有多种,请按要求写出其中两种结构简式:
①分子中不含甲基的芳香酸:
②遇FeCl3显紫色且苯环上只有两个取代基的芳香醛:
符合上述条件的芳香醛共有 种
29.(10分)元素周期表反映了元素性质的周期性变化规律。请根据短周期元素在周期表中的位置、结构和相关性质,回答下列问题:
⑴ 短周期元素中,原子最外层电子数和电子层数相等且核电荷数最大的元素R的电子排布式是 。
 ⑵ 第二周期元素中,除Be、B、Ne三种元素外,其他元素的氢化物沸点如下表1所示,其中A的化学式为
;请你按沸点由低到高的顺序写出四种氢化物的分子式 :
⑵ 第二周期元素中,除Be、B、Ne三种元素外,其他元素的氢化物沸点如下表1所示,其中A的化学式为
;请你按沸点由低到高的顺序写出四种氢化物的分子式 :
 ,其中E沸点最低的原因是
,第三周期元素单质的熔点(℃)变化如下图I所示,其中h元素单质的晶体类型是
。
,其中E沸点最低的原因是
,第三周期元素单质的熔点(℃)变化如下图I所示,其中h元素单质的晶体类型是
。
⑶ 第二、第三周期的某些元素中能形成具有图II所示的结构单元的单质丙和化合物丁,丙和丁的晶体类型相同,且丙与丁在高温时能发生置换反应。若该反应中丙被破坏了1 mol共价键,则参加反应的丁的质量为 g。
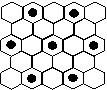 (4)元素丙的某种单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,此单质与熔融的钾相互作用,形成某种青铜色的物质(其中的元素钾用“●”表示),原子分布如图所示,该物质的化学式为
___
。
(4)元素丙的某种单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,此单质与熔融的钾相互作用,形成某种青铜色的物质(其中的元素钾用“●”表示),原子分布如图所示,该物质的化学式为
___
。
27.(10分)石油资源紧张曾是制约我国轿车业发展,尤其是制约轿车进入家庭的重要因素。据2001年5月28日某媒体报道,中国宣布将推广“车用乙醇汽油”。所谓乙醇汽油就是在汽油中加入适量乙醇混合而成的一种燃料。
(1)汽油是由石油分馏和裂化所得的低沸点烃,其分子中的碳原子数一般在5~11的范围内。如戊烷,其分子式为C5H12,试写出它的一氯代物只有一种结构的某同分异构体的结构简式 。
(2)乙醇燃烧时如果氧气不足,可能还有CO生成。请写出乙醇不完全燃烧生成CO2、CO、H2O(其中生成的CO2与CO的质量比为11∶14)的化学反应方程式
(3)某种天然高分子化合物X在酶的作用下可生成一种化合物Y,Y在另一种酶的作用下可生成乙醇,试写出Y的结构简式 ,并根据Y的结构特点指出它可能发生的化学反应 。
(4)工业上还可以用石油裂解的重要产品--乙烯来制取乙醇,请写出由乙烯制乙醇的化学反应方程式:
(5)车用乙醇汽油称为环保燃料,其原因是
26.(10分)下图是从铝土矿X中提取其主要成分的两种相互结合的方案,已知A为红褐色沉淀,D、F为白色沉淀,F经两次失水转化为G,Ⅰ、Ⅱ、Ⅲ、Ⅳ是相同的操作。
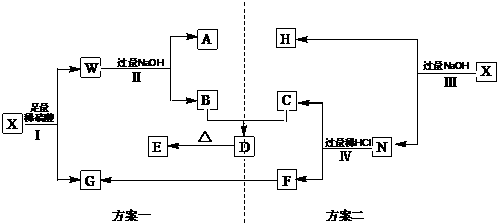
(1) X的主要成分是____________、_____________、 (用氧化物的化学式表示)。
(2)F的化学式是__________。
(3)写出下列转化的离子方程式:
B+C→D__________________________________________________
(4)要使X的利用率最高,则方案一与方案二所取矿石的质量比为__________。
(5)两方案结合的优点是
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com