
题目列表(包括答案和解析)
2.2004年,美国科学家通过“勇气”号太空车探测出水星大气中含有一种称为硫化羰(化学式为COS)的物质,己知硫化羰的结构与二氧化碳相似,但能在氧气中完全燃烧,下列有关硫化羰的说法中正确的是
A.硫化羰是酸性氧化物 B.硫化羰是由极性键构成的非极性分子
C.硫化羰可用做灭火剂 D.硫化羰在氧气中完全燃烧后的生成物是CO2和SO2
28.(10分)
A.2005年11月13日,吉林石化公司双苯厂发生的爆炸事件,使大量的苯胺及其生产原料(苯、硝基苯等)进入松花江,造成松花江水体被严重污染。
(1)下列有关叙述正确的是 (填序号)。
A.进入水体的苯会溶于水,造成鱼类大量中毒死亡
B.进入水体的硝基苯会浮在水面上迅速流向下游
C.工业上用硝基苯制取苯胺是氧化反应
D.苯和硝基苯的混合物可通过蒸馏的方法将其分离
(2)自来水厂对上述受污染的江水进行净化处理,采用的经济有效的方法是 (填序号)。
A.分液 B.过滤 C.用活性炭吸附有毒物质 D.加热蒸发
(3)磺胺类药物,常用于肠道抗菌感染的治疗,工业上可用苯为原料通过下列反应制得磺胺。(转化关系中-H2O、-HCl、-CH3COOH分别表示反应中有H2O、HCl、CH3COOH生成)
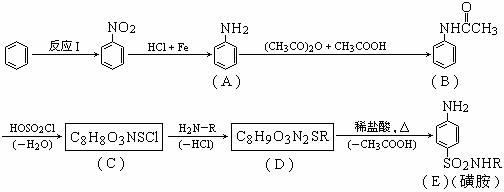
①反应Ⅰ的反应类型是 反应。
②分析上述反应过程中所提供的有关信息,写出C的结构简式: 。
③写出D → E的化学方程式:
。
B.在极性分子中,正电荷重心同负电荷重心间的距离称偶极长,通常用d表示。极性分子的极性强弱同偶极长和正(或负)电荷重心的电量(q)有关,一般用偶极矩(μ)来衡量。分子的偶极矩定义为偶极长和偶极上一端电荷电量的乘积,即μ=d·q。试回答以下问题:
(1)HCl、CS2、H2S、SO2四种分子中μ=0的是 ;
(2)对硝基氯苯、邻硝基氯苯、间硝基氯苯,3种分子的偶极矩由大到小的排列顺序是:
;
(3)实验测得:μPF3=1.03、μBCl3=0。由此可知,PF3分子是 构型,
BC13分子是 构型。
(4)治癌药Pt(NH3)2Cl2具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个角上。已知该化合物有两种异构体,棕黄色者μ>0,淡黄色者μ=0。试画出两种异构体的构型图,并比较在水中的溶解度。
构型图:
淡黄色者 ,棕黄色者 ;
在水中溶解度较大的是 。
高三毕业班高考模拟考试
27.(10分)
(1)苯氯乙酮是一具有荷花香味且有强催泪作用的化学试剂,它的结构简式如右图所示:
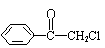 则苯氯乙酮不可能具有的化学性质是
(填字母序号)
则苯氯乙酮不可能具有的化学性质是
(填字母序号)
A、加成反应 B、取代反应 C、消去反应
D、水解反应 E、银镜反应
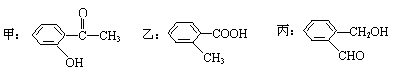
(2)今有化合物
①请写出丙中含氧官能团的名称
②请判别上述哪些化合物互为同分异构体:
③请按酸性由强至弱排列甲、乙、丙的顺序:
(3)由丙烯经下列反应可制得F、G两种高分子化合物,它们都是常用的塑料。
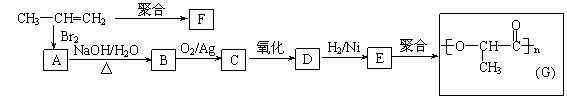
①丙烯分子中,最多有 个原子在同一个平面上;
②聚合物F的结构简式是 ;
③B转化为C的化学方程式是 ;
④在一定条件下,两分子E能脱去两分子水形成一种六元环状化合物,该化合物的结构简式
是 。
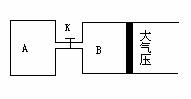
26.(10分)如图所示,当关闭K时,向A中充入4molX、14molY,向B中充入2molX、7molY,起始时V(A)=V(B)=a升,在相同温度和有催化剂存在的条件下,两容器各自发生下列反应:
2X(g)+2Y(g)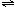 Z(g)+2W(g);△H<0达到平衡(Ⅰ)时,B中密度变为原来的
Z(g)+2W(g);△H<0达到平衡(Ⅰ)时,B中密度变为原来的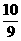 ,试回答:
,试回答:
(1)B中X的转化率α(X)B为 ,Y的转化率α(Y)A为 。
 (2)A中Z和B中的W物质的量的比较:
(2)A中Z和B中的W物质的量的比较:
n(Z)A n(W)B (填<、>、或=)
(3)打开K,过一段时间重新达平衡(Ⅱ)时,B的体
积为 升(用含a的代数式表示,连通管中气
体体积不计)
(4)在温度不变的情况下,要使B容器恢复原来反应前的体积,可采取的措施是
。
25.(10分)聚合氯化铝晶体的化学式为[Al2(OH)nCl6-n·xH2O]m,它是一种高效无机水处理剂,它的制备原理是调节增大AlCl3溶液的pH,通过促进其水解而结晶析出。其制备原料主要是铝加工行业的废渣--铝灰,它主要含Al2O3、Al,还有SiO2等杂质。聚合氯化铝生产的工艺流程如下:

(1)搅拌加热操作过程中发生反应的离子方程式 ;
。
(2)生产过程中操作B和D的名称均为 (B和D为简单操作)。
(3)反应中副产品a是 (用化学式表示)。
(4)生产过程中可循环使用的物质是 (用化学式表示)。
(5)调节pH至4.0~4.5的目的是 。
(6)实验室要测定水处理剂产品中n和x的值。为使测定结果更准确,需得到的晶体较纯净。
生产过程中C物质可选用 。
A.NaOH B.Al C.氨水 D.Al2O3 E.NaAlO2
0.05 mol·L-1AgNO3溶液中的溶解度分别为S1、S2、S3、S4,则S1、S2、S3、S4由大到小的
顺序为 。
(2)下列曲线分别表示元素的某种性质与核电荷的关系(Z为核电荷数,Y为元素的有关性质)。把与下面元素有关的性质相符的曲线标号填入相应的空格中:
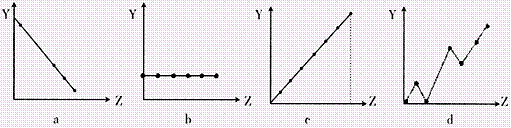
①ⅡA族元素的价电子数 ;
②第3周期元素的最高化合价 ;
③F-、Na+、Mg2+、Al3+的离子半径 。
(3)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3:4;M元素原子的最外层电子数与电子层数之比为4:3;N-、Z+、X+离子的半径逐渐减小;化合物XN常温下为气体。据此回答:
①N的最高价氧化物的水化物的化学式为 。
②化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1:1:1,A溶液中水的电离程度比B溶液中
水的电离程度小。则化合物A中的化学键类型为 ,
B的化学式为 。
③工业上制取单质M的化学方程式为 。
24.(10分)(1)若AgC1在水中、0.01 mol·L-1 CaCl2溶液中、0.01 mol·L-1 NaCl溶液中及
23.(10分)氧化铜是一种黑色固体,可溶于稀硫酸。某同学想知道是稀硫酸的哪种粒子(H2O,H+,SO42-)能使氧化铜溶解。请你和他一起通过如图Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动。
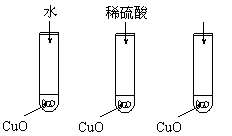 (1)某同学提出的假设是
(1)某同学提出的假设是
;
(2)通过实验Ⅰ可以证明
;
 (3)要证明另外两种粒子能否溶解氧化铜,还需要进行
(3)要证明另外两种粒子能否溶解氧化铜,还需要进行
实验Ⅱ和Ⅲ,在Ⅱ中加入稀硫酸后氧化铜溶解,则
进一步所做的确认为:在Ⅲ中先加入 ,再加入 。
(4)探究结果为 。
你认为除实验Ⅱ和Ⅲ所用的试剂外,还能溶解氧化铜的一种常见物质是 。
22.(10分)间接碘量法测定胆矾中铜含量的原理和方法如下:
已知:在弱酸性条件下,Cu2+与I-作用可生成I2,I2溶于过量的KI溶液中:I2+I-=I3-,又知氧化性:Fe3+>Cu2+>I2>FeF63-;析出I2可用c mol/LNa2S2O3标准溶液滴定,其反应为:
2S2O32-+I3-=S4O62-+3I-。
操作:准确称取ag胆矾试样(可能含少量Fe2(SO4)3),置于250 mL碘量瓶(带磨口塞的锥形瓶)中,加50 mL蒸馏水、5 mL 3 mol/LH2SO4溶液、少量NaF,再加入足量的10% KI溶液,摇匀。盖上碘量瓶瓶盖,置于暗处5 min,充分反应后,加入指示剂,用Na2S2O3标准溶液滴定至终点,共用去V mL标准溶液。回答下列问题:
⑴实验中,加KI前需加入少量NaF,其作用可能是
;
加3mol/LH2SO4溶液的作用可能是 。
⑵滴定实验中所用指示剂是 ;滴定终点的判断方法为
。
⑶本实验中用碘量瓶而不用普通锥形瓶是因为:
。
⑷硫酸铜与碘化钾反应后被还原白色的碘化亚铜沉淀,该反应的离子方程式为:
。
⑸根据本次实验结果,该胆矾试样中铜元素的质量分数ω(Cu)= 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com