
题目列表(包括答案和解析)
66. 某种有机物分子的球棍模型如右图,图中“棍”代表单键、双键或三键,不同大小的球代表不同元素的原子,且三种元素位于不同的短周期。下列关于该有机物的叙述不正确的是
某种有机物分子的球棍模型如右图,图中“棍”代表单键、双键或三键,不同大小的球代表不同元素的原子,且三种元素位于不同的短周期。下列关于该有机物的叙述不正确的是
A.有机物的化学式为C2HCl3 B.分子中所有原子在同一平面内
C.该有机物难溶于水 D.可由乙炔和氯化氢加成得到
65.下列各组数据中,前者比后者大的是
A.常温、常压下,pH=9的KOH溶液和pH=10的KCN溶液中由水电离出的OH-浓度
B.100 mL 0.1 mol·L-1的CH3COOH溶液和10 mL 1.0 mol·L-1的CH3COOH溶液中H+的数目
C.Na2CO3溶液中HCO3-和OH-的数目
D.纯水在20℃和95℃时的pH
64. 在25mL 0.1 mol·L-1 NaOH溶液中逐滴加入0.2 mol·L-1醋酸溶液,曲线如图所示,下列有关离子浓度的比较中正确的是
在25mL 0.1 mol·L-1 NaOH溶液中逐滴加入0.2 mol·L-1醋酸溶液,曲线如图所示,下列有关离子浓度的比较中正确的是
A.在A、B间任何一点,溶液中一定都有:
c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
C.在C点,c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
D.在D点,c(CH3COO-)+c(CH3COOH)=2c(Na+)
63.两种浓度不同的NaOH溶液,c(H+)分别为1.0×10-14mol·L-1和1.0×10-12mol·L-1,将这两种溶液等体积混合后,所得溶液的c(H+)约为
A.0.5×(10-14+10-12)mol·L-1 B.5×(10-15+10-11)mol·L-1
C.2.0×10-1mol·L-1 D.2.0×10-14mol·L-1
62.在温度不变的状况下,将0.1 mol·L-1 CH3COOH溶液用水稀释,对其所发生的变化,下列叙述不正确的是
A.电离常数不变 B.导电性增强 C.c(H+)减小 D.c(OH-)减小
61.下列物质的分类组合完全正确的是
 名称
名称编号 |
强电解质 |
弱电解质 |
非电解质 |
|
A |
NaNO3
|
CH3COOH |
Cl2
|
|
B |
H2SO4
|
H3PO4
|
CS2
|
|
C |
BaSO4
|
HClO4
|
C2H6
|
|
D |
H2SO3
|
Al(OH)3
|
CO2
|
60.某工业生产中发生反应:2A(g)+B(g)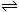 2M(g);△H<0。下列有关该工业生产的说法中正确的是
2M(g);△H<0。下列有关该工业生产的说法中正确的是
A.工业上在合成M时,一定采用高压条件,因为高压有利于M的生成
B.若物质B廉价易得,工业上一般采用加入过量的B,以提高A和B的转化率
C.工业上一般采用高温合成M,因温度越高,反应物的转化率越高
D.工业生产中常采用催化剂,因为使用催化剂可提高M的日产量
59.在一定条件下,某体积为2 L的密闭容器中发生了如下反应:3X(g)+Y(g) 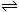 2Z(g),反应达到平衡后,X、Y、Z三者物质的量之比为325。保持其他条件不变,升温重新达到平衡时,X和Y的物质的量分别为0.9 mol和0.4 mol,则下列说法中正确的是
2Z(g),反应达到平衡后,X、Y、Z三者物质的量之比为325。保持其他条件不变,升温重新达到平衡时,X和Y的物质的量分别为0.9 mol和0.4 mol,则下列说法中正确的是
A.升温后平衡向正方向移动
B.升温重新达到平衡后Z的物质的量为0.1 mol
C.该反应的△H<0
D.升温重新达到平衡后Z的物质的量浓度为0.1 mol·L-1
58.在恒温时,一固定容积的容器内发生如下反应:2NO2(g)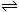 N2O4(g),达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡时,与第一次平衡相比,NO2的体积分数
N2O4(g),达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡时,与第一次平衡相比,NO2的体积分数
A.不变 B.增大 C.减小 D.无法判断
57. 右图为可逆反应:A(s)+D(g)
右图为可逆反应:A(s)+D(g)
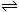 E(g);△H<0的逆反应速率随时间的变化情况,试根据图中曲线判断下列说法中不正确的是
E(g);△H<0的逆反应速率随时间的变化情况,试根据图中曲线判断下列说法中不正确的是
A.t3时刻可能采取的措施是减小c(D)
B.t5时刻可能采取的措施是升温
C.t7时刻可能采取的措施是减小压强
D.t5~t6时间段平衡向逆反应方向移动
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com