
题目列表(包括答案和解析)
25.(1)3.6 mol (2分)
(2)≥0 (3分)(说明:答“任意值”可得分)
(3)3.6 mol< n (SO3)≤4 mol(3分)
24、⑴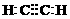 ⑵H2 ⑶Fe2O3若CuO ⑷C+H2O
⑵H2 ⑶Fe2O3若CuO ⑷C+H2O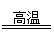 CO+H2
CO+H2
23.⑴SiO2 ⑵无机非金属材料
(2)SiCl4+2H2O=SiO2+4HCl或SiCl4+3H2O=H2SiO3+4HCl;NH3+HCl=NH4Cl
22.(1)S、Al(2分)(说明:写对1个得1分)
(2)Na、Al、S、O(2分)
(3)2Na2O2 +2CO2 = 2Na2CO3 + O2(2分)
(4)3S
+ 6OH- = 2S2- + 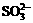 + 3H2O(2分)
+ 3H2O(2分)
21、⑴2Na+2H2O=2NaOH+H2↑
⑵验纯,用向下排气法收集一试管氢气,用拇指堵住,移近火焰,移开拇指点火。若听到轻微的“扑”声,则表明H2纯净。
⑶较多的钠与水反应放出大量的热,使试管内H2与O2的混和气点燃而爆炸。
⑷钠比水轻,比苯重,落在苯水交界处。钠与H2O反应产生的H2使钠浮起,脱离水面,反应停止;当钠表面的H2逸出,钠又回落,与水反应,如此反复,就可减慢Na与H2O反应速度。
20.(1)CuO (2分) 调节溶液pH至4-5,除去Fe3+(2分)(答降低溶液酸度,除去Fe3+可得分)
(2)4OH--4e- = O2↑+2H2O (2分) 2Cu2++2H2O2Cu+O2↑+4H+(2分)(不配平、条件错误不得分)
(3) (2分)
(2分)
19.(1)②(2分)
(2) ×100% (2分)(说明:答
×100% (2分)(说明:答 得分) 偏高(2分)
得分) 偏高(2分)
29、(11分)分子式为C13H16O2的惕各酸苯乙酯广泛用于香精的调香剂。已知:
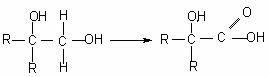
为了合成该物,某实验室的科技人员设计了下列合成路线:
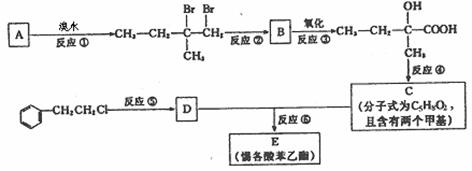
试回答下列问题:
(1) 试写出:A的结构简式_______________;B的结构简式________________。
(2) 反应②中另加的试剂是_______________;反应④的一般条件是______________。
(3) 试写出反应生成E的化学方程式:____________________________________________。
(4) 上述合成路线中属于取代反应的是 (填编号)。
 高三理综化学科第四次月考试卷
高三理综化学科第四次月考试卷
28、(14分)已知X、Y、Z、W四种元素是元素周期表中连续三个短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的核外电子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍,试推断:
(1)X、Z二种元素的元素符号:X_________Z__________
(2)由以上元素中的两种元素组成的能溶于水且水溶液显碱性的化合物的电子
式分别为__________________、___________________、___________________
(3)由X、Y、Z所形成的常见离子化合物是___________,它与W的最高价氧化
物的水化物的浓溶液加热时反应的离子方程式__________
(4)在由X、Y、Z、W四种元素形成的常见化合物或单质中,不能形成的晶体类型是_________.
27、(23分)Ⅰ:(10分)t℃时,将3molA和2molB气体通入体积为2L的密闭容器中(容积不变),发生如下反应:3A(气)+B(气) 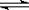 xC(气),2min时反应达到平衡状态(温度不变),剩余1.8molB,并测得C的浓度为0.4mol/L,请填写下列空白:
xC(气),2min时反应达到平衡状态(温度不变),剩余1.8molB,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)x=__________。
(2)比较达到平衡时,A、B两反应物的转化率之比为α(A):α(B)= ;
(3)若继续向原平衡混合物的容器中通入少量氦气(氦气和A、B、C都不反应)后,下列说法中正确的是____________(填写字母序号)
A.化学平衡向正反应方向移动 B.化学平衡向逆反应方向移动
C.化学平衡不会发生移动 D.正、逆反应的化学反应速率保持不变
(4)在t℃时,若向原平衡混合物的容器中再充入amolC,欲使达到新的平衡时,各物质的物质的量分数与原平衡相同,则至少应再充入____ ______(填A或B)________mol(用a表示)。
Ⅱ:(13分)(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,16.0gN2H4在氧气中完全燃烧生成氮气,放出热量312kJ
(25℃时),N2H4完全燃烧反应的热化学方程式是 。
(2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%-30%的KOH溶液。
肼-空气燃料电池放电时:
 正极的电极反应式是
。
正极的电极反应式是
。
负极的电极反应式 。
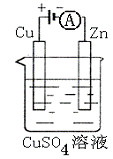
(3)右图是一个电化学过程示意图。
①锌片上发生的电极反应是 。
②假设使用肼-空气燃料电池作为本过程中的电源,
铜片的质量变化128g,则肼一空气燃料电池理论
上消耗标准状况下的空气 L
(假设空气中氧气体积含量为20%)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com