
题目列表(包括答案和解析)
17.X、Y、Z为短周期元素,X的最外层电子数是Y原子最外层电子数的2倍,Y的原子序数比X的原子序数多5,Z原子的最外层电子数比Y多3。下列叙述正确的是( )
A.原子半径的大小顺序:Y>Z>X
B.Z单质与X单质直接反应可生成两种化合物
C.工业上,电解X和Y形成的化合物制取Y单质
D.Y、Z元素的最高价氧化物对应的水化物不能互相反应
16.有下列五个化学方程式(X、Y、Z均为正值):
 ①C2H2(g)+H2(g) C2H4(g)
①C2H2(g)+H2(g) C2H4(g)
|
 ②CH4(g)
H2(g)+
②CH4(g)
H2(g)+ C2H4(g)
C2H4(g)
 ③C(s)+2H2(g) CH4(g);△H=-X kJ·mol-1
③C(s)+2H2(g) CH4(g);△H=-X kJ·mol-1
 ④C(s)+
④C(s)+ H2(g)
H2(g)  C2H2(g);△H=-Y kJ·mol-1
C2H2(g);△H=-Y kJ·mol-1
 ⑤C(s)+H2(g)
⑤C(s)+H2(g)
 C2H4(g);△H=-Z kJ·mol-1
C2H4(g);△H=-Z kJ·mol-1
当温度下降时①式平衡向右移动,②式平衡向左移动。据此判定③-⑤式中关于X、Y、Z的大小顺序排列正确的是 ( )
A.X>y>Z B.X>Z>Y C.Y>X>Z D.Z>X>Y
15. 在一定温度下,向体积恒定为2L的密闭容器里充入2mol M和一定量的N,发生如下反应:M(g)+N(g) E(g);当反应进行到4min时达到平衡,测知M的浓度为0.2mol·L-1。下列说法正确的是 ( )
在一定温度下,向体积恒定为2L的密闭容器里充入2mol M和一定量的N,发生如下反应:M(g)+N(g) E(g);当反应进行到4min时达到平衡,测知M的浓度为0.2mol·L-1。下列说法正确的是 ( )
A.4min时,M的转化率为80%
B.4min时,用M表示的反应速率为0.8mol·L-1·min-1
C.4min后,向容器中充入不参与反应的稀有气体,M的物质的量减小
D.2min时,M的物质的量浓度为0.6mol·L-1
14. 以水为溶剂进行中和滴定的原理是:H3O++OH-
以水为溶剂进行中和滴定的原理是:H3O++OH- 2H2O。已知液态SO2和纯水的导电性相近,因为液态SO2也能发生自电离:2SO2 SO +SO2+;△H>0。下列叙述中,错误的是 ( )
+SO2+;△H>0。下列叙述中,错误的是 ( )
A.若以液态SO2为溶剂,用SOCl2滴定Na2SO3,该滴定反应可以表示为:
SO +SO2+
+SO2+ 2SO2
B.在一定温度下,液态SO2中c(SO )与c(SO2+)的乘积是一个常数
)与c(SO2+)的乘积是一个常数
C.液态SO2中自电离的存在,说明SO2是离子化合物
D.适当升高温度,液态SO2的导电能力增强
12.水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O +O2+xOH-
+O2+xOH- Fe3O4+S4O +2H2O,下列说法中,正确的是 ( )
+2H2O,下列说法中,正确的是 ( )
A.每生成1mol Fe3O4,反应转移的电子总数为4mol
B.Fe2+和S2O 都是还原剂
都是还原剂
C.1mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为1/3mol
D.x=2
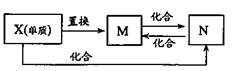 13.右图中,M、N为含X元素的常见化合物。
13.右图中,M、N为含X元素的常见化合物。
则X元素为 ( )
A.Fe B.Cu
C.N D.C
11.某黄色溶液中可能含有下列离子:K+、NH 、Fe3+、Ba2+、SO
、Fe3+、Ba2+、SO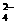 、HCO
、HCO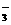 、Cl-、S2-,为检验其成分,先对溶液进行初步分析。下列判断中,不正确的是 ( )
、Cl-、S2-,为检验其成分,先对溶液进行初步分析。下列判断中,不正确的是 ( )
A.溶液中存在大量Fe3+ B.溶液中可能存在大量Ba2+
C.溶液中不存在大量HCO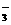 和S2- D.溶液可能呈强碱性
和S2- D.溶液可能呈强碱性
10.实验测得气态无水氯化铝在1.01×105Pa、不同温度(t3>t2>t1)时的密度(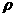 )和气体摩尔体积(Vm)为
)和气体摩尔体积(Vm)为
|
t/℃ |
t1 |
t2 |
t3 |
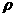 /g·L-1 /g·L-1 |
5.00 |
2.67 |
1.48 |
|
Vm/L·mol-1 |
53.4 |
70.0 |
90.0 |
可见,t2℃时无水氯化铝存在形式的化学式为 ( )
|
C.Al3Cl9 D.Al2Cl6
|
9.下列离子方程式中,正确的是 ( )
A.向Mg(HCO3)2溶液中加入过量的NaOH溶液
Mg2++2HCO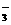 +2OH-
+2OH-
MgCO3↓+CO +2H2O
+2H2O
B.向NH4Al(SO4)2溶液中滴入Ba(OH)2使SO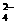 反应完全
反应完全
2Ba2++4OH-+Al3++2SO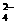
2BaSO↓+AlO +2H2O
+2H2O
C.足量的CO2通入饱和碳酸钠溶液中:CO2+CO +H2O
+H2O 2HCO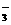
D.向Fe(NO3)2溶液中加入稀盐酸:3Fe2++4H++NO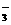
3Fe3++NO↑+2H2O
8.实验室用质量分数为98%、密度为1.84g·cm-3的浓硫酸配制100g 10%H2SO4溶液。配制过程中需要用到的仪器有: ( )
①托盘天平 ②10mL量筒 ③100mL量筒 ④烧杯
⑤玻璃棒 ⑥100mL容量瓶 ⑦胶头滴管
A.②③④⑤⑦ B.②④⑤⑥⑦ C.①④⑤⑥⑦ D.②③④⑤⑥⑦
7.下列实验操作中,不会发生安全事故的是 ( )
A.用无水醋酸钠和碱石灰混合加热制取甲烷,直接点燃,观察燃烧的现象
B.用消石为与NH4Cl固体混和加热,产生的气体用导管直接通入水中制取浓氨水
C.没入水下切割、取用少量白磷,剩余的白磷立即放回原试剂瓶中
D.做完铜与浓硫酸反应实验的试管,直接用大量水冲洗
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com