
题目列表(包括答案和解析)
2.关于胶体和溶液的叙述中正确的是
A.胶体带电荷,而溶液呈电中性
B.胶体加入某些盐可产生沉淀,而溶液不能
C.胶体是一种介稳性的分散系,而溶液是一种非常稳定的分散系
D.胶体能够发生丁达尔现象,溶液也能发生丁达尔现象
1.设NA代表阿伏加德罗常数,下列说法正确的是
A.5.6 g铁与足量盐酸反应转移的电子数为0.3NA
B.100 mL 2.0 mol/L的盐酸与醋酸溶液中氢离子均为0.2NA
C.标准状况下,22.4 L氦气与22.4 L氟气所含原子数均为2 NA
D.常温常压下,20 g重水(D2O)中含有的电子数为10NA
24.(6分)将一定量氧化铜粉末加入到100mL0.5mol/L的硫酸中,微热至氧化铜全部溶解,再向该蓝色溶液中加入铁粉10克充分反应后过滤,烘干,得干燥的固体物质仍为10克。
(1)参加反应的铁为多少克?
(2)原加入的氧化铜为多少克?
(3)最后得到的溶液仍为100mL,其物质的量浓度为多少?
23.(5分)(1)可以验证镁、铝的金属性强弱的实验是 。
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
(2)现有MgCl2溶液、AlCl3溶液、NaOH溶液、氨水、盐酸等几种物质,试设计实验方案证明镁、铝的金属性强弱。
22.(9分)短周期元素形成的纯净物A、B、C、D、E是转化关系如下图所示,物质A与物质B之间的反应不在溶液中进行(E可能与A、B两种物质中的某种相同)。
|


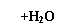
|



|
|


|


请回答下列问题:
(1)若C是离子化合物,D是一种强碱,写出C的一种化学式 。
(2)若E的水溶液呈现弱酸性,D是既能溶于强酸、又有溶于强碱的化合物。
①用电离方程式解释D既能溶于强酸,又能溶于强碱的原因。
。
②用等式表示E与NaOH溶液反应后生成正盐的溶液中所有离子浓度之间的关系
。
(3)若C是一种气体,D是一种强酸,则:
①C与水反应的化学方程式为 。
 ②有人认为“浓H2SO4可以干燥气体C”。某同学
②有人认为“浓H2SO4可以干燥气体C”。某同学
为了验证该观点是否正确,用右图装置进行实验。
实验过程中,浓H2SO4中未发现有气体逸出,且变
为红棕色,则你得出的结论是 。
③已知常温下物质A与物质B生成1mol气体C的焓变为-57.07kJ, 1 mol气体C与H2O反应生成D溶液和E气体的焓变为-46kJ,写出物质A与物质B及水生成D溶液的热化学方程式 。
21.(4分)某化学反应的反应物和产物如下:
KMnO4 + KI+ H2SO4→ MnSO4 + I2 + KIO3 + K2SO4 + H2O
(1)该反应的氧化剂是 (2)如果该反应方程式中I2和KIO3的系数都是5
①KMnO4的系数是 ②在上面的化学反应式上标出电子转移的方向和数目。
(3)如果没有对该方程式中的某些系数作限定,可能的配平系数有许多组。原因是
。
20.(5分)下列中学化学中常见物质的转化关系图中,反应条件及部分反应物和产物未全部注明,已知A、D为金属单质,其他为化合物。试推断:
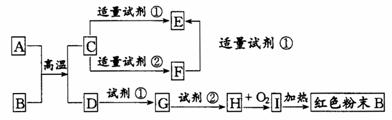
(1)写出物质的化学式:
A:_______ C:________ I:________
|
座 号 |
|
(2)写出下列反应的方程式:
C→F的离子方程式
H→I的化学方程式
19. (7分)X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系
(7分)X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系
(部分反应物、产物及反应条件已略去)。请回答:
(1)W的电子式是 。(2)X与Y在溶液中反应的离子方程式是
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用右图装置(夹持固定装置已略去)进行实验,装置III中产生白色沉淀,装置V中可收集到一种无色气体。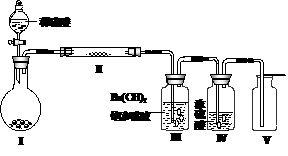 ①装置Ⅰ中反应的化学方程式是
①装置Ⅰ中反应的化学方程式是
。
装置Ⅱ中物质的化学式是 。
②用Ⅹ含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置Ⅴ中气体,该化合物的化学式是 ,所需仪器装置是 (从上图选择必要的装置,填写编号)。
18.(9分)某化学小组欲探究铁及其化合物的氧化性和还原性,请回答下列问题:
(1)除胶头滴管外,你认为本实验必不可缺少的一种玻璃仪器是 。
(2)请帮他们完成以下实验报告:
实验目的:探究铁及其化合物的氧化性和还原性。
试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、铜片。
实验记录(划斜线部分不必填写):
|
序号 |
实验内容 |
实验现象 |
离子方程式 |
实验结论 |
|
① |
在FeCl2溶液中滴入适量氯水 |
溶液由浅绿色变为棕黄色 |
|
Fe2+具有还原性 |
|
② |
在FeCl2溶液中加入锌片 |
|
Zn+Fe2+=Zn2++Fe |
|
|
③ |
在FeCl3溶液中加入足量铁粉 |
|
Fe+2Fe3+=3 Fe2+ |
Fe3+具有氧化性 |
|
④ |
|
|
|
Fe3+具有氧化性 |
实验结论:Fe只有还原性,Fe3+只有氧化性,Fe2+既有氧化性,又有还原性。
(3)根据以上结论判断,下列物质中既有氧化性,又有还原性的有: 。(填序号)
A.Cl2 B.Na C.Na+ D.Cl- E.SO2 F.NO2
(4)亚铁盐在溶液中易被氧化,而实验室中需要纯净的亚铁盐溶液。那么保存亚铁盐溶液时应该 防止亚铁盐被氧化。
17.(7分)实验室要配置100mL1mol./L的KOH溶液,试回答
(1)用不到的仪器是
A 烧杯 B 250mL容量瓶 C天平 D胶头滴管 E玻璃棒 F 100mL容量瓶 G漏斗
(2) 配置时要称取KOH的质量为
(3)从下面选出正确的操作并写出正确的顺序 (填序号)。
A洗涤 B干燥 C量取 D称量 E 定容 F转移溶液 G稀释 H溶解 I冷却 J摇匀
(4)实验中出现下列情况要如何处理?
A 加蒸馏水时不小心加过了刻度线 ;
B 加蒸馏水到离刻度线1~2cm处时应 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com