
题目列表(包括答案和解析)
4.下列实验设计能够成功的是:
|
|
实验目的 |
实验步骤及现象 |
|||
|
A |
检验亚硫酸钠试样是否变质 |
 |
|||
|
B |
检验某卤代烃是否是氯代烃 |
 |
|||
|
C |
证明酸性条件下H2O2氧化性比I2强 |
 |
|||
|
D |
除去氯化钠溶液中的少量硫酸钠 |
溶液 |
3.下列说法正确的是:
A.化学式符合XOH(X代表某一元素)的物质一定是碱
B.分子式为C6H6的物质一定是苯
C.最简单的烯烃一定是乙烯
D.含碳量最高的烃一定是乙炔
2.《新科学家》网站报道,科学家通过电解Fe2O3-SiO2-CaO的熔融液(1600℃)制得了铁和氧气。与常规方法比,将该方法用于工业上大规模冶铁,以下优点分析错误的是:
A.副产物可做工业用氧 B.大幅度降低能耗
C.大幅度降低温室气体的排放 D.制得更纯的铁
1.新华社2007年3月21日电,全国科学技术名词审定委员会21日公布:111号元素(符号为Rg)的中文名称为“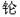 ”(读音为伦)。下列说法正确的是:
”(读音为伦)。下列说法正确的是:
A.111号元素是第6周期、第ⅠA族的金属元素 B.111号元素属于过渡元素
C.111号元素为非金属元素 D.111号元素质量数为111
29、(共15分)
(1)(共4分)C7H8O (2分) ,  (2分)
(2分)
(2)(共4分)
CH3COOH + 
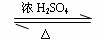
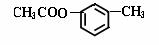 + H2O (3分)
+ H2O (3分)
酯化反应 或取代反应(1分)
(3)(共7分) 6种(3分);
 、
、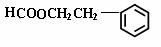 (写对一个2分,共4分)
(写对一个2分,共4分)
28.(13分)(1)、 IA (1分 ) 。 (2)、 物理变化 (1分) 。
(3).2NaCl+2H2O=2NaOH+H2↑+Cl2↑;(2分) 585 t。(3分)
(4).反应② NaOH+SO2=NaHSO3 (2分);反应④NaHSO3+HCl=NaCl+H2Cl+SO2↑。(2分)
(5)、 C 、D 。(其余每空2分)
(1)B.C D.O E.Al
(2)二氧化碳、乙炔等直线型分子的电子式
(3)NH4HCO3 (NH4)2CO3等。
(4)HCO3-+ OH-== H2O + CO32-
(5)2Al+Fe2O3  Al2O3
+ 2Fe
Al2O3
+ 2Fe
(6) N2 + 3H2 2NH3
2NH3
(7) 正极:O2 + 4e- + 2H2O == 4OH-
27.(共17分)
(1)①FeS、Fe(2分) B装置增重、量气管有气体(2分)。
② V/400(3分)
(2)洗气瓶(1分) 2OH-+H2S== 2H2O+S2-(2分)
(3)证明H2S已被完全吸收(2分) 黑色沉淀(1分)
(4)硫(2分) 漏斗、玻璃棒(2分)
22. (10分) a、b、c、d、e是短周期元素,周期表中a与b、b与c相邻;a与e的最外层电子数之比为2:3,b的最外层电子数比e的最外层电子数少1个;常见化合物d2c2与水反应生成c的单质,且溶液使酚酞试液变红。
(1) e的元素符号是__________。
(2)a、b、c的氢化物稳定性顺序为(用分子式表示)______________________;b的氢化物和b的最高价氧化物的水化物反应生成Z,则Z中的化学键类型为____________,Z的晶体类型为_____________;ab-离子的电子式为____________。
(3)一定量的d2c2与ac2反应后的固体物质,恰好与0.8 mol稀盐酸溶液完全反应,并收集到0.25 mol气体,则用物质的量表示该固体物质的组成为 _、 ____________。
21.(12分)短周期元素的单质X、Y、Z在通常状况下均为气态,并有下列转化关
 系(反应条件已略去):
系(反应条件已略去):
已知: a.常见双原子单质分子中,X分子含共价键最多。
b.甲分子中含10个电子,乙分子含有18个电子。
(1)X的电子式是 。
 (2)实验室可用下图所示装置(缺少收集装置,夹持固定装置略去)制备并收集甲。
(2)实验室可用下图所示装置(缺少收集装置,夹持固定装置略去)制备并收集甲。
①在图中方框内绘出用烧瓶收集甲的仪器装置简图(夹持固定装置略去)。
②试管中的试剂是(填写化学式) 。
③烧杯中溶液由无色变为红色,其原因用电离方程式表示为 。
(3)磷在Z中燃烧可生成两种产物,其中一种产物丁的分子中各原子最外层不全是8电子结构,丁的化学式是 。
(4)n mol丁与n mol丙在一定条件下反应,生成4n mol乙和另一化合物,该化合物蒸气的密度是相同状况下氢气的174倍,其化学式是 。
20.(8分)有一无色透明溶液,欲确定是否含有下列离子:Na+、Mg2+、Al3+、Fe2+、Ba2+、NO 、SO
、SO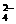 、Cl-、I-、HCO
、Cl-、I-、HCO ,取该溶液实验如下:
,取该溶液实验如下:
|
实验步骤 |
实验现象 |
|
①取少量该溶液,加几滴甲基橙 |
溶液变红色 |
|
②取少量该溶液,浓缩,加Cu片和浓H2SO4,加热 |
有无色气体产生,后在空气中又变成红棕色 |
|
③取少量该溶液,加BaCl2溶液 |
有白色沉淀生成 |
|
④取③中上层清液,加AgNO3溶液 |
有白色沉淀生成,且不溶于HNO3 |
|
⑤取少量该溶液,加NaOH溶液 |
有白色沉淀生成,当NaOH过量时沉淀部分溶解 |
(1)溶液中肯定存在的离子是________________________。
(2)溶液中肯定不存在的离子是________________________。
(3)为进一步确定其他离子,应该补充的实验步骤是______ _____。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com